Clear Sky Science · ar
إعادة توظيف أدوية موافق عليها من إدارة الغذاء والدواء كعوامل حماية عصبية متعددة الأهداف لمرض الزهايمر عبر الفحص الحاسوبي والتحقق التجريبي
لماذا قد تساعد أدوية قديمة ذاكرة تتلاشى
يسلب مرض الزهايمر الملايين من ذاكرتهم واستقلالهم، والأدوية الحالية تخفف الأعراض لفترة محدودة فقط. تطوير أدوية جديدة بالكامل عملية بطيئة ومكلفة ومحفوفة بالمخاطر. تطرح هذه الدراسة سؤالاً بسيطاً لكنه قوي: هل يمكننا البحث بين الأدوية التي تمت الموافقة عليها واختبار سلامتها لأمراض أخرى، وإيجاد أدوية تحمي الدماغ المسن بهدوء وعلى عدة واجهات في وقت واحد؟
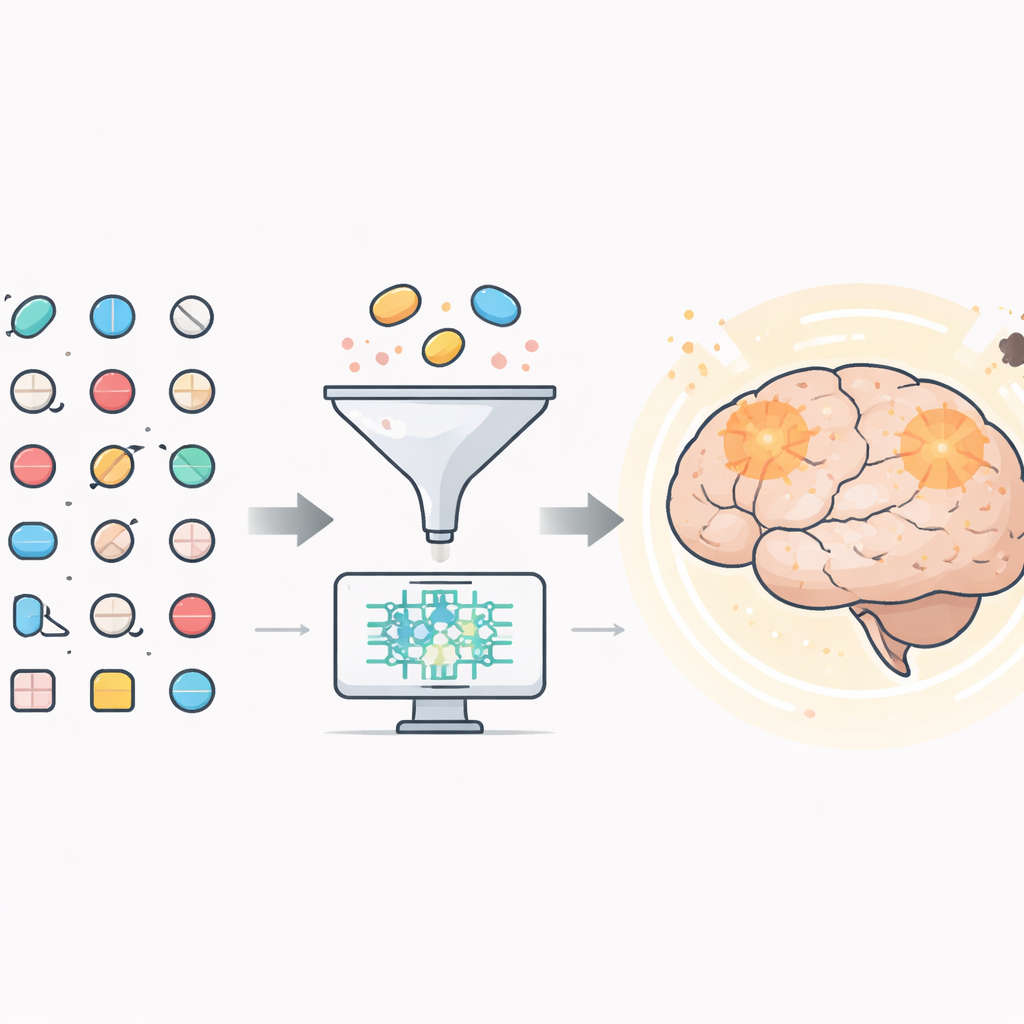
البحث عن مساعدين خفيين في أدوية موجودة
بدأ الباحثون بأكثر من 1500 دواء تمت الموافقة عليها بالفعل من قبل إدارة الغذاء والدواء الأمريكية. باستخدام أدوات حاسوبية، قاموا أولاً بترشيح أي مركبات من غير المرجح أن تصل إلى الدماغ، لأن علاج الزهايمر يجب أن يعبر الحاجز الدموي الدماغي. اجتاز هذا الاختبار حوالي 600 مرشح. بعد ذلك، استخدموا نماذج ثلاثية الأبعاد مفصّلة لإنزيم دماغي رئيسي يُسمى BACE1، لمعرفة أي الأدوية يمكن أن تتشبث بموقعه النشط بطريقة مستقرة ومناسبة. يعد BACE1 مهماً لأنه يساعد في قطع بروتين أكبر إلى بيتا أميلويد، الجزئية اللاصقة التي تتجمع لتشكل لويحات في أدمغة المصابين بالزهايمر.
إيجاد مرشح دوائي متعدد المهام
من هذا الفحص الافتراضي تم تحديد 14 نتيجة واعدة، واخترعت أربعة للدراسة عن قرب بناءً على مدى ملاءمتها للإنزيم وخصائصها الكيميائية ومعرفة سلامتها في الاستخدام طويل الأمد. ثم أجرت الفريق محاكاة حاسوبية طويلة لمراقبة سلوك كل مرشح أثناء ارتباطه بـ BACE1 مع مرور الوقت. حافظت الأربعة كلها على ثبات داخل جيب الإنزيم، لكن مركباً واحداً، الموسوم ZINC000019796155، برز لتفاعلاته المواتية مع أهم مناطق BACE1. أشارت هذه المحاكاة إلى أن الدواء قد يقلل قدرة الإنزيم على إنتاج بيتا أميلويد دون إزعاج استقرار البروتين نفسه.
اختبار كيف يحمي الدواء كيمياء الدماغ
التنبؤات الحاسوبية خطوة أولى فقط، لذا اختبر العلماء المرشحين الأربعة في تجارب مخبرية. كلهم أبطأوا نشاط BACE1، وأظهر ZINC000019796155 أقوى تأثير، وإن كان أضعف من مثبطات تجريبية ذات فعالية عالية. والأهم من ذلك، عندما فحصوا عمليات أخرى مرتبطة بالزهايمر، وجدوا أن هذا المركب نفسه يثبط إنزيمًا آخر، بوتيريل كولينستراز، الذي يزداد نشاطه مع تقدم المرض ويحلّل ناقلاً كيميائياً مرتبطاً بالذاكرة. وقد خفض أيضاً تكتل بيتا أميلويد في أنبوب اختبار وأظهر نشاطاً مضاداً للأكسدة قوياً، ما يعني قدرته على تحييد الجذور الحرة الضارة التي تسهم في موت خلايا الدماغ.
حماية الخلايا العصبية من الضرر
لمعرفة كيف تترجم هذه الأفعال داخل الخلايا الحية، عرّض الفريق خلايا شبيهة بالعصب البشري مشتقة من الإنسان لبيروكسيد الهيدروجين، وهو مركب يحاكي الإجهاد التأكسدي الموجود في أدمغة الزهايمر وعادة ما يقتل العديد من الخلايا. عندما كانت الخلايا معالجة مسبقاً بـ ZINC000019796155، نجت نسبة أكبر بكثير. وكشفت تحليلات لاحقة لبروتينات الخلايا أن المركب خفّض مؤشرات الموت الخلوي المبرمج وخفض مستويات عوامل رئيسية في تكوّن اللويحات والتشابكات، بما في ذلك سلف بيتا أميلويد، وإنزيم BACE1 نفسه، وشكل معدل من بروتين تاو يميل لتشكيل ألياف ملتوية داخل الخلايا العصبية. وفي الوقت نفسه، عزز إشارات على طول مسارات معروفة للحفاظ على تاو في حالة أكثر صحة وأقل لزوجة.
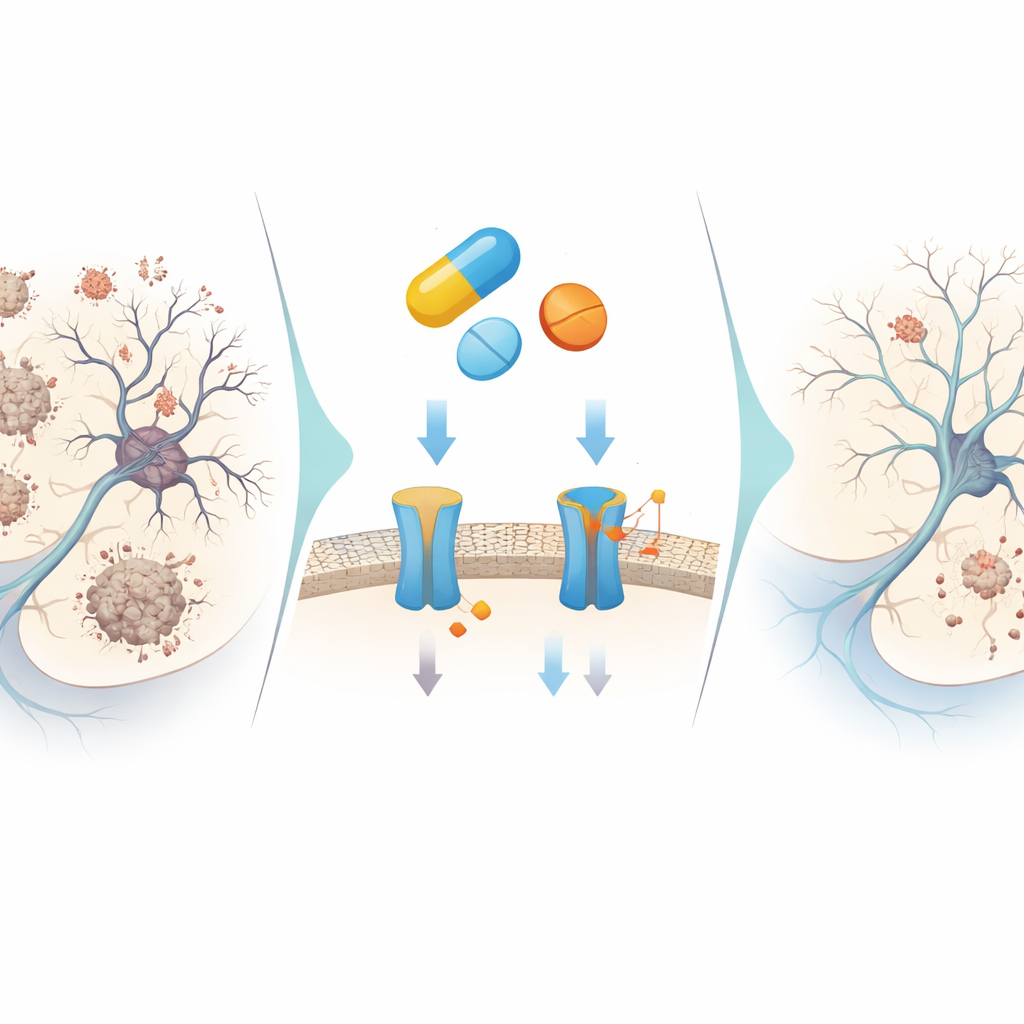
ما الذي قد يعنيه هذا للعلاج المستقبلي
بالنظر إلى النتائج مجتمعة، تشير الدراسة إلى أن ZINC000019796155، دواء معتمد بالفعل، يمكن أن يعمل كأداة جزيئية متعددة الصغر: يعيق جزئياً إنتاج بيتا أميلويد، يبطئ تجمّعه، يحد من تحلل ناقل ذاكرة أساسي، يطمس المؤكسدات الضارة، ويساعد على توجيه الخلايا العصبية بعيداً عن مسارات الانتحار الخلوي وتكوين التشابكات. تأثيراته معتدلة بدلاً من مفرطة، وهو ما قد يكون أكثر أماناً في ضوء الإخفاقات السابقة لمثبطات BACE1 القوية جداً. وعلى الرغم من أن المركب سيحتاج إلى ضبط كيميائي واختبارات دقيقة في الحيوانات ولاحقاً لدى البشر، توضح هذه الدراسة كيف أن الفحص الحاسوبي الذكي الممزوج بتجارب مخبرية موجهة يمكن أن يكشف أدواراً جديدة للحماية الدماغية لأدوية مألوفة، فاتحاً مساراً أكثر كفاءة نحو علاجات مستقبلية للزهايمر.
الاستشهاد: Phemphunananchai, K., Waiwut, P., Phetcharaburanin, J. et al. Repurposing FDA-approved drugs as multi-target neuroprotective agents for Alzheimer’s disease via computational screening and experimental validation. Sci Rep 16, 11688 (2026). https://doi.org/10.1038/s41598-026-46708-2
الكلمات المفتاحية: مرض الزهايمر, إعادة توظيف الأدوية, تثبيط BACE1, علاج متعدد الأهداف, حماية عصبية