Clear Sky Science · ru
Переназначение одобренных FDA препаратов как многоцелевых нейропротективных средств при болезни Альцгеймера с помощью компьютерного скрининга и экспериментальной валидации
Почему старые лекарства могут помочь угасающей памяти
Болезнь Альцгеймера лишает миллионы людей воспоминаний и независимости, и существующие препараты лишь временно облегчают симптомы. Разработка новых лекарств медленная, дорогая и рискованная. В этом исследовании поставлен простой, но мощный вопрос: можно ли просмотреть уже одобренные и проверенные с точки зрения безопасности препараты, назначенные для других состояний, и найти те, которые тихо защищают стареющий мозг по нескольким направлениям одновременно?
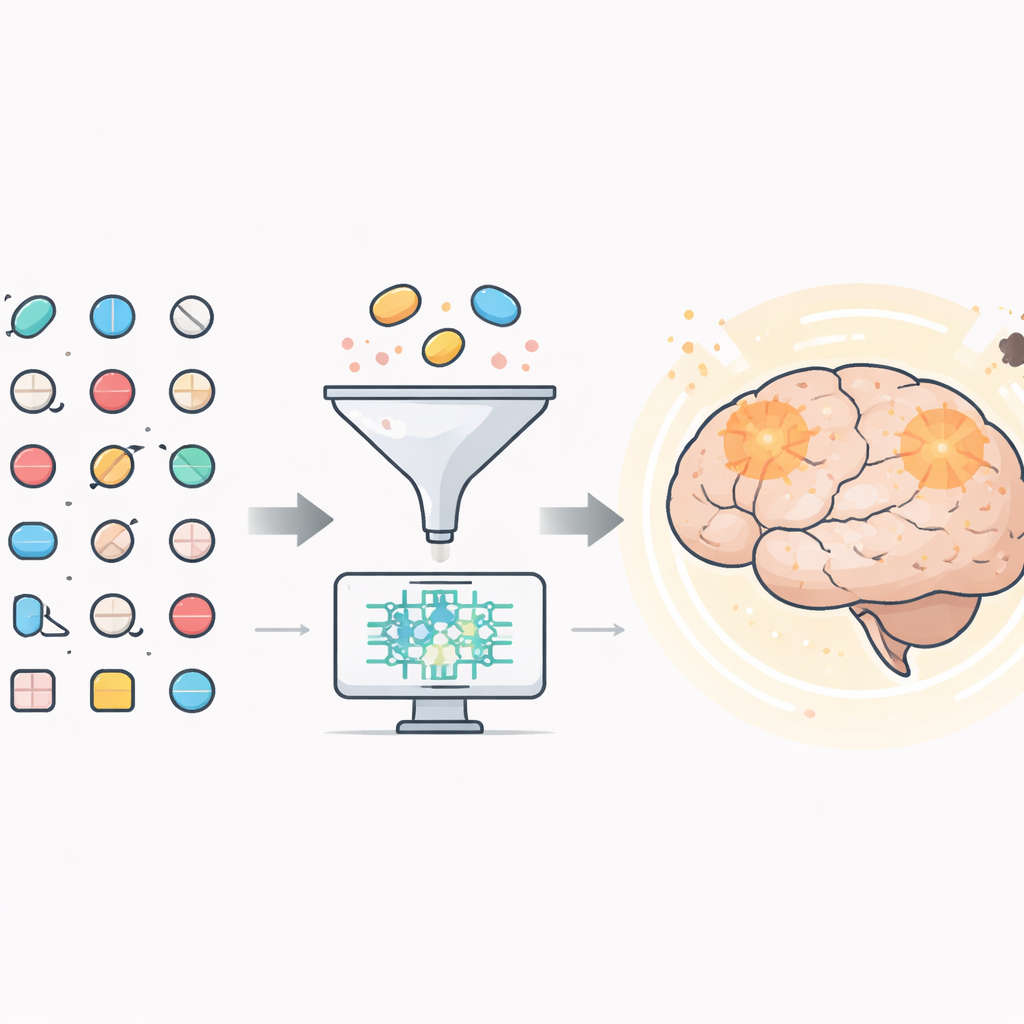
Поиск скрытых помощников среди существующих препаратов
Исследователи начали с более чем 1500 препаратов, уже одобренных Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США. С помощью компьютерных инструментов они сначала отфильтровали соединения, которые вряд ли смогут добраться до мозга, поскольку лечение болезни Альцгеймера должно преодолевать гематоэнцефалический барьер. Около 600 кандидатур прошли этот отбор. Затем использовали детальные 3D‑модели ключевого мозгового фермента, называемого BACE1, чтобы увидеть, какие препараты могут прочно и плотно связываться с его активным участком. BACE1 важен тем, что он участвует в расщеплении более крупного белка до амилоид‑бета — липкого фрагмента, который слипается в бляшки в мозге людей с болезнью Альцгеймера.
Поиск многофункционального кандидата
Из этого виртуального скрининга было выделено 14 перспективных попаданий, из которых четыре выбрали для более тщательного изучения на основании того, как хорошо они вписываются в фермент, их химических свойств и известной безопасности при длительном применении. Команда затем провела долгие компьютерные симуляции, чтобы наблюдать за поведением каждого кандидата в связке с BACE1 во времени. Все четыре оставались стабильными в кармане фермента, но одно соединение, маркированное ZINC000019796155, выделилось благоприятными взаимодействиями с наиболее критическими участками BACE1. Эти симуляции предположили, что препарат может снизить способность фермента производить амилоид‑бета, не дестабилизируя сам белок.
Проверка того, как препарат защищает мозговую химию
Компьютерные прогнозы — лишь первый шаг, поэтому учёные протестировали четыре кандидата в лабораторных экспериментах. Все они замедляли активность BACE1, и ZINC000019796155 показал самый сильный эффект, хотя и слабее по сравнению с высокопотентными экспериментальными ингибиторами. Важно, что при изучении других процессов, связанных с Альцгеймером, выяснилось: этот же соединение ингибировало другой фермент — бутирылхолинэстеразу, активность которой возрастает по мере прогрессирования болезни и который разрушает медиатор, связанный с памятью. Оно также уменьшало агрегацию амилоид‑бета в пробирке и демонстрировало выраженную антиоксидантную активность, то есть могло нейтрализовать вредные свободные радикалы, способствующие гибели нервных клеток.
Защита нервных клеток от повреждения
Чтобы понять, как эти эффекты проявляются в живых клетках, команда подвергла полученные от человека нервоподобные клетки действию перекиси водорода, химического вещества, имитирующего окислительный стресс, наблюдаемый при Альцгеймере, и обычно убивающего многие клетки. Когда клетки предварительно обрабатывали ZINC000019796155, выживало значительно больше клеток. Дальнейший анализ белков клетки показал, что соединение снижало маркеры программируемой клеточной гибели и уменьшало уровни ключевых факторов, участвовавших в образовании бляшек и нейрофибриллярных клубков, включая предшественник амилоид‑бета, сам фермент BACE1 и модифицированную форму белка тау, склонную к образованию спиральных нитей внутри нейронов. При этом оно усиливало сигналы по путям, известным тем, что поддерживают тау в более здоровом, менее «липком» состоянии.
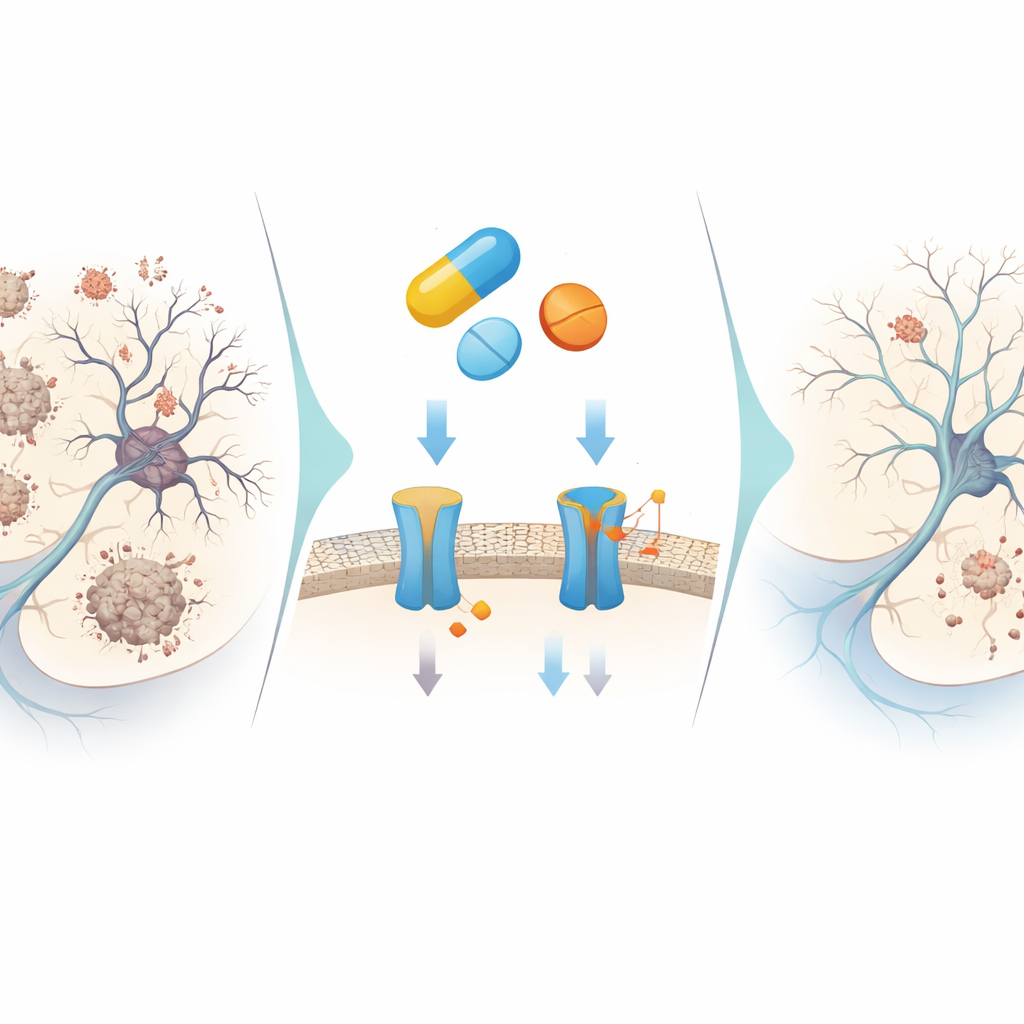
Что это может значить для будущего лечения
В сумме результаты указывают, что ZINC000019796155, уже одобренный препарат, может действовать как небольшой молекулярный мультитул: частично блокировать образование амилоид‑бета, замедлять его агрегацию, ограничивать расщепление ключевого медиатора памяти, гасить вредные окислители и помогать направлять нервные клетки от путей самоуничтожения и образования клубков. Его эффекты умеренные, а не экстремальные, что может оказаться безопаснее на фоне прежних неудач с чрезмерно сильными ингибиторами BACE1. Хотя соединение потребует химической доработки и тщательной проверки на животных и, в конечном итоге, на людях, это исследование иллюстрирует, как умный компьютерный отбор в сочетании с целенаправленными лабораторными экспериментами может выявить новые нейропротективные роли знакомых лекарств, открывая более эффективный путь к будущим терапиям при болезни Альцгеймера.
Цитирование: Phemphunananchai, K., Waiwut, P., Phetcharaburanin, J. et al. Repurposing FDA-approved drugs as multi-target neuroprotective agents for Alzheimer’s disease via computational screening and experimental validation. Sci Rep 16, 11688 (2026). https://doi.org/10.1038/s41598-026-46708-2
Ключевые слова: Болезнь Альцгеймера, репозиционирование лекарств, ингибирование BACE1, многоцелевое лечение, нейропротекция