Clear Sky Science · pt
Reaproveitamento de medicamentos aprovados pela FDA como agentes neuroprotetores multitarget para a doença de Alzheimer por triagem computacional e validação experimental
Por que remédios antigos podem ajudar uma memória que se apaga
A doença de Alzheimer rouba a memória e a independência de milhões de pessoas, e os medicamentos disponíveis hoje só aliviam os sintomas por um período limitado. Desenvolver fármacos novos é lento, caro e arriscado. Este estudo faz uma pergunta simples, porém poderosa: podemos buscar entre medicamentos já aprovados e testados quanto à segurança para outras condições e encontrar alguns que protejam discretamente o cérebro envelhecido em várias frentes ao mesmo tempo?
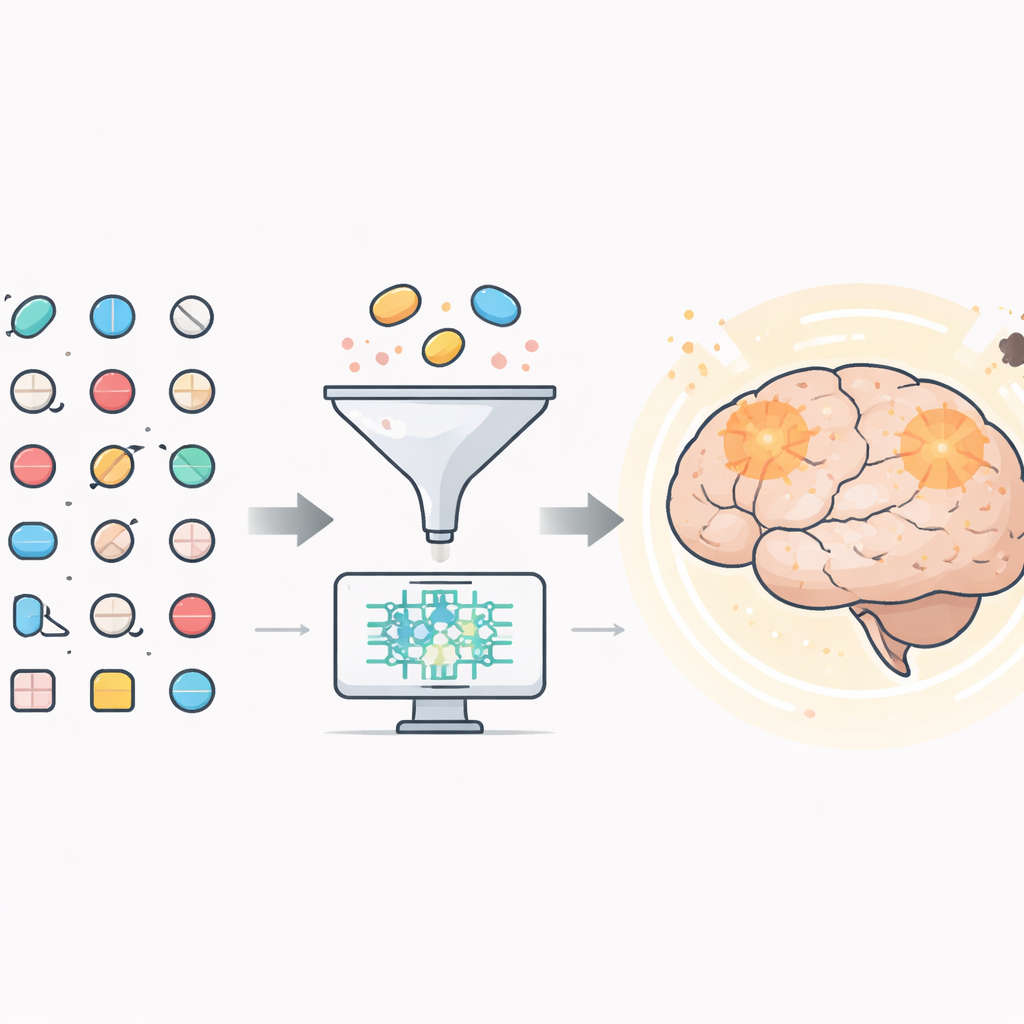
Procurando ajudantes ocultos em medicamentos existentes
Os pesquisadores começaram com mais de 1.500 medicamentos já aprovados pela Food and Drug Administration dos EUA. Usando ferramentas computacionais, primeiro filtraram qualquer composto pouco provável de alcançar o cérebro, já que um tratamento para Alzheimer precisa atravessar a barreira hematoencefálica. Cerca de 600 candidatos passaram nesse teste. Em seguida, utilizaram modelos 3D detalhados de uma enzima cerebral chave, chamada BACE1, para ver quais medicamentos podiam se prender ao sítio ativo de forma estável e ajustada. BACE1 é importante porque ajuda a cortar uma proteína maior em amyloid‑beta, o fragmento pegajoso que se aglomera em placas nos cérebros de pessoas com Alzheimer.
Encontrando um candidato multitarefa
Dessa triagem virtual surgiram 14 resultados promissores, e quatro foram escolhidos para estudo mais aprofundado com base em quão bem se encaixavam na enzima, suas características químicas e sua segurança conhecida em uso prolongado. A equipe então executou longas simulações computacionais para observar como cada candidato se comportava enquanto ligado à BACE1 ao longo do tempo. Todos os quatro se mantiveram estáveis no bolso da enzima, mas um composto, rotulado ZINC000019796155, destacou‑se por suas interações favoráveis com as regiões mais críticas da BACE1. Essas simulações sugeriram que o medicamento poderia reduzir a capacidade da enzima de produzir amyloid‑beta sem desestabilizar a própria proteína.
Testando como o medicamento protege a química cerebral
Previsões computacionais são apenas um primeiro passo, então os cientistas testaram os quatro candidatos em experimentos de laboratório. Todos reduziram a atividade da BACE1, e o ZINC000019796155 apresentou o efeito mais forte, embora ainda inferior ao de inibidores experimentais de alta potência. Importante, ao examinarem outros processos ligados ao Alzheimer, eles descobriram que esse mesmo composto inibia outra enzima, a butirilcolinesterase, que se torna mais ativa com o progresso da doença e degrada um mensageiro químico associado à memória. Também reduziu a agregação de amyloid‑beta em ensaio in vitro e mostrou forte atividade antioxidante, indicando que poderia neutralizar radicais livres danosos que contribuem para a morte de células cerebrais.
Protegendo os neurônios do dano
Para ver como essas ações se traduzem dentro de células vivas, a equipe expôs células semelhantes a neurônios derivadas de humanos a peróxido de hidrogênio, um químico que imita o estresse oxidativo observado em cérebros com Alzheimer e que normalmente mata muitas células. Quando as células foram pré‑tratadas com ZINC000019796155, muitas mais sobreviveram. Análises adicionais das proteínas celulares revelaram que o composto reduziu marcadores de morte celular programada e diminuiu os níveis de participantes-chave na formação de placas e emaranhados, incluindo o precursor da amyloid‑beta, a própria enzima BACE1 e uma forma modificada da proteína tau que tende a formar fibras torcidas dentro dos neurônios. Ao mesmo tempo, aumentou sinais em vias conhecidas por manter a tau em um estado mais saudável e menos aderente.
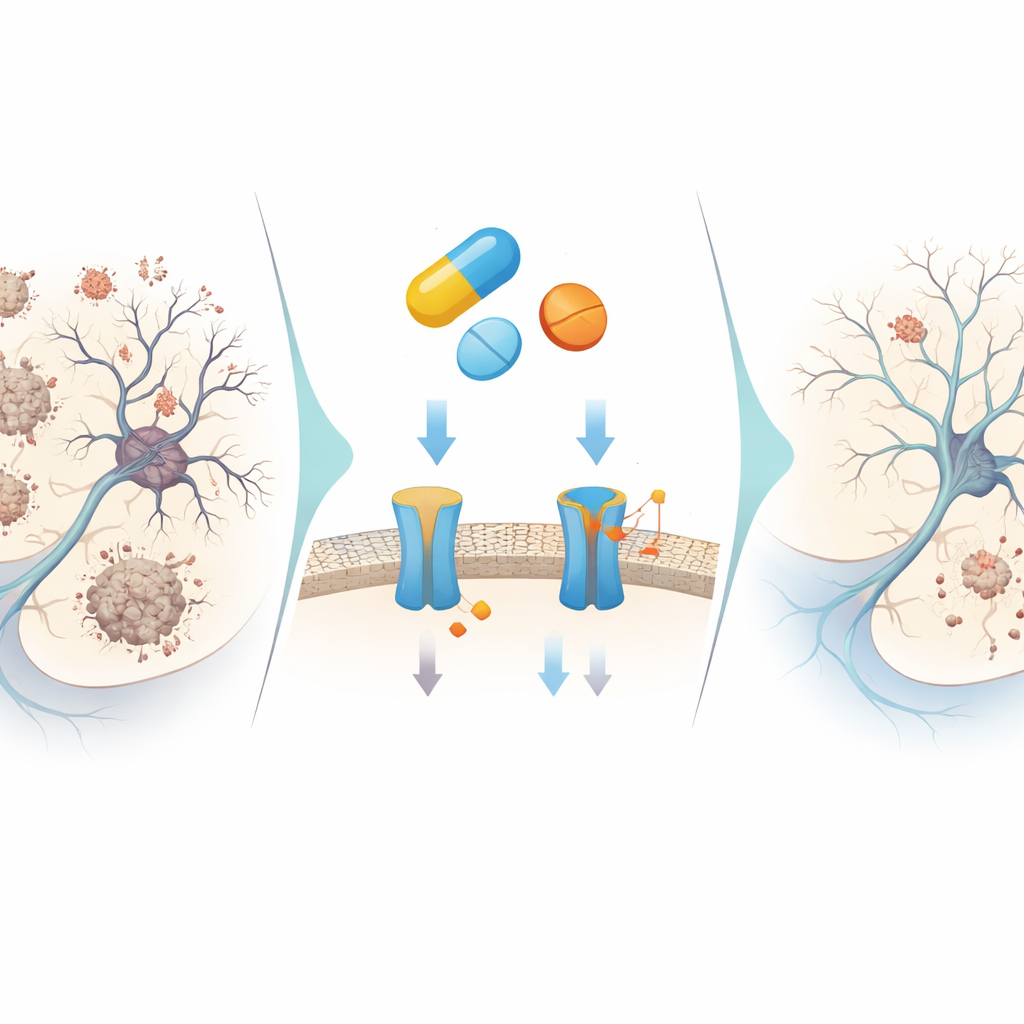
O que isso pode significar para tratamentos futuros
Em conjunto, os resultados sugerem que ZINC000019796155, um fármaco já aprovado, pode agir como uma pequena ferramenta molecular multitarefas: bloqueia parcialmente a produção de amyloid‑beta, retarda sua agregação, limita a degradação de um mensageiro chave da memória, neutraliza oxidantes nocivos e ajuda a afastar os neurônios de vias de autodestruição e da formação de emaranhados. Seus efeitos são moderados, e não extremos, o que pode ser mais seguro dados os fracassos anteriores de bloqueadores de BACE1 muito potentes. Embora o composto precise de ajustes químicos e testes cuidadosos em animais e, eventualmente, em humanos, este estudo ilustra como triagem computacional inteligente combinada com experimentos laboratoriais direcionados pode revelar novos papéis neuroprotetores para medicamentos conhecidos, abrindo uma rota mais eficiente rumo a futuras terapias para Alzheimer.
Citação: Phemphunananchai, K., Waiwut, P., Phetcharaburanin, J. et al. Repurposing FDA-approved drugs as multi-target neuroprotective agents for Alzheimer’s disease via computational screening and experimental validation. Sci Rep 16, 11688 (2026). https://doi.org/10.1038/s41598-026-46708-2
Palavras-chave: Doença de Alzheimer, reaproveitamento de medicamentos, inibição de BACE1, terapia multitarget, neuroproteção