Clear Sky Science · fr
Réaffectation de médicaments approuvés par la FDA en agents neuroprotecteurs multi‑cibles pour la maladie d’Alzheimer via criblage informatique et validation expérimentale
Pourquoi de vieux médicaments pourraient aider une mémoire qui s’efface
La maladie d’Alzheimer prive des millions de personnes de leurs souvenirs et de leur autonomie, et les traitements actuels ne soulagent les symptômes que pendant une période limitée. Mettre au point de nouveaux médicaments est long, coûteux et risqué. Cette étude pose une question simple mais puissante : peut‑on rechercher parmi des médicaments déjà approuvés et testés pour leur sécurité dans d’autres indications, et en trouver qui protègent discrètement le cerveau âgé sur plusieurs fronts à la fois ?
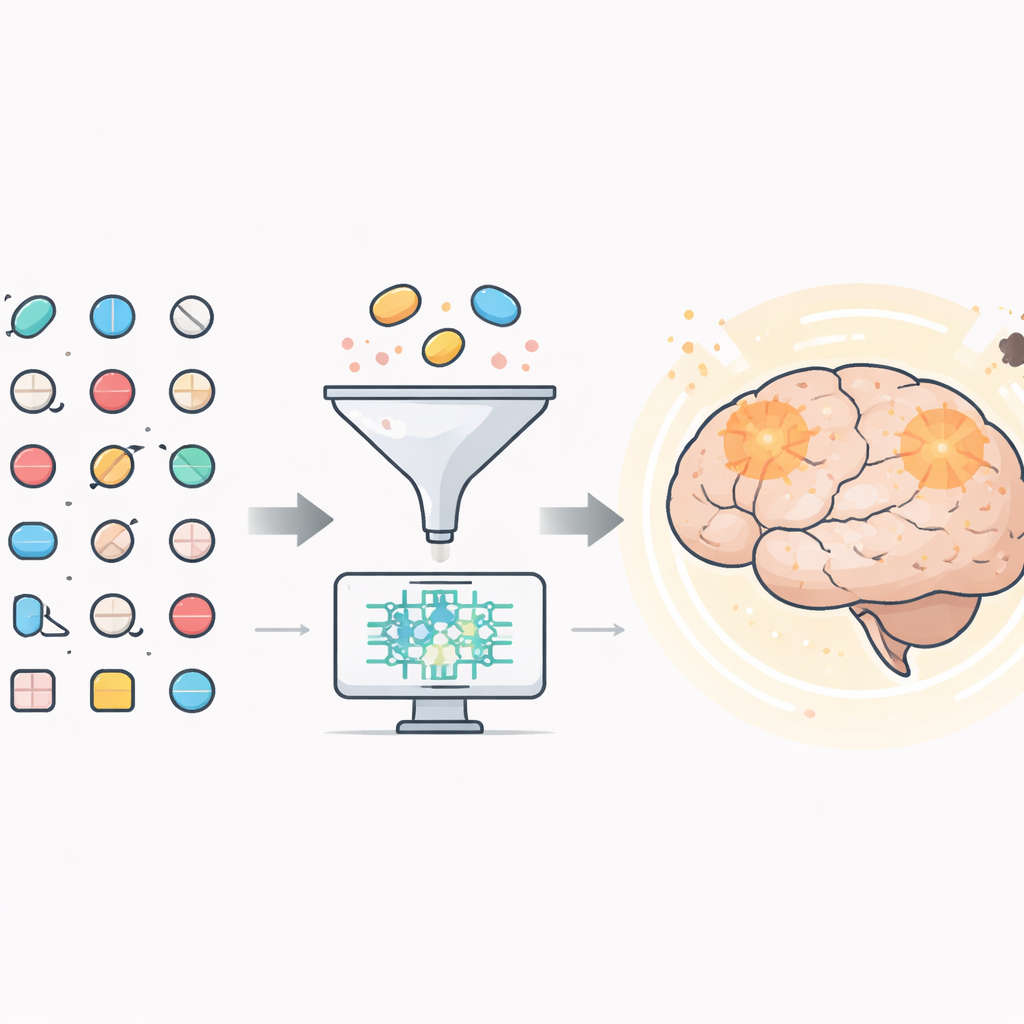
À la recherche d’aides cachées dans des médicaments existants
Les chercheurs ont commencé avec plus de 1 500 médicaments déjà approuvés par la Food and Drug Administration des États‑Unis. À l’aide d’outils informatiques, ils ont d’abord éliminé les composés peu susceptibles d’atteindre le cerveau, puisqu’un traitement contre Alzheimer doit franchir la barrière hémato‑encéphalique. Environ 600 candidats ont passé ce test. Ensuite, ils ont utilisé des modèles 3D détaillés d’une enzyme cérébrale clé, appelée BACE1, pour voir quels médicaments pouvaient se lier de manière stable et ajustée à son site actif. BACE1 est importante car elle aide à découper une protéine plus grande en amyloïde‑bêta, le fragment collant qui s’agglomère en plaques dans le cerveau des personnes atteintes d’Alzheimer.
Identifier un candidat médicament multitâche
À partir de ce criblage virtuel, 14 candidats prometteurs ont été identifiés, et quatre ont été retenus pour une étude plus approfondie en fonction de leur affinité pour l’enzyme, de leurs caractéristiques chimiques et de leur sécurité connue en usage prolongé. L’équipe a ensuite réalisé de longues simulations informatiques pour observer le comportement de chaque candidat lié à BACE1 au fil du temps. Les quatre sont restés stables dans la cavité de l’enzyme, mais un composé, référencé ZINC000019796155, s’est distingué par ses interactions favorables avec les régions les plus critiques de BACE1. Ces simulations suggèrent que le médicament pourrait réduire la capacité de l’enzyme à produire de l’amyloïde‑bêta sans déstabiliser la protéine elle‑même.
Tester comment le médicament protège la chimie cérébrale
Les prédictions informatiques ne sont qu’une première étape, aussi les scientifiques ont‑ils testé les quatre candidats en laboratoire. Tous ont ralenti l’activité de BACE1, et ZINC000019796155 a montré l’effet le plus marqué, bien que moins puissant que des inhibiteurs expérimentaux très efficaces. Fait important, en examinant d’autres processus liés à Alzheimer, ils ont constaté que ce même composé inhibait une autre enzyme, la butyrylcholinestérase, qui devient plus active au fur et à mesure de la progression de la maladie et dégrade un messager chimique lié à la mémoire. Il a également réduit l’agrégation de l’amyloïde‑bêta en tube à essai et montré une forte activité antioxydante, ce qui signifie qu’il peut neutraliser des radicaux libres délétères qui contribuent à la mort des cellules cérébrales.
Protéger les cellules nerveuses des dommages
Pour voir comment ces actions se traduisent à l’intérieur des cellules vivantes, l’équipe a exposé des cellules dérivées d’humains et similaires à des neurones au peroxyde d’hydrogène, un produit chimique qui imite le stress oxydatif observé dans les cerveaux atteints d’Alzheimer et qui tue normalement de nombreuses cellules. Lorsque les cellules ont été prétraitées avec ZINC000019796155, beaucoup ont survécu. Une analyse approfondie des protéines cellulaires a révélé que le composé atténuait les marqueurs de la mort cellulaire programmée et réduisait les niveaux d’acteurs clés dans la formation des plaques et des enchevêtrements, y compris le précurseur de l’amyloïde‑bêta, l’enzyme BACE1 elle‑même, et une forme modifiée de la protéine tau qui tend à former des fibres enroulées à l’intérieur des neurones. Parallèlement, il a renforcé les signaux dans des voies connues pour maintenir la tau dans un état plus sain et moins collant.
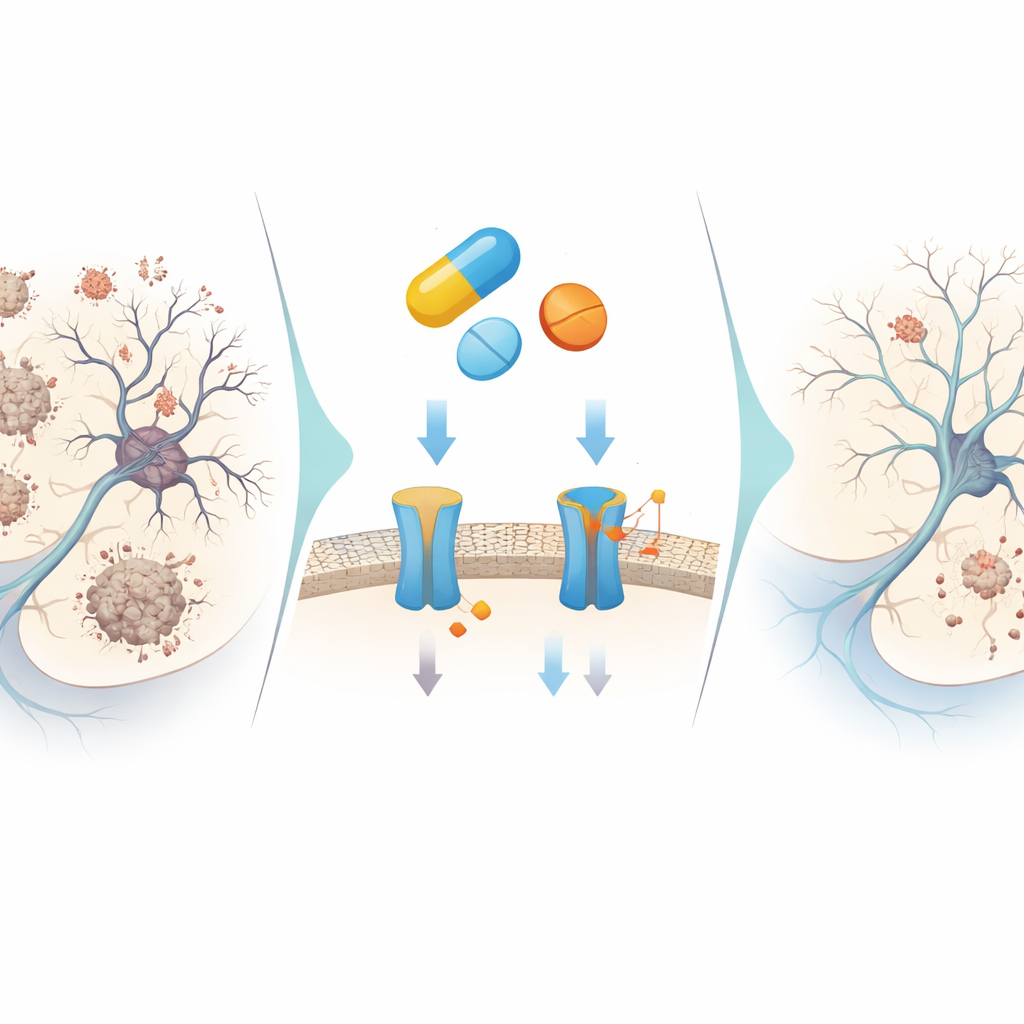
Ce que cela pourrait signifier pour les traitements futurs
Dans l’ensemble, les résultats suggèrent que ZINC000019796155, un médicament déjà approuvé, peut agir comme un petit outil moléculaire multifonction : il bloque partiellement la production d’amyloïde‑bêta, ralentit son agrégation, limite la dégradation d’un messager clé de la mémoire, éteint les oxydants nocifs et aide à détourner les cellules nerveuses des voies d’autodestruction et de formation d’enchevêtrements. Ses effets sont modérés plutôt qu’extrêmes, ce qui peut être plus sûr au vu des échecs passés d’inhibiteurs de BACE1 trop puissants. Bien que le composé nécessite un affinage chimique et des tests rigoureux chez l’animal puis chez l’homme, cette étude illustre comment un criblage informatique intelligent associé à des expériences de laboratoire ciblées peut révéler de nouveaux rôles protecteurs pour le cerveau des médicaments familiers, ouvrant une voie plus efficace vers de futures thérapies contre Alzheimer.
Citation: Phemphunananchai, K., Waiwut, P., Phetcharaburanin, J. et al. Repurposing FDA-approved drugs as multi-target neuroprotective agents for Alzheimer’s disease via computational screening and experimental validation. Sci Rep 16, 11688 (2026). https://doi.org/10.1038/s41598-026-46708-2
Mots-clés: maladie d’Alzheimer, réorientation de médicaments, inhibition de BACE1, thérapie multi‑cible, neuroprotection