Clear Sky Science · it
Riproposizione di farmaci approvati dalla FDA come agenti neuroprotettivi multi‑bersaglio per la malattia di Alzheimer tramite screening computazionale e convalida sperimentale
Perché i vecchi medicinali potrebbero aiutare una memoria che svanisce
La malattia di Alzheimer sottrae a milioni di persone i ricordi e l’autonomia, e i farmaci attuali possono soltanto alleviare i sintomi per un periodo limitato. Sviluppare nuovi farmaci è lento, costoso e rischioso. Questo studio pone una domanda semplice ma potente: è possibile cercare tra medicinali già approvati e testati per la sicurezza in altre condizioni e trovare quelli che proteggono silenziosamente il cervello invecchiato su più fronti contemporaneamente?
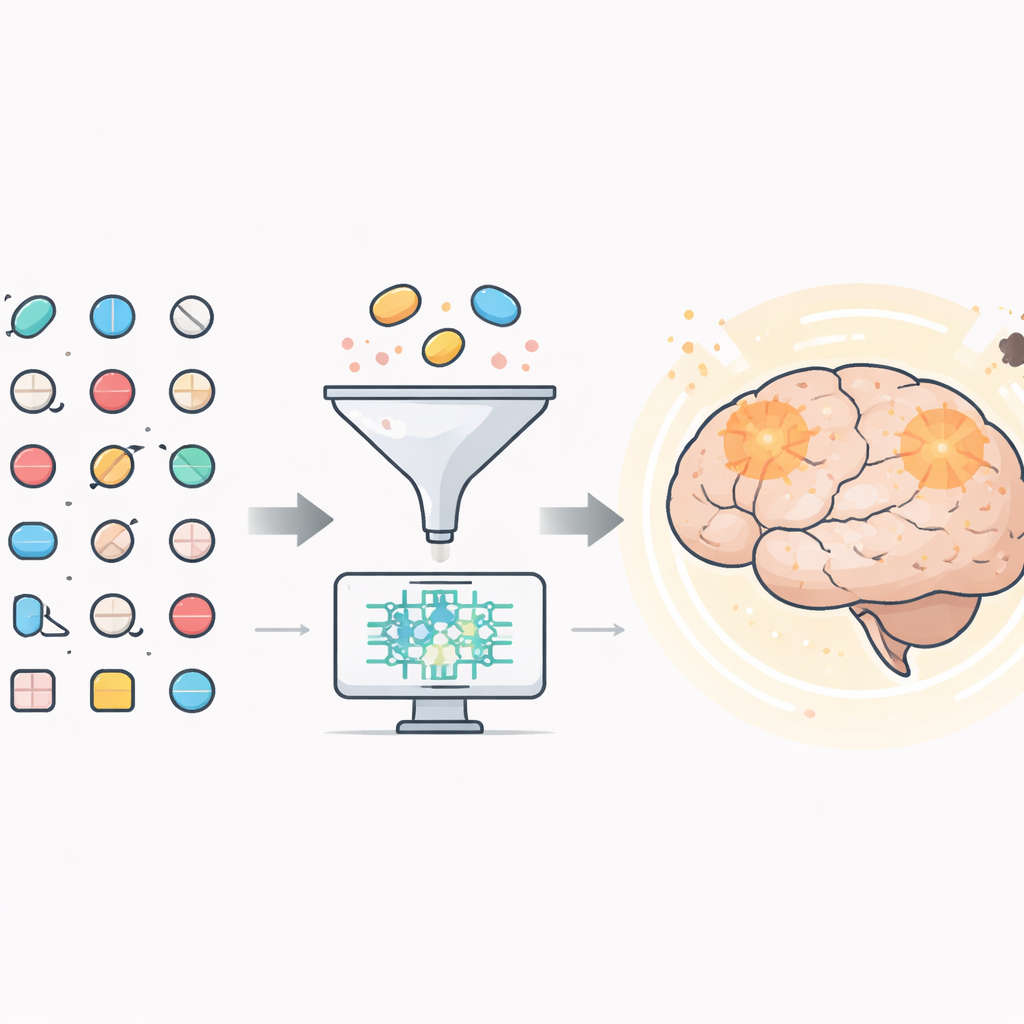
Cercare aiutanti nascosti nei farmaci esistenti
I ricercatori hanno iniziato con oltre 1.500 farmaci già approvati dalla Food and Drug Administration statunitense. Con strumenti informatici hanno innanzitutto scartato i composti improbabili di raggiungere il cervello, poiché un trattamento per l’Alzheimer deve attraversare la barriera emato‑encefalica. Circa 600 candidati hanno superato questo test. Successivamente hanno usato modelli 3D dettagliati di un enzima cerebrale chiave, chiamato BACE1, per vedere quali farmaci potevano legarsi al suo sito attivo in modo stabile e aderente. BACE1 è importante perché contribuisce a tagliare una proteina più grande in amiloide‑beta, il frammento appiccicoso che forma placche nel cervello delle persone con Alzheimer.
Trovare un candidato farmacologico multitasking
Dallo screening virtuale sono emersi 14 risultati promettenti, e quattro sono stati selezionati per uno studio più approfondito in base alla loro affinità per l’enzima, alle caratteristiche chimiche e alla sicurezza nota in uso prolungato. Il gruppo ha poi eseguito lunghe simulazioni al computer per osservare come si comportava ciascun candidato legato a BACE1 nel tempo. Tutti e quattro sono rimasti stabili nella tasca dell’enzima, ma un composto, etichettato ZINC000019796155, si è distinto per le interazioni favorevoli con le regioni più critiche di BACE1. Queste simulazioni suggerivano che il farmaco potrebbe ridurre la capacità dell’enzima di produrre amiloide‑beta senza destabilizzare la proteina stessa.
Testare come il farmaco protegge la chimica cerebrale
Le previsioni al calcolatore sono solo un primo passo, quindi gli scienziati hanno testato i quattro candidati in esperimenti di laboratorio. Tutti hanno rallentato l’attività di BACE1, e ZINC000019796155 ha mostrato l’effetto più marcato, sebbene ancora più debole rispetto a potenti inibitori sperimentali. Importante, all’esame di altri processi legati all’Alzheimer, questo stesso composto ha inibito anche un altro enzima, la butirilcolinesterasi, che diventa più attivo con la progressione della malattia e degrada un mediatore chimico legato alla memoria. Ha inoltre ridotto l’aggregazione dell’amiloide‑beta in provetta e mostrato forte attività antiossidante, ossia la capacità di neutralizzare radicali liberi dannosi che contribuiscono alla morte delle cellule cerebrali.
Proteggere i neuroni dai danni
Per vedere come queste azioni si traducono nelle cellule viventi, il team ha esposto cellule neuronali di origine umana a perossido di idrogeno, una sostanza che imita lo stress ossidativo osservato nei cervelli con Alzheimer e che normalmente uccide molte cellule. Quando le cellule sono state pretrattate con ZINC000019796155, molte di più sono sopravvissute. Un’analisi più approfondita delle proteine cellulari ha rivelato che il composto attenuava i segni della morte cellulare programmata e riduceva i livelli di elementi chiave nella formazione di placche e grovigli, inclusi il precursore dell’amiloide‑beta, l’enzima BACE1 stesso e una forma modificata della proteina tau che tende a formare fibre contorte all’interno dei neuroni. Allo stesso tempo, potenziava i segnali lungo vie note per mantenere la tau in uno stato più sano e meno aggregante.
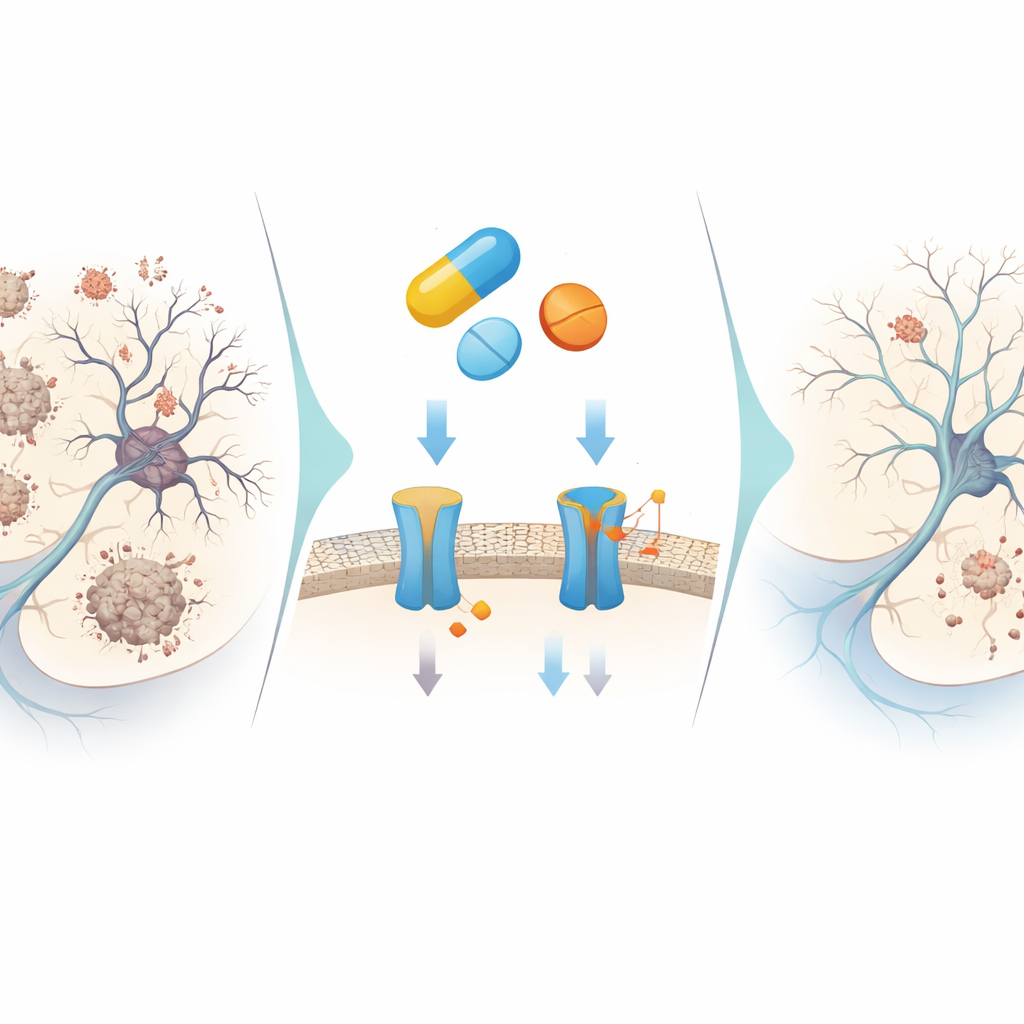
Cosa potrebbe significare per i futuri trattamenti
Nel loro insieme, i risultati suggeriscono che ZINC000019796155, un farmaco già approvato, può comportarsi come un piccolo attrezzo molecolare: blocca parzialmente la produzione di amiloide‑beta, rallenta la sua aggregazione, limita la degradazione di un mediatore chiave della memoria, spegne ossidanti dannosi e contribuisce a deviare i neuroni dalle vie di autodistruzione e dalla formazione di grovigli. I suoi effetti sono moderati piuttosto che estremi, il che potrebbe essere più sicuro alla luce dei fallimenti passati di inibitori di BACE1 troppo potenti. Sebbene il composto necessiti di ottimizzazioni chimiche e di accurati test in modelli animali e infine nell’uomo, questo studio illustra come uno screening computazionale intelligente combinato con esperimenti di laboratorio mirati possa svelare nuovi ruoli neuroprotettivi per medicinali familiari, aprendo una via più efficiente verso future terapie per l’Alzheimer.
Citazione: Phemphunananchai, K., Waiwut, P., Phetcharaburanin, J. et al. Repurposing FDA-approved drugs as multi-target neuroprotective agents for Alzheimer’s disease via computational screening and experimental validation. Sci Rep 16, 11688 (2026). https://doi.org/10.1038/s41598-026-46708-2
Parole chiave: malattia di Alzheimer, riproposizione di farmaci, inibizione di BACE1, terapia multi‑bersaglio, neuroprotezione