Clear Sky Science · es
Reutilización de fármacos aprobados por la FDA como agentes neuroprotectores multitarget para la enfermedad de Alzheimer mediante cribado computacional y validación experimental
Por qué los medicamentos antiguos podrían ayudar a una memoria que se desvanece
La enfermedad de Alzheimer le arrebata a millones de personas sus recuerdos y su independencia, y los fármacos actuales solamente alivian los síntomas durante un tiempo limitado. Desarrollar medicamentos completamente nuevos es lento, costoso y arriesgado. Este estudio plantea una pregunta simple pero potente: ¿podemos buscar entre medicamentos ya aprobados y comprobados en seguridad para otras condiciones y encontrar aquellos que protejan discretamente el cerebro envejecido en varios frentes a la vez?
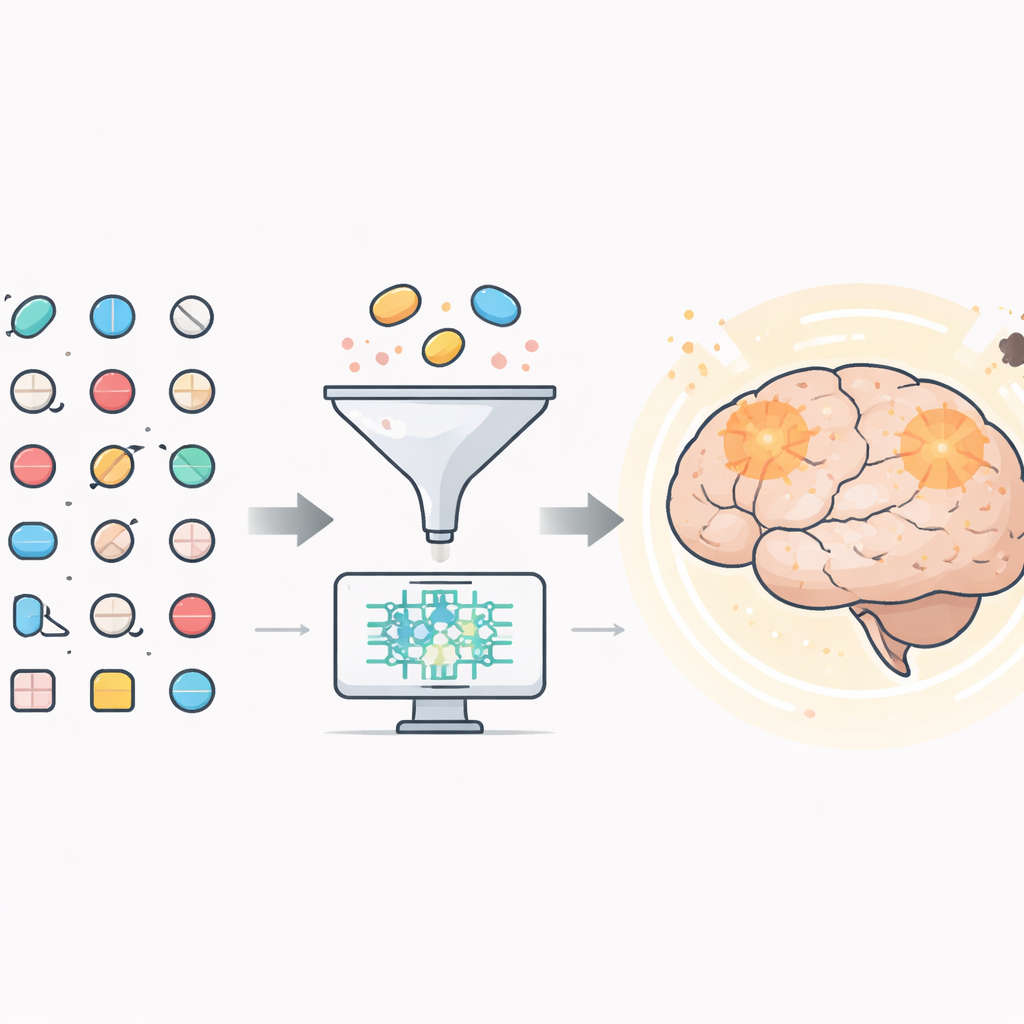
Buscando ayudantes ocultos en fármacos existentes
Los investigadores partieron de más de 1.500 fármacos ya aprobados por la Food and Drug Administration de Estados Unidos. Usando herramientas informáticas, primero descartaron los compuestos poco probables de alcanzar el cerebro, ya que un tratamiento para el Alzheimer debe atravesar la barrera hematoencefálica. Unos 600 candidatos superaron esta prueba. A continuación, emplearon modelos 3D detallados de una enzima cerebral clave, llamada BACE1, para ver qué fármacos podían unirse a su sitio activo de manera estable y ajustada. BACE1 es importante porque ayuda a cortar una proteína mayor en amiloide-beta, el fragmento pegajoso que forma acúmulos en los cerebros de personas con Alzheimer.
Encontrando un candidato farmacológico multitarea
De este cribado virtual se identificaron 14 hallazgos prometedores, y se seleccionaron cuatro para un estudio más detenido en función de su encaje con la enzima, sus características químicas y su seguridad conocida en uso prolongado. El equipo realizó luego largas simulaciones por ordenador para observar cómo se comportaba cada candidato mientras estaba unido a BACE1 a lo largo del tiempo. Los cuatro permanecieron estables en el bolsillo de la enzima, pero un compuesto, etiquetado ZINC000019796155, destacó por sus interacciones favorables con las regiones más críticas de BACE1. Estas simulaciones sugirieron que el fármaco podría reducir la capacidad de la enzima para producir amiloide-beta sin desestabilizar la proteína en sí.
Probando cómo el fármaco protege la química cerebral
Las predicciones informáticas son solo un primer paso, por lo que los científicos probaron los cuatro candidatos en experimentos de laboratorio. Todos ralentizaron la actividad de BACE1, y ZINC000019796155 mostró el efecto más fuerte, aunque todavía más débil que inhibidores experimentales de alta potencia. De forma importante, al examinar otros procesos relacionados con el Alzheimer, encontraron que este mismo compuesto inhibía otra enzima, la butirilcolinesterasa, que se vuelve más activa a medida que progresa la enfermedad y descompone un mensajero químico ligado a la memoria. También redujo la agregación de amiloide-beta en un tubo de ensayo y mostró una fuerte actividad antioxidante, lo que significa que podría neutralizar radicales libres dañinos que contribuyen a la muerte de las neuronas.
Protegiendo las células nerviosas del daño
Para ver cómo se traducen estas acciones dentro de células vivas, el equipo expuso células de tipo neuronal derivadas de humanos a peróxido de hidrógeno, un químico que imita el estrés oxidativo observado en cerebros con Alzheimer y que normalmente mata muchas células. Cuando las células fueron pretratadas con ZINC000019796155, muchas más sobrevivieron. Un análisis adicional de proteínas celulares reveló que el compuesto atenuó marcadores de muerte celular programada y redujo los niveles de actores clave en la formación de placas y ovillos, incluido el precursor de amiloide-beta, la propia enzima BACE1 y una forma modificada de la proteína tau que tiende a formar fibras retorcidas dentro de las neuronas. Al mismo tiempo, potenció señales en vías conocidas por mantener la tau en un estado más saludable y menos propenso a agregarse.
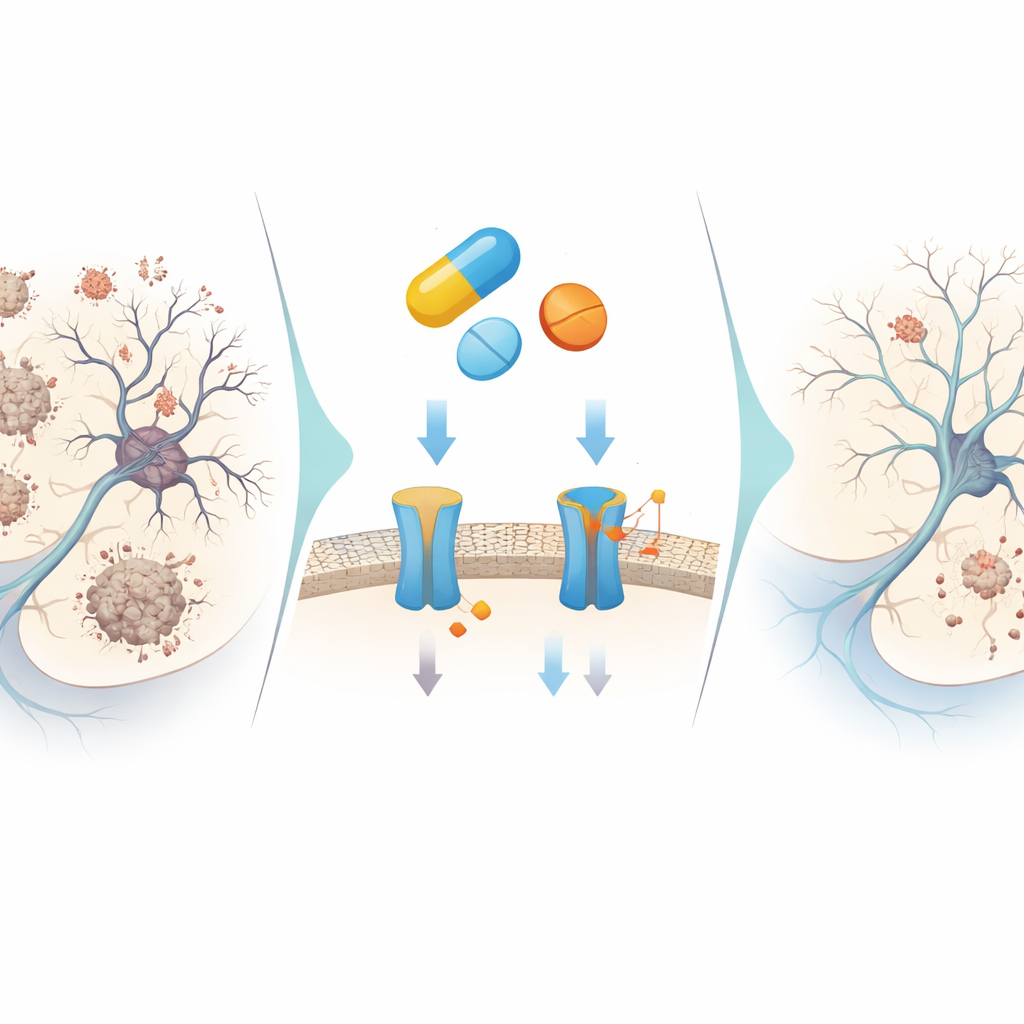
Lo que esto podría significar para tratamientos futuros
En conjunto, los resultados sugieren que ZINC000019796155, un fármaco ya aprobado, puede actuar como una pequeña herramienta molecular multifunción: bloquea parcialmente la producción de amiloide-beta, ralentiza su agregación, limita la degradación de un mensajero clave de la memoria, apaga oxidantes nocivos y ayuda a desviar a las células nerviosas de las vías de autodestrucción y de la formación de ovillos. Sus efectos son moderados más que extremos, lo que podría ser más seguro dado el historial de fracasos con bloqueadores de BACE1 excesivamente potentes. Aunque el compuesto requerirá optimización química y pruebas cuidadosas en animales y, eventualmente, en personas, este estudio ilustra cómo el cribado informático inteligente combinado con experimentos de laboratorio dirigidos puede descubrir nuevos roles neuroprotectores para fármacos familiares, abriendo una ruta más eficiente hacia futuras terapias contra el Alzheimer.
Cita: Phemphunananchai, K., Waiwut, P., Phetcharaburanin, J. et al. Repurposing FDA-approved drugs as multi-target neuroprotective agents for Alzheimer’s disease via computational screening and experimental validation. Sci Rep 16, 11688 (2026). https://doi.org/10.1038/s41598-026-46708-2
Palabras clave: Enfermedad de Alzheimer, reutilización de fármacos, inhibición de BACE1, terapia multitarget, neuroprotección