Clear Sky Science · sv
XMD8-92 och JWG-045 uppvisar anti‑feroptotiska aktiviteter, oberoende av hämning av ERK5
Varför det ger viktig insikt att skydda döende cancerceller
Cancerforskare undersöker en överraskande form av celldöd som kallas ferroptos, där järn och oxiderade fetter samverkar för att skapa hål i cellmembran. Eftersom många svårbehandlade tumörer är ovanligt känsliga för denna process testas läkemedel som utlöser ferroptos som ett nytt sätt att döda cancerceller. I denna studie ville man ta reda på om blockering av ett cancerfrämjande protein, ERK5, påverkar hur bröstcancerceller svarar på ferroptos. I arbetet upptäckte forskarna en oväntad vändning: två vitt använda kemikalier som blockerar ERK5 skyddar faktiskt cancerceller från ferroptotisk död via en helt annan mekanism.
Hur ett stress‑signalprotein möter en ovanlig dödsväg
ERK5 ingår i ett signalsystem som hjälper celler att reagera på tillväxtsignaler och stressiga förhållanden. Tumörer med hög ERK5‑aktivitet växer ofta snabbare, sprider sig lättare och är mer motståndskraftiga mot andra riktade läkemedel. En separat forskningslinje har visat att ett skyddande enzym kallat GPX4, som normalt rensar bort skadliga peroxider från cellmembran, är avgörande för att förhindra ferroptos. När GPX4 blockeras av kemikalier som RSL3 blir fetterna i cellmembranet oxiderade, membranet bryts gradvis ner och cellen dör på ett karakteristiskt, järnberoende sätt. Eftersom ERK5 kan interagera fysiskt med GPX4 undrade författarna om detta stress‑signalprotein skulle göra cancerceller mer eller mindre känsliga för ferroptos.
Läkemedel som hjälper och läkemedel som inte gör någonting
Gruppen började med att gräva i stora databaser över cancerceller och fann att tumörer med höga ERK5‑nivåer tenderade att vara mer känsliga för GPX4‑blockerande läkemedel, särskilt när cellerna antagit ett mer rörligt, aggressivt så kallat mesenkymalt tillstånd. De gick sedan vidare till laborationsexperiment med flera bröst‑ och livmoderhalscancer‑cellinjer. När de behandlade celler med RSL3 för att utlösa ferroptos höll två ERK5‑inriktade föreningar, XMD8‑92 och JWG‑045, oväntat många celler vid liv. Andra hämmare riktade mot samma signalsystem — nyare ERK5‑blockerare JWG‑071 och BAY‑885, samt ett läkemedel som verkar ett steg uppströms vid MEK5 — gav inget sådant skydd. I samtliga fall uppförde sig den standardmässiga ferroptos‑blockeraren Ferrostatin‑1 som väntat, vilket bekräftade att RSL3 verkligen dödade celler via ferroptos.
När blockering av ett mål inte egentligen är förklaringen
För att pröva om den skyddande effekten verkligen involverade ERK5 minskade forskarna eller tog bort ERK5 helt i flera cancercellinjer med genetiska verktyg, inklusive short hairpin‑RNA och CRISPR‑genredigering. Om ERK5 varit avgörande för den anti‑feroptotiska effekten av dessa läkemedel borde radering av ERK5 ha upphävt skyddet. Istället fortsatte XMD8‑92 och JWG‑045 att rädda celler från RSL3‑inducerad död även när ERK5 knappt gick att detektera eller var helt frånvarande. Däremot hade JWG‑071 och BAY‑885 fortsatt ingen effekt. Teamet uteslöt också en känd off‑target, det kromatinassocierade proteinet BRD4, eftersom separata BRD4‑hämmare inte efterliknade det ferroptos‑blockerande beteendet. Tillsammans pekade resultaten på en tidigare oigenkänd off‑target‑aktivitet som är unik för XMD8‑92 och JWG‑045.
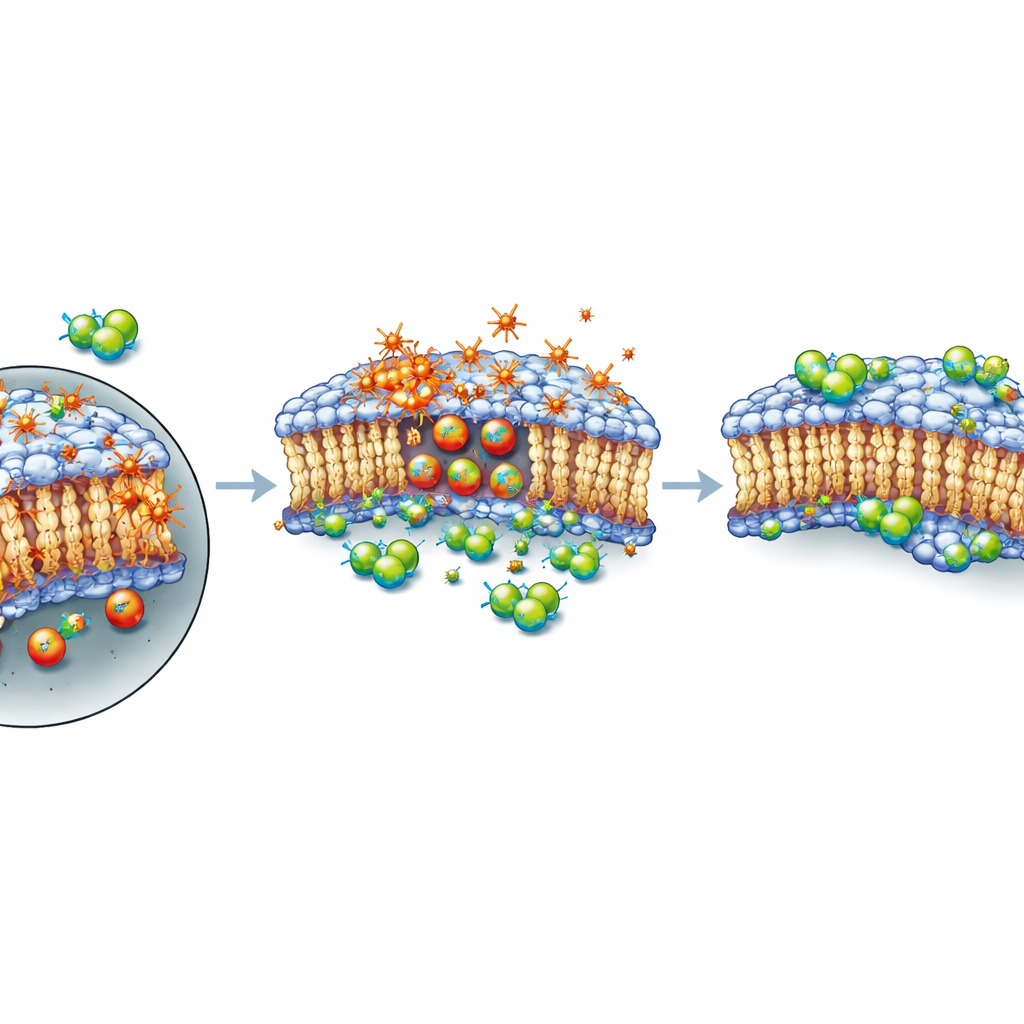
Ett skydd för cellens yttre hud, inte en broms på skadan
Nästa fråga var hur dessa föreningar ingrep i dödsprocessen. Genom att följa genaktivitet under flera timmar efter XMD8‑92‑behandling såg de endast måttliga förändringar i kända ferroptos‑relaterade gener och ingen tydlig, samordnad förändring i den övergripande ferroptos‑signaleringen. Med en fluorescerande färg som lyser upp oxiderade fetter visade de att XMD8‑92 inte hindrade lipidperoxidation; om något ökade oxidation när cellerna fick både RSL3 och XMD8‑92. Ändå överlevde cellerna bättre. I noggrant tidsinställda experiment var en kort exponering för RSL3 ensam tillräcklig för att fälla cellernas öde, även efter att läkemedlet spolats bort. Men om XMD8‑92 tillsattes efter den korta pulsen återhämtade sig många celler. Detta mönster tyder på att föreningen inte förhindrar den initiala kemiska skadan; istället verkar den hjälpa till att bibehålla eller reparera plasmamembranet, åtminstone temporärt, så att celler kan stå emot en period av intensiv oxidativ stress innan de så småningom går under om skadan fortsätter att ackumuleras.
Vad detta betyder för cancerforskning och läkemedelsdesign
För icke‑specialister är huvudbudskapet att inte alla läkemedel beter sig som deras etiketter antyder. Två molekyler som ofta används för att studera och hämma ERK5 visar sig ha en extra, kraftfull effekt: de kan fördröja en form av järn‑driven, membranrupturerande celldöd utan att egentligen stoppa den bakomliggande kemiska skadan. Detta off‑target‑skydd är viktigt av två skäl. För det första varnar det forskare för att resultat erhållna med XMD8‑92 och JWG‑045 kanske inte på ett tillförlitligt sätt speglar vad som händer när endast ERK5 blockeras. För det andra antyder det förekomsten av läkemedelsåtkomliga mekanismer som stärker membranreparation under extrem stress, något som en dag skulle kunna utnyttjas för att skydda friska vävnader i sjukdomar där ferroptos går ur kontroll. För nu understryker arbetet behovet av att kombinera nyare, mer selektiva hämmare med genetiska verktyg när man utforskar ERK5‑biologi, och att behandla korrelationer mellan gen‑nivåer och läkemedelsresponser med försiktighet snarare än att anta direkt orsakssamband.
Citering: Zhang, W., Kan, K., Pidd, A.B. et al. XMD8-92 and JWG-045 exhibit anti-ferroptotic activities, independently of inhibiting ERK5. Sci Rep 16, 11337 (2026). https://doi.org/10.1038/s41598-026-42079-w
Nyckelord: ferroptos, ERK5‑hämmare, bröstcancer, celldöds‑vägar, läkemedels off‑target‑effekter