Clear Sky Science · fr
XMD8-92 et JWG-045 présentent des activités anti‑ferroptotiques, indépendamment de l’inhibition d’ERK5
Pourquoi protéger des cellules cancéreuses en train de mourir peut encore beaucoup nous apprendre
Les chercheurs en cancérologie explorent une forme surprenante de mort cellulaire appelée ferroptose, dans laquelle le fer et les lipides oxydés s’allient pour percer les membranes cellulaires. Comme de nombreuses tumeurs difficiles à traiter sont particulièrement vulnérables à ce processus, des médicaments déclenchant la ferroptose sont testés comme nouvelle stratégie pour éliminer les cellules cancéreuses. Cette étude visait à examiner si le blocage d’une protéine promotrice de cancer, ERK5, influence la réponse des cellules du sein à la ferroptose. Ce faisant, les auteurs ont découvert une tournure inattendue : deux composés largement utilisés pour inhiber ERK5 protègent en réalité les cellules cancéreuses de la mort ferroptotique par une voie complètement différente.
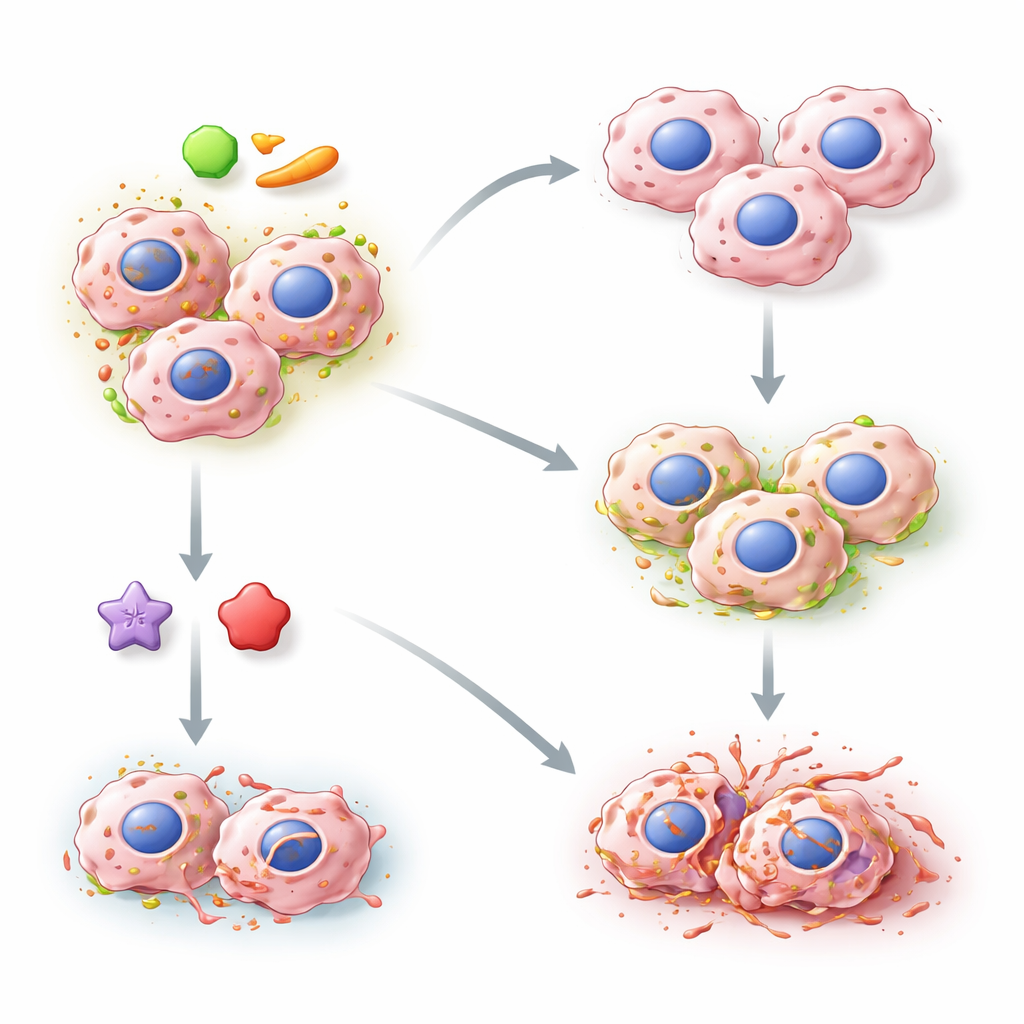
Comment une protéine de signalisation du stress rencontre une voie de mort inhabituelle
ERK5 fait partie d’un réseau de signalisation qui aide les cellules à répondre aux signaux de croissance et aux conditions de stress. Les tumeurs présentant une activité élevée d’ERK5 ont souvent une croissance plus rapide, une dissémination accrue et une résistance à d’autres thérapies ciblées. Des travaux parallèles ont montré qu’une enzyme protectrice, GPX4, qui élimine normalement les peroxydes nocifs des membranes cellulaires, est essentielle pour prévenir la ferroptose. Lorsqu’on bloque GPX4 avec des composés comme RSL3, les lipides membranaires s’oxydent, la membrane se dégrade progressivement et la cellule meurt d’une manière distincte dépendante du fer. Parce qu’ERK5 peut interagir physiquement avec GPX4, les auteurs se sont demandé si cette protéine de signalisation du stress pouvait rendre les cellules cancéreuses plus ou moins sensibles à la ferroptose.
Des médicaments qui aident et des médicaments sans effet
L’équipe a d’abord exploré de larges bases de données de lignées cancéreuses et constaté que les tumeurs exprimant beaucoup d’ERK5 avaient tendance à être plus sensibles aux inhibiteurs de GPX4, en particulier lorsque les cellules avaient adopté un état mésenchymateux plus mobile et agressif. Ils sont ensuite passés à des expériences en laboratoire sur plusieurs lignées de cancer du sein et du col de l’utérus. Lorsqu’ils ont traité les cellules par RSL3 pour déclencher la ferroptose, deux composés ciblant ERK5, XMD8‑92 et JWG‑045, ont de façon inattendue permis à de nombreuses cellules de survivre. D’autres inhibiteurs visant la même voie de signalisation — des bloqueurs d’ERK5 plus récents comme JWG‑071 et BAY‑885, ainsi qu’un médicament agissant une étape en amont sur MEK5 — n’ont offert aucune protection. Dans tous les cas, la molécule standard bloquant la ferroptose, Ferrostatin‑1, s’est comportée comme prévu, confirmant que RSL3 tuait bien les cellules par ferroptose.
Lorsque bloquer une cible n’est pas vraiment la raison
Pour vérifier si cet effet protecteur impliquait réellement ERK5, les chercheurs ont réduit ou supprimé complètement ERK5 dans plusieurs lignées de cellules cancéreuses à l’aide d’outils génétiques, y compris des ARN courts en épingle et l’édition génique CRISPR. Si ERK5 était essentiel pour l’action anti‑ferroptotique de ces composés, la suppression d’ERK5 devrait abolir la protection. Au lieu de cela, XMD8‑92 et JWG‑045 ont continué à sauver les cellules de la mort induite par RSL3, même lorsque ERK5 était à peine détectable ou entièrement absent. En revanche, JWG‑071 et BAY‑885 restaient inefficaces. L’équipe a également écarté un off‑target connu, la protéine associée à la chromatine BRD4, car des inhibiteurs spécifiques de BRD4 n’ont pas reproduit le comportement bloquant la ferroptose. Ensemble, ces résultats indiquent une activité hors‑cible jusque‑là inconnue, propre à XMD8‑92 et JWG‑045.
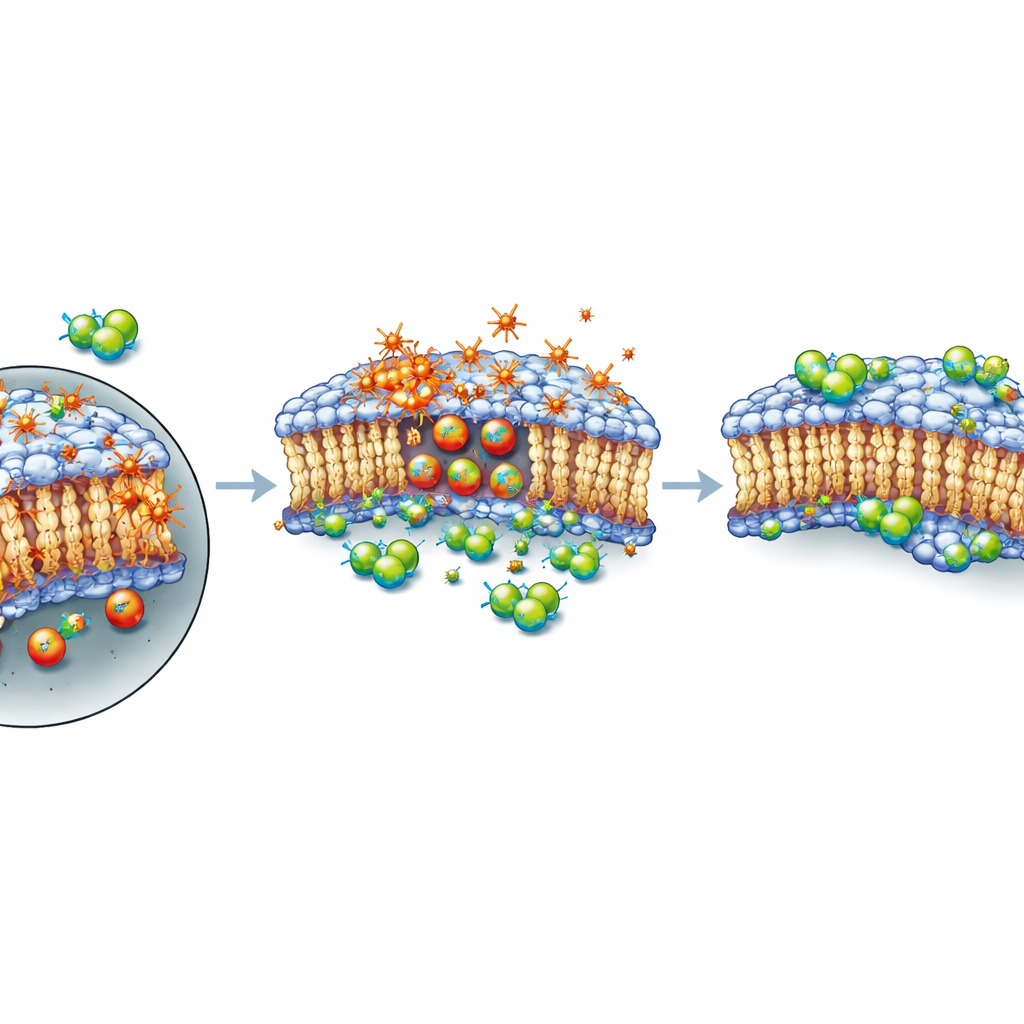
Un bouclier pour la « peau » de la cellule, pas un frein au dommage
Les auteurs se sont ensuite demandé comment ces composés intervenaient dans le processus de mort. En suivant l’activité génique pendant plusieurs heures après le traitement par XMD8‑92, ils n’ont observé que des variations modestes dans des gènes connus liés à la ferroptose et aucun changement clair et coordonné dans la signalisation globale de la ferroptose. En utilisant un colorant fluorescent qui s’allume en présence de lipides oxydés, ils ont montré que XMD8‑92 n’arrêtait pas la peroxydation lipidique ; si quelque chose, l’oxydation augmentait lorsque les cellules recevaient à la fois RSL3 et XMD8‑92. Pourtant, les cellules survivaient mieux. Dans des expériences soigneusement synchronisées, une exposition brève à RSL3 seule suffisait à sceller le destin des cellules, même après lavage du composé. Mais si XMD8‑92 était ajouté après cette courte impulsion, de nombreuses cellules récupéraient. Ce schéma suggère que le composé n’empêche pas le dommage chimique initial ; il semble plutôt aider à maintenir ou réparer la membrane plasmique, du moins temporairement, permettant aux cellules de supporter une période de stress oxydatif intense avant de succomber éventuellement si les dommages continuent de s’accumuler.
Ce que cela signifie pour la recherche sur le cancer et la conception de médicaments
Pour un public non spécialiste, le message central est que tous les médicaments ne se comportent pas comme l’indiquent leurs étiquettes. Deux molécules largement utilisées pour étudier et inhiber ERK5 possèdent en réalité un effet supplémentaire et puissant : elles peuvent retarder une forme de mort cellulaire dépendante du fer et provoquant la rupture membranaire sans arrêter le dommage chimique sous‑jacent. Cette protection hors‑cible est importante pour deux raisons. D’abord, elle alerte les chercheurs que les résultats obtenus avec XMD8‑92 et JWG‑045 peuvent ne pas refléter fidèlement ce qui se produit lorsque seul ERK5 est bloqué. Ensuite, elle suggère l’existence de mécanismes accessibles aux médicaments qui renforcent la réparation membranaire lors d’un stress extrême, qui pourraient un jour être exploités pour protéger les tissus sains dans des maladies où la ferroptose est incontrôlée. Pour l’instant, ce travail souligne la nécessité d’associer des inhibiteurs plus récents et plus sélectifs à des outils génétiques lors de l’exploration de la biologie d’ERK5, et d’aborder les corrélations entre niveaux d’expression génique et réponses médicamenteuses avec prudence plutôt que d’en déduire systématiquement une relation de cause à effet.
Citation: Zhang, W., Kan, K., Pidd, A.B. et al. XMD8-92 and JWG-045 exhibit anti-ferroptotic activities, independently of inhibiting ERK5. Sci Rep 16, 11337 (2026). https://doi.org/10.1038/s41598-026-42079-w
Mots-clés: ferroptose, inhibiteurs d’ERK5, cancer du sein, voies de mort cellulaire, effets hors‑cible des médicaments