Clear Sky Science · es
XMD8-92 y JWG-045 muestran actividades antiferroptóticas, independientemente de inhibir ERK5
Por qué proteger células cancerosas moribundas aún puede enseñarnos mucho
Los investigadores del cáncer están explorando una sorprendente forma de muerte celular llamada ferroptosis, en la que el hierro y los lípidos dañados se combinan para perforar las membranas celulares. Dado que muchos tumores difíciles de tratar son particularmente vulnerables a este proceso, se están probando fármacos que inducen ferroptosis como una nueva forma de matar células cancerosas. Este estudio se propuso examinar si bloquear una proteína promotora del cáncer, ERK5, influye en la respuesta de las células de cáncer de mama a la ferroptosis. Al hacerlo, los autores descubrieron una vuelta inesperada: dos compuestos ampliamente utilizados para bloquear ERK5 en realidad protegen a las células cancerosas de la muerte ferroptótica a través de una vía completamente diferente.
Cómo una proteína de señalización del estrés se cruza con una vía de muerte inusual
ERK5 forma parte de una red de señalización que ayuda a las células a responder a señales de crecimiento y a condiciones de estrés. Los tumores con alta actividad de ERK5 suelen crecer más rápido, diseminarse con mayor facilidad y resistir otros fármacos dirigidos. Otra línea de investigación ha mostrado que una enzima protectora llamada GPX4, que normalmente elimina peróxidos perjudiciales de las membranas celulares, es esencial para prevenir la ferroptosis. Cuando GPX4 es bloqueada por compuestos como RSL3, los lípidos de la membrana celular se oxidan, la membrana se degrada gradualmente y la célula muere de una forma distintiva dependiente del hierro. Dado que ERK5 puede interactuar físicamente con GPX4, los autores se preguntaron si esta proteína de señalización del estrés podría hacer que las células cancerosas fueran más o menos sensibles a la ferroptosis.
Fármacos que ayudan y fármacos que no hacen nada
El equipo primero examinó grandes bases de datos de líneas celulares cancerosas y encontró que los tumores con niveles altos de ERK5 tendían a ser más sensibles a los fármacos que bloquean GPX4, especialmente cuando las células habían adoptado un estado más móvil y agresivo, denominado mesenquimal. Luego pasaron a experimentos de laboratorio con varias líneas celulares de cáncer de mama y de cuello uterino. Cuando trataron las células con RSL3 para inducir ferroptosis, dos compuestos dirigidos a ERK5, XMD8-92 y JWG-045, mantuvieron inesperadamente con vida a muchas células. Otros inhibidores dirigidos a la misma vía de señalización—bloqueadores más recientes de ERK5 como JWG-071 y BAY-885, y un fármaco que actúa un paso aguas arriba en MEK5—no ofrecieron esta protección. En todos los casos, la molécula estándar que bloquea la ferroptosis, Ferrostatin-1, se comportó como se esperaba, confirmando que RSL3 estaba matando células mediante ferroptosis.
Cuando bloquear un objetivo no es realmente la razón
Para probar si este efecto protector realmente implicaba a ERK5, los investigadores redujeron o eliminaron completamente ERK5 en varias líneas celulares cancerosas usando herramientas genéticas, incluyendo ARN de horquilla corta y edición génica CRISPR. Si ERK5 fuera esencial para la acción antiferroptótica de estos compuestos, entonces eliminar ERK5 debería abolir la protección. En cambio, XMD8-92 y JWG-045 continuaron rescatando células de la muerte inducida por RSL3 incluso cuando ERK5 era apenas detectable o estaba completamente ausente. En contraste, JWG-071 y BAY-885 seguían sin efecto. El equipo también descartó un objetivo fuera de diana conocido, la proteína asociada a la cromatina BRD4, porque inhibidores específicos de BRD4 no imitaron el comportamiento de bloqueo de la ferroptosis. En conjunto, estos resultados apuntan a una actividad fuera de objetivo previamente no reconocida, exclusiva de XMD8-92 y JWG-045.
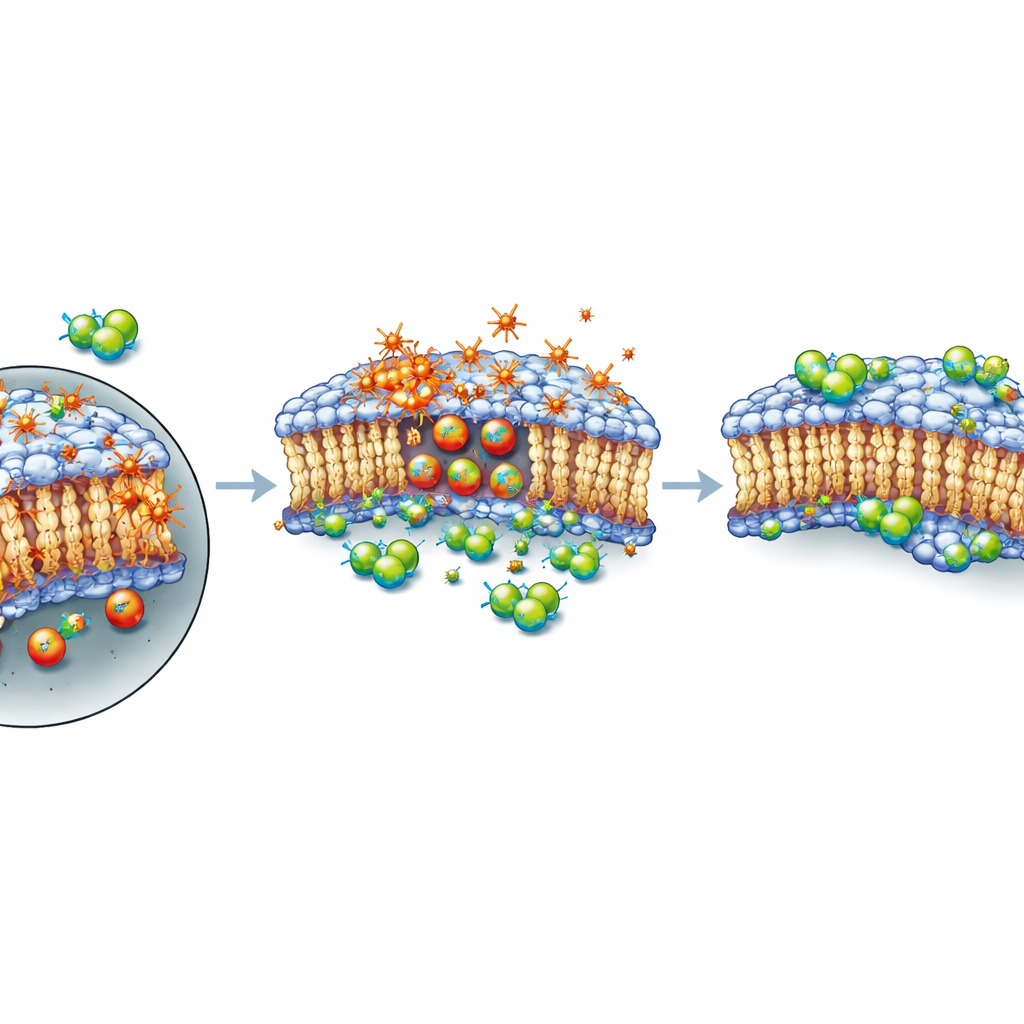
Un escudo para la piel exterior de la célula, no un freno al daño
A continuación, los autores se preguntaron cómo intervenían estos compuestos en el proceso de muerte. Al rastrear la actividad génica durante varias horas tras el tratamiento con XMD8-92, observaron solo cambios modestos en genes relacionados con la ferroptosis y ningún cambio claro y coordinado en la señalización global de ferroptosis. Usando un tinte fluorescente que se ilumina con los lípidos oxidados, mostraron que XMD8-92 no detenía la peroxidación lipídica; si acaso, la oxidación aumentó cuando las células recibieron tanto RSL3 como XMD8-92. Sin embargo, las células seguían sobreviviendo mejor. En experimentos cronometrados con cuidado, una breve exposición a RSL3 por sí sola fue suficiente para sellar el destino de las células, incluso después de lavar el fármaco. Pero si XMD8-92 se añadía tras ese pulso corto, muchas células se recuperaban. Este patrón sugiere que el compuesto no previene el daño químico inicial; en su lugar, parece ayudar a mantener o reparar la membrana plasmática, al menos temporalmente, de modo que las células puedan soportar un periodo de intenso estrés oxidativo antes de sucumbir eventualmente si el daño continúa acumulándose.
Qué significa esto para la investigación del cáncer y el diseño de fármacos
Para los no especialistas, el mensaje principal es que no todos los fármacos se comportan como indican sus etiquetas. Dos moléculas ampliamente utilizadas para estudiar e inhibir ERK5 resultan tener un efecto adicional y potente: pueden retrasar una forma de muerte celular impulsada por hierro y ruptura de membrana sin detener realmente el daño químico subyacente. Esta protección fuera de objetivo es importante por dos razones. Primero, advierte a los investigadores de que los resultados obtenidos con XMD8-92 y JWG-045 pueden no reflejar de forma fiable lo que ocurre cuando solo se bloquea ERK5. Segundo, sugiere la existencia de mecanismos accesibles a fármacos que refuerzan la reparación de membranas durante estrés extremo, que en el futuro podrían aprovecharse para proteger tejidos sanos en enfermedades donde la ferroptosis se descontrole. Por ahora, el trabajo subraya la necesidad de combinar inhibidores más nuevos y selectivos con herramientas genéticas al investigar la biología de ERK5, y de tratar las correlaciones entre niveles génicos y respuestas a fármacos con cautela, en lugar de asumir una relación directa de causa y efecto.
Cita: Zhang, W., Kan, K., Pidd, A.B. et al. XMD8-92 and JWG-045 exhibit anti-ferroptotic activities, independently of inhibiting ERK5. Sci Rep 16, 11337 (2026). https://doi.org/10.1038/s41598-026-42079-w
Palabras clave: ferroptosis, inhibidores de ERK5, cáncer de mama, vías de muerte celular, efectos fuera de objetivo de fármacos