Clear Sky Science · de
XMD8-92 und JWG-045 zeigen anti‑ferroptotische Aktivitäten, unabhängig von der Hemmung von ERK5
Warum das Schützen sterbender Krebszellen uns trotzdem viel lehren kann
Krebsforscher untersuchen eine überraschende Form des Zelltods namens Ferroptose, bei der Eisen und geschädigte Fette zusammenwirken und Löcher in Zellmembranen reißen. Da viele schwer zu behandelnde Tumore ungewöhnlich anfällig für diesen Prozess sind, werden Wirkstoffe, die Ferroptose auslösen, als neue Methode getestet, Krebszellen zu töten. Diese Studie wollte klären, ob die Hemmung eines krebsfördernden Proteins, ERK5, beeinflusst, wie Brustkrebszellen auf Ferroptose reagieren. Dabei entdeckten die Forschenden eine unerwartete Wendung: Zwei weit verbreitete ERK5‑blockierende Substanzen schützen Krebszellen vor ferroptotischem Tod über einen völlig anderen Weg.
Wie ein Stress‑Signalprotein auf einen ungewöhnlichen Todesweg trifft
ERK5 ist Teil eines Signalsystems, das Zellen hilft, auf Wachstumsreize und Stressbedingungen zu reagieren. Tumore mit hoher ERK5‑Aktivität wachsen häufig schneller, breiten sich leichter aus und sind gegen andere gezielte Therapien resistent. Eine andere Forschungsrichtung hat gezeigt, dass ein schützendes Enzym namens GPX4, das normalerweise schädliche Peroxide in Zellmembranen beseitigt, entscheidend ist, um Ferroptose zu verhindern. Wenn GPX4 durch Substanzen wie RSL3 blockiert wird, oxidieren Membranlipide, die Membran bricht allmählich zusammen und die Zelle stirbt auf charakteristische, eisenabhängige Weise. Da ERK5 physisch mit GPX4 interagieren kann, fragten die Autorinnen und Autoren, ob dieses Stress‑Signalprotein Krebszellen empfindlicher oder widerstandsfähiger gegenüber Ferroptose machen könnte.
Wirkstoffe, die helfen, und solche, die nichts bewirken
Das Team durchforstete zunächst große Krebszell‑Datenbanken und stellte fest, dass Tumore mit hohem ERK5‑Spiegel tendenziell empfindlicher gegenüber GPX4‑blockierenden Wirkstoffen waren, besonders wenn die Zellen einen mobileren, aggressiveren sogenannten mesenchymalen Zustand angenommen hatten. Anschließend führten sie Laborversuche mit mehreren Brust‑ und Gebärmutterhalskrebszelllinien durch. Als sie Zellen mit RSL3 behandelten, um Ferroptose auszulösen, hielten zwei ERK5‑gerichtete Verbindungen, XMD8‑92 und JWG‑045, unerwartet viele Zellen am Leben. Andere Inhibitoren, die auf denselben Signalweg abzielen — neuere ERK5‑Blocker JWG‑071 und BAY‑885 sowie ein Wirkstoff, der einen Schritt stromaufwärts an MEK5 wirkt — boten diesen Schutz nicht. In allen Fällen verhielt sich das übliche Ferroptose‑Blockermolekül Ferrostatin‑1 wie erwartet, was bestätigte, dass RSL3 die Zellen tatsächlich über Ferroptose tötete.
Wenn das Blockieren des Zielproteins nicht wirklich der Grund ist
Um zu prüfen, ob dieser schützende Effekt wirklich ERK5 einbezog, reduzierten oder entfernten die Forschenden ERK5 in mehreren Krebszelllinien mithilfe genetischer Werkzeuge, darunter short hairpin‑RNA und CRISPR‑Geneditierung. Wenn ERK5 für die anti‑ferroptotische Wirkung dieser Wirkstoffe essentiell wäre, müsste das Löschen von ERK5 den Schutz aufheben. Stattdessen retteten XMD8‑92 und JWG‑045 weiterhin Zellen vor RSL3‑induziertem Tod, selbst wenn ERK5 kaum nachweisbar oder vollständig abwesend war. Im Gegensatz dazu zeigten JWG‑071 und BAY‑885 weiterhin keine Wirkung. Das Team schloss auch ein bekanntes Off‑Target, das chromatinassoziierte Protein BRD4, aus, weil separate BRD4‑Inhibitoren das ferroptoseblockierende Verhalten nicht nachahmten. Zusammen deuten diese Ergebnisse auf eine zuvor unerkannte Off‑Target‑Aktivität hin, die XMD8‑92 und JWG‑045 gemeinsam ist.
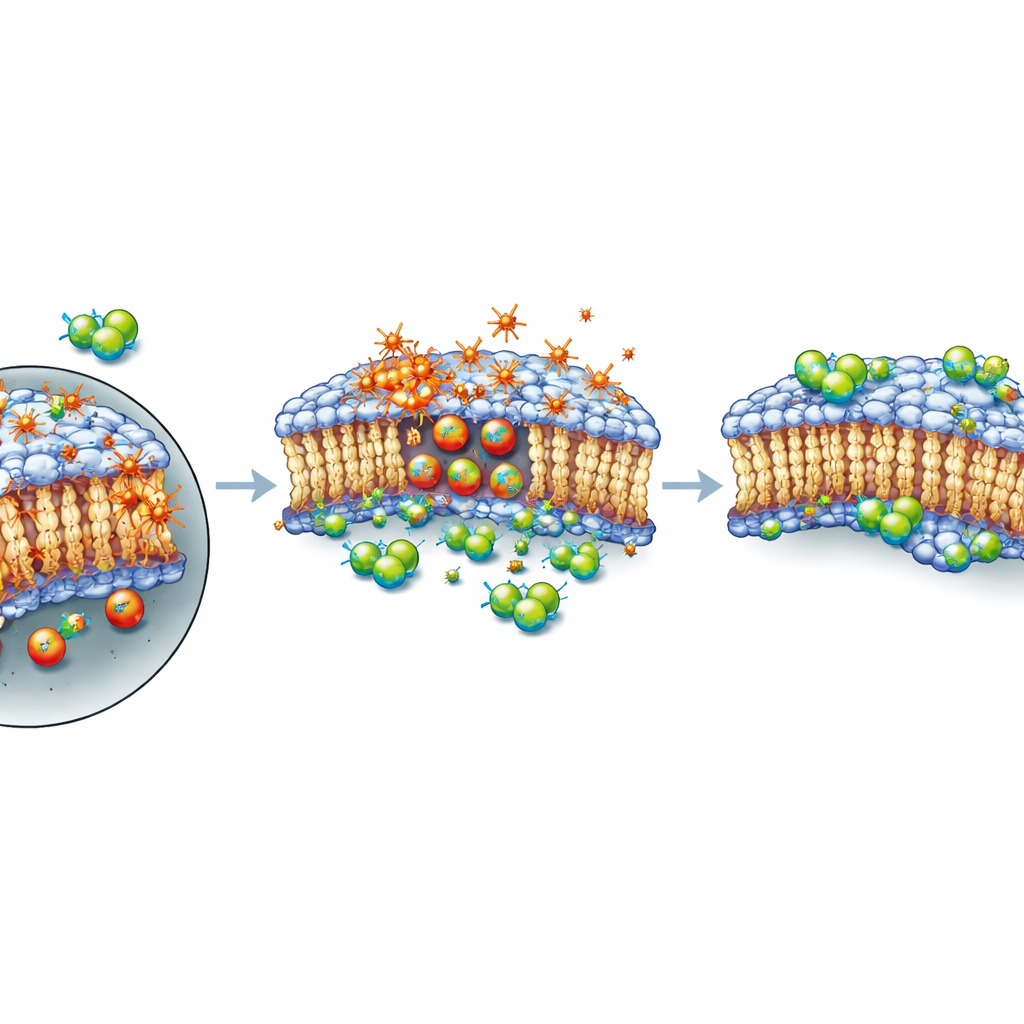
Ein Schutzschild für die Außenhaut der Zelle, kein Bremsklotz für den Schaden
Als Nächstes fragten die Autorinnen und Autoren, wie diese Verbindungen in den Todesprozess eingreifen. Durch die Verfolgung der Genaktivität über mehrere Stunden nach XMD8‑92‑Behandlung sahen sie nur moderate Verschiebungen bekannter ferroptosebezogener Gene und keine klare, koordinierte Änderung im gesamten Ferroptose‑Signalnetzwerk. Mittels eines fluoreszierenden Farbstoffs, der oxidierte Fette sichtbar macht, zeigten sie, dass XMD8‑92 die Lipidperoxidation nicht stoppte; wenn überhaupt, nahm die Oxidation zu, wenn Zellen sowohl RSL3 als auch XMD8‑92 erhielten. Dennoch überlebten die Zellen besser. In zeitlich genau gesteuerten Experimenten reichte eine kurze Exposition gegenüber RSL3 allein aus, um das Schicksal der Zellen zu besiegeln, selbst nachdem das Medikament weggewaschen worden war. Wurde jedoch XMD8‑92 nach dieser kurzen Pulsexposition hinzugefügt, erholten sich viele Zellen. Dieses Muster legt nahe, dass die Verbindung den initialen chemischen Schaden nicht verhindert; stattdessen scheint sie zu helfen, die Plasmamembran vorübergehend aufrechtzuerhalten oder zu reparieren, sodass Zellen eine Phase intensiven oxidativen Stresses überstehen können, bevor sie bei anhaltender Schädigung schließlich unterliegen.
Was das für Krebsforschung und Wirkstoffentwicklung bedeutet
Für Nicht‑Spezialisten lautet die Kernbotschaft: Nicht alle Wirkstoffe verhalten sich so, wie ihr Etikett suggeriert. Zwei Moleküle, die breit zur Erforschung und Hemmung von ERK5 verwendet werden, weisen eine zusätzliche, starke Wirkung auf: Sie können eine Form des eisengetriebenen, membrandurchstoßenden Zelltods verzögern, ohne die zugrunde liegende chemische Schädigung tatsächlich zu stoppen. Diese Off‑Target‑Schutzwirkung ist aus zwei Gründen wichtig. Erstens warnt sie Forschende davor, dass mit XMD8‑92 und JWG‑045 gewonnene Ergebnisse möglicherweise nicht zuverlässig widerspiegeln, was passiert, wenn nur ERK5 blockiert wird. Zweitens deutet sie auf die Existenz von medikabel zugänglichen Mechanismen hin, die die Membranreparatur unter extremem Stress stärken — Mechanismen, die eines Tages genutzt werden könnten, um gesundes Gewebe in Erkrankungen zu schützen, in denen Ferroptose außer Kontrolle gerät. Für den Moment unterstreicht die Arbeit die Notwendigkeit, neuere, selektivere Inhibitoren mit genetischen Werkzeugen zu kombinieren, wenn ERK5‑Biologie untersucht wird, und Korrelationen zwischen Genleveln und Wirkstoffantworten mit Vorsicht zu behandeln, statt eine direkte Kausalität vorauszusetzen.
Zitation: Zhang, W., Kan, K., Pidd, A.B. et al. XMD8-92 and JWG-045 exhibit anti-ferroptotic activities, independently of inhibiting ERK5. Sci Rep 16, 11337 (2026). https://doi.org/10.1038/s41598-026-42079-w
Schlüsselwörter: Ferroptose, ERK5-Inhibitoren, Brustkrebs, Zelltod‑Signalwege, Off‑Target‑Wirkungen von Wirkstoffen