Clear Sky Science · pl
XMD8-92 i JWG-045 wykazują aktywność anty-ferroptotyczną, niezależnie od hamowania ERK5
Dlaczego ochrona umierających komórek nowotworowych może wciąż wiele nas nauczyć
Naukowcy badają zaskakującą formę śmierci komórkowej zwaną ferroptozą, w której żelazo i utlenione lipidy współdziałają, tworząc uszkodzenia błon komórkowych. Ponieważ wiele trudnych do leczenia nowotworów jest szczególnie podatnych na ten proces, leki wywołujące ferroptozę testowane są jako nowy sposób zabijania komórek nowotworowych. W tym badaniu postanowiono sprawdzić, czy blokowanie białka sprzyjającego rakowi, ERK5, wpływa na wrażliwość komórek raka piersi na ferroptozę. W trakcie prac badacze odkryli niespodziewany zwrot akcji: dwie powszechnie używane substancje blokujące ERK5 w rzeczywistości chronią komórki nowotworowe przed śmiercią ferroptotyczną poprzez zupełnie inny mechanizm.
Jak białko sygnalizujące stres spotyka nietypową ścieżkę śmierci
ERK5 jest częścią sieci sygnalizacyjnej, która pomaga komórkom reagować na sygnały wzrostu i warunki stresowe. Guzy o wysokiej aktywności ERK5 często rosną szybciej, łatwiej się rozprzestrzeniają i wykazują oporność na inne leki celowane. Równoległa linia badań wykazała, że enzym ochronny GPX4, który zwykle usuwa szkodliwe nadtlenki z błon komórkowych, jest niezbędny do zapobiegania ferroptozie. Gdy GPX4 jest blokowany przez substancje takie jak RSL3, lipidy w błonie ulegają utlenieniu, błona stopniowo się rozpada i komórka obumiera w charakterystyczny, zależny od żelaza sposób. Ponieważ ERK5 może fizycznie wchodzić w interakcję z GPX4, autorzy zastanawiali się, czy to białko sygnalizujące stres może zwiększać lub zmniejszać wrażliwość komórek nowotworowych na ferroptozę.
Leki, które pomagają, i leki, które nic nie robią
Zespół najpierw przeanalizował duże bazy danych komórek nowotworowych i stwierdził, że guzy o wysokim poziomie ERK5 mają tendencję do większej wrażliwości na leki blokujące GPX4, zwłaszcza gdy komórki przyjęły bardziej ruchliwy, agresywny stan zwany mezenchymalnym. Następnie przeprowadzono eksperymenty laboratoryjne na kilku liniach komórek raka piersi i szyjki macicy. Gdy komórki traktowano RSL3, aby wywołać ferroptozę, dwie związki celujące w ERK5, XMD8-92 i JWG-045, nieoczekiwanie utrzymywały przy życiu wiele komórek. Inne inhibitory ukierunkowane na tę samą ścieżkę — nowsze blokery ERK5 JWG-071 i BAY-885 oraz lek działający krok wcześniej, na MEK5 — nie zapewniały takiej ochrony. We wszystkich przypadkach standardowa cząsteczka blokująca ferroptozę, Ferrostatyna-1, zachowywała się zgodnie z oczekiwaniami, potwierdzając, że RSL3 rzeczywiście zabijał komórki przez ferroptozę.
Kiedy blokowanie celu nie jest właściwą przyczyną
Aby sprawdzić, czy efekt ochronny rzeczywiście obejmuje ERK5, badacze zmniejszyli lub całkowicie usunęli ERK5 z kilku linii komórkowych przy użyciu narzędzi genetycznych, w tym krótkich włosowatych RNA (shRNA) i edycji genów CRISPR. Gdyby ERK5 był niezbędny dla anty-ferroptotycznego działania tych leków, usunięcie ERK5 powinno było znieść ochronę. Zamiast tego XMD8-92 i JWG-045 nadal ratowały komórki przed śmiercią wywołaną przez RSL3, nawet gdy ERK5 był ledwie wykrywalny lub całkowicie nieobecny. Dla porównania, JWG-071 i BAY-885 nadal nie wykazywały efektu. Zespół wykluczył także znany efekt pozacelemowy — białko związane z chromatyną BRD4 — ponieważ inne inhibitory BRD4 nie naśladowały zachowania blokującego ferroptozę. Razem te wyniki wskazują na wcześniej nieznaną aktywność pozacelemową charakterystyczną dla XMD8-92 i JWG-045.
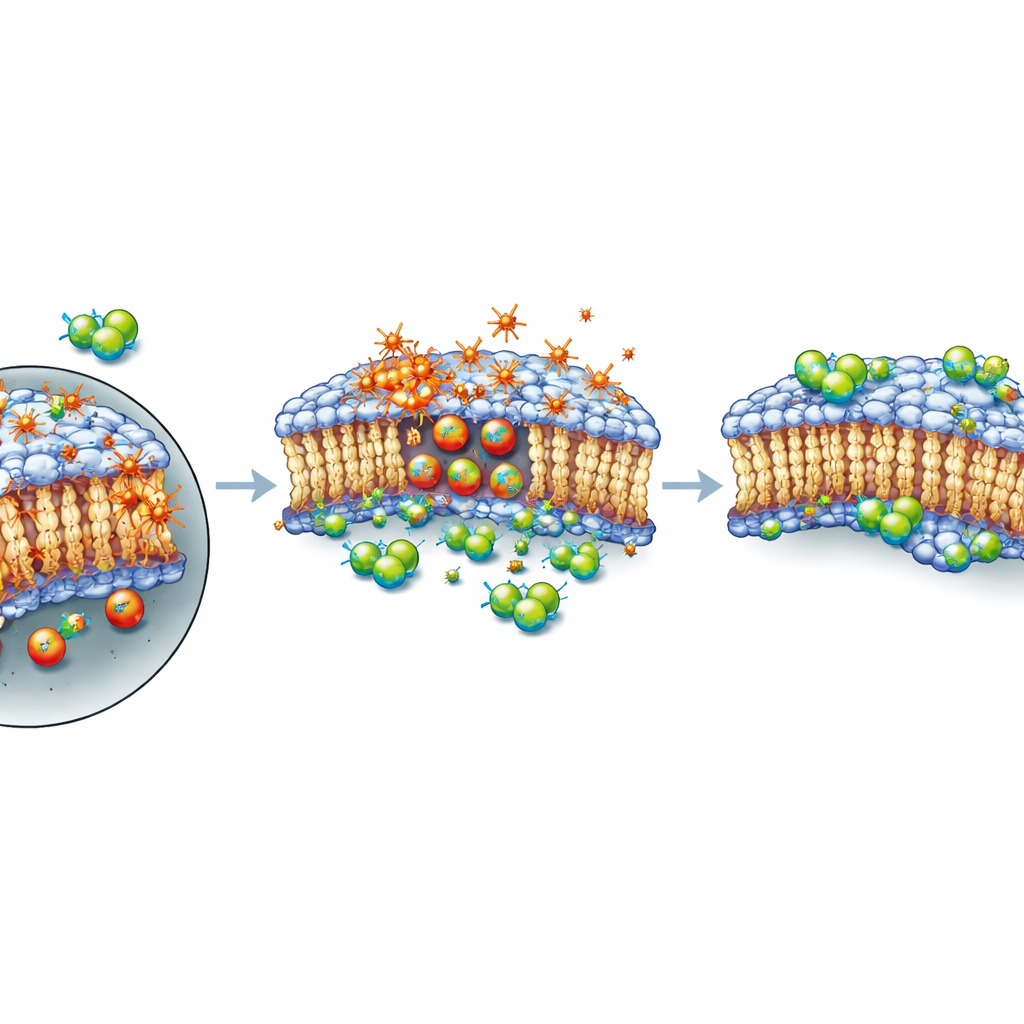
Tarcza dla zewnętrznej powłoki komórki, a nie hamulec dla uszkodzeń
Następnie autorzy zapytali, jak te związki ingerują w proces śmierci. Śledząc aktywność genów przez kilka godzin po podaniu XMD8-92, zauważyli jedynie umiarkowane zmiany w znanych genach związanych z ferroptozą i brak wyraźnej, skoordynowanej zmiany w ogólnym sygnale ferroptotycznym. Używając fluorescencyjnego barwnika, który świeci w obecności utlenionych lipidów, pokazali, że XMD8-92 nie zatrzymuje peroksydacji lipidów; jeśli w ogóle, utlenianie wzrastało, gdy komórki otrzymały zarówno RSL3, jak i XMD8-92. Mimo to komórki przeżywały lepiej. W starannie zaplanowanych eksperymentach krótka ekspozycja tylko na RSL3 wystarczyła, by przypieczętować los komórek, nawet po wypłukaniu leku. Jednak jeśli XMD8-92 dodano po tym krótkim impulsie, wiele komórek zdołało się zregenerować. Ten wzorzec sugeruje, że związek nie zapobiega początkowemu uszkodzeniu chemicznemu; zamiast tego wydaje się wspierać utrzymanie lub naprawę błony plazmatycznej, przynajmniej tymczasowo, tak że komórki mogą wytrzymać okres intensywnego stresu oksydacyjnego, zanim ostatecznie ulegną, jeśli uszkodzenia będą dalej narastać.
Co to znaczy dla badań nad rakiem i projektowania leków
Dla osób spoza specjalności główne przesłanie jest takie, że nie wszystkie leki zachowują się zgodnie z tym, co sugerują ich etykiety. Dwie cząsteczki powszechnie używane do badania i hamowania ERK5 okazują się mieć dodatkowy, silny efekt: mogą opóźniać formę żelazozależnej, prowadzącej do rozerwania błony śmierci komórkowej, nie zatrzymując przy tym podstawowego uszkodzenia chemicznego. Ta ochrona pozacelemowa jest ważna z dwóch powodów. Po pierwsze, ostrzega badaczy, że wyniki uzyskane przy użyciu XMD8-92 i JWG-045 mogą nie odzwierciedlać rzetelnie tego, co dzieje się przy samodzielnym zablokowaniu ERK5. Po drugie, sugeruje istnienie dostępnych dla leków mechanizmów wzmacniających naprawę błony w warunkach ekstremalnego stresu, które w przyszłości mogłyby zostać wykorzystane do ochrony zdrowych tkanek w chorobach, gdzie ferroptoza wymyka się spod kontroli. Na razie praca podkreśla potrzebę łączenia nowszych, bardziej selektywnych inhibitorów z narzędziami genetycznymi przy badaniu biologii ERK5 oraz ostrożnego traktowania korelacji między poziomami genów a odpowiedziami na leki, zamiast zakładania bezpośredniej przyczynowości.
Cytowanie: Zhang, W., Kan, K., Pidd, A.B. et al. XMD8-92 and JWG-045 exhibit anti-ferroptotic activities, independently of inhibiting ERK5. Sci Rep 16, 11337 (2026). https://doi.org/10.1038/s41598-026-42079-w
Słowa kluczowe: ferroptoza, inhibitory ERK5, rak piersi, ścieżki śmierci komórkowej, efekty pozacelemowe leków