Clear Sky Science · nl
XMD8-92 en JWG-045 vertonen anti-ferroptotische activiteit, onafhankelijk van remming van ERK5
Waarom het beschermen van stervende kankercellen ons nog veel kan leren
Kankeronderzoekers bestuderen een verrassende vorm van celdood genaamd ferroptose, waarbij ijzer en beschadigde vetten samenwerken om gaten in celmembranen te slaan. Omdat veel moeilijk te behandelen tumoren ongewoon kwetsbaar zijn voor dit proces, worden geneesmiddelen die ferroptose induceren getest als een nieuwe manier om kankercellen te doden. In deze studie wilden de onderzoekers nagaan of het blokkeren van een kankerverhogend eiwit, ERK5, beïnvloedt hoe borstkankecellen reageren op ferroptose. Daarbij ontdekten ze een onverwachte wending: twee veelgebruikte ERK5-remmende chemicaliën beschermen kankercellen juist tegen ferroptotische dood via een geheel andere route.
Hoe een stress‑signalerend eiwit een ongebruikelijke doodroute ontmoet
ERK5 maakt deel uit van een signaleringsnetwerk dat cellen helpt te reageren op groeisignalen en stressvolle omstandigheden. Tumoren met hoge ERK5-activiteit groeien vaak sneller, verspreiden zich gemakkelijker en zijn bestand tegen andere gerichte geneesmiddelen. Een afzonderlijke onderzoekslijn heeft aangetoond dat een beschermend enzym, GPX4, dat normaal schadelijke peroxiden uit celmembranen verwijdert, essentieel is om ferroptose te voorkomen. Wanneer GPX4 wordt geblokkeerd door chemicaliën zoals RSL3, raken vetten in het celmembraan geoxideerd, breekt het membraan geleidelijk af en sterft de cel op een karakteristieke, ijzerafhankelijke manier. Omdat ERK5 fysiek kan interageren met GPX4, vroegen de auteurs zich af of dit stress‑signalerende eiwit kankercellen gevoeliger of juist minder gevoelig voor ferroptose zou maken.
Geneesmiddelen die helpen en middelen die niets doen
Het team doorzocht eerst grote kankercel-databases en vond dat tumoren met hoge ERK5-niveaus vaker gevoeliger leken voor GPX4-blokkerende middelen, vooral wanneer de cellen een mobielere, agressievere zogenoemde mesenchymale staat hadden aangenomen. Vervolgens gingen ze over op labo-experimenten met verschillende borstkanker- en baarmoederhalskankercellijnen. Wanneer ze cellen behandelden met RSL3 om ferroptose te induceren, hielden twee ERK5-gerichte verbindingen, XMD8-92 en JWG-045, onverwacht veel cellen in leven. Andere remmers die op hetzelfde signaleringspad gericht zijn — nieuwere ERK5-remmers JWG-071 en BAY-885, en een geneesmiddel dat een stap stroomopwaarts werkt op MEK5 — boden deze bescherming niet. In alle gevallen gedroeg de standaard ferroptose-remmer Ferrostatin-1 zich zoals verwacht, wat bevestigde dat RSL3 cellen daadwerkelijk via ferroptose dode.
Wanneer het blokkeren van een doelwit niet echt de reden is
Om te testen of dit beschermende effect werkelijk ERK5 betrof, verminderden of verwijderden de onderzoekers ERK5 in meerdere kankercellijnen met behulp van genetische middelen, waaronder short hairpin RNA en CRISPR-genbewerking. Als ERK5 essentieel zou zijn voor de anti‑ferroptotische werking van deze middelen, dan zou het deleten van ERK5 die bescherming moeten wegnemen. In plaats daarvan bleven XMD8-92 en JWG-045 cellen redden van RSL3-geïnduceerde dood, zelfs wanneer ERK5 nauwelijks detecteerbaar of geheel afwezig was. Ter vergelijking hadden JWG-071 en BAY-885 nog steeds geen effect. Het team sloot ook één bekende off-target, het chromatine-geassocieerde eiwit BRD4, uit omdat afzonderlijke BRD4-remmers het ferroptose-blokkerende gedrag niet nabootsten. Gezamenlijk wezen deze resultaten op een eerder niet-herkende off-target activiteit die uniek is voor XMD8-92 en JWG-045.
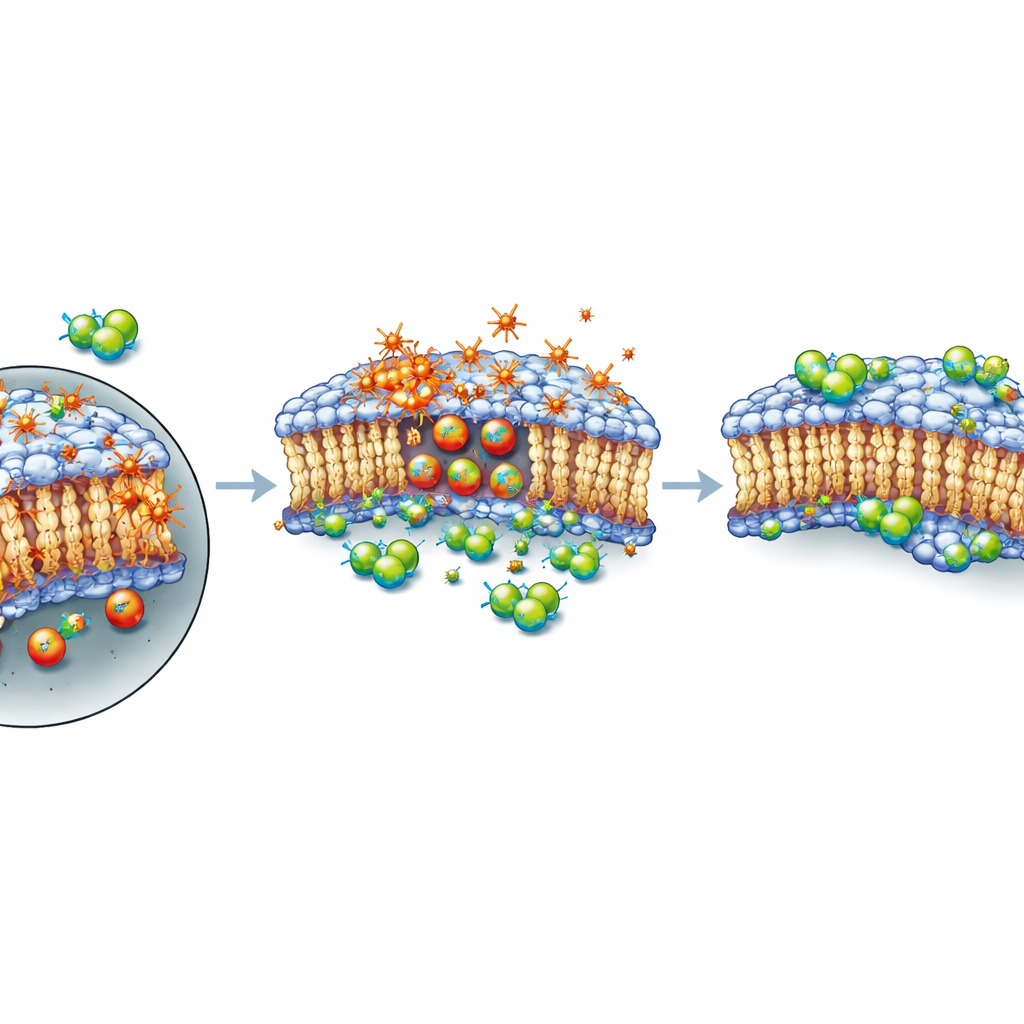
Een schild voor de buitenste huid van de cel, geen rem op de schade
Vervolgens vroegen de auteurs hoe deze verbindingen intervenieerden in het doodsproces. Door de genactiviteit enkele uren na XMD8-92-behandeling te volgen, zagen ze slechts bescheiden verschuivingen in bekende ferroptose-gerelateerde genen en geen duidelijke, gecoördineerde verandering in de algehele ferroptose-signalisatie. Met een fluorescente kleurstof die geoxideerde vetten laat oplichten, toonden ze aan dat XMD8-92 de lipideperoxidatie niet stopte; zo mogelijk nam de oxidatie toe wanneer cellen zowel RSL3 als XMD8-92 ontvingen. Toch overleefden cellen beter. In nauw getimede experimenten was een korte blootstelling aan RSL3 alleen al genoeg om het lot van cellen te bezegelen, zelfs nadat het middel werd weggespoeld. Maar als XMD8-92 na die korte puls werd toegevoegd, herstelden veel cellen zich. Dit patroon suggereert dat de verbinding de initiële chemische schade niet voorkomt; in plaats daarvan lijkt het te helpen het plasmamembraan te onderhouden of te herstellen, althans tijdelijk, zodat cellen een periode van intense oxidatieve stress kunnen doorstaan voordat ze uiteindelijk bezwijken als de schade blijft oplopen.
Wat dit betekent voor kankeronderzoek en geneesmiddelontwerp
Voor niet‑specialisten is de kernboodschap dat niet alle geneesmiddelen zich gedragen zoals hun etiketten suggereren. Twee moleculen die veel worden gebruikt om ERK5 te bestuderen en te remmen, blijken een extra, krachtige werking te hebben: ze kunnen een vorm van ijzer‑gedreven, membraan‑scheurende celdood uitstellen zonder de onderliggende chemische schade daadwerkelijk te stoppen. Deze off-target bescherming is belangrijk om twee redenen. Ten eerste waarschuwt het onderzoekers dat resultaten verkregen met XMD8-92 en JWG-045 mogelijk niet betrouwbaar weergeven wat er gebeurt wanneer uitsluitend ERK5 wordt geblokkeerd. Ten tweede suggereert het het bestaan van geneesmiddel-bereikbare mechanismen die membraanherstel versterken tijdens extreme stress, wat ooit gebruikt zou kunnen worden om gezonde weefsels te beschermen in ziekten waar ferroptose uit de hand loopt. Voor nu onderstreept dit werk de noodzaak om nieuwere, meer selectieve remmers te combineren met genetische tools bij het onderzoeken van ERK5-biologie, en om correlaties tussen genexpressie en geneesmiddelreacties met voorzichtigheid te behandelen in plaats van een directe oorzaak‑en‑gevolgrelatie aan te nemen.
Bronvermelding: Zhang, W., Kan, K., Pidd, A.B. et al. XMD8-92 and JWG-045 exhibit anti-ferroptotic activities, independently of inhibiting ERK5. Sci Rep 16, 11337 (2026). https://doi.org/10.1038/s41598-026-42079-w
Trefwoorden: ferroptose, ERK5-remmers, borstkanker, celdoodroutes, off-target effecten van geneesmiddelen