Clear Sky Science · ar
تظهر XMD8-92 و JWG-045 نشاطات مضادة للفيروبتوزيس، مستقلة عن تثبيط ERK5
لماذا يمكن لحماية الخلايا السرطانية المحتضرة أن تعلمنا الكثير
يستكشف باحثو السرطان شكلاً مفاجئًا من موت الخلايا يُسمى الفيروبتوزيس، حيث يتعاون الحديد والدهون المتأكسدة لثقب أغشية الخلايا. وبما أن العديد من الأورام شديدة المقاومة للعلاج تكون عرضة بشكل غير اعتيادي لهذه العملية، تُجرَّب أدوية تُحفِّز الفيروبتوزيس كطريقة جديدة لقتل الخلايا السرطانية. هدفت هذه الدراسة إلى فحص ما إذا كان حجب بروتين يروّج للسرطان، ERK5، يؤثر على استجابة خلايا سرطان الثدي للفيروبتوزيس. وخلال ذلك، اكتشف الباحثون مفاجأة: مركبان كيميائيان مستخدمان على نطاق واسع لوقف ERK5 يحميان الخلايا السرطانية من الموت الفيروبتوزيتي عبر مسار مختلف تمامًا.
كيف يلتقي بروتين إشارة الإجهاد بمسار موت غير اعتيادي
يعد ERK5 جزءًا من شبكة إشارات تساعد الخلايا على الاستجابة لإشارات النمو والظروف المجهدة. عادةً ما تنمو الأورام ذات نشاط ERK5 العالي أسرع وتنتشر بسهولة أكبر وتقاوم أدويةً مستهدفة أخرى. وقد أوضح خط بحثي منفصل أن إنزيمًا حمائيًا يُسمى GPX4، الذي يزيل فوق الأكاسيد الضارة من أغشية الخلايا، ضروري لمنع الفيروبتوزيس. عندما يُثبَّط GPX4 بواسطة مركبات مثل RSL3، تتأكسد الدهون في غشاء الخلية، ويتحلل الغشاء تدريجيًا، وتموت الخلية بطريقة مميزة تعتمد على الحديد. وبما أن ERK5 يمكن أن يتفاعل ماديًا مع GPX4، تساءل المؤلفون عما إذا كان بروتين إشارات الإجهاد هذا قد يجعل الخلايا السرطانية أكثر أو أقل حساسية للفيروبتوزيس.
أدوية تساعد وأدوية لا تفعل شيئًا
في البداية استخرج الفريق بيانات من قواعد كبيرة للخلايا السرطانية ووجد أن الأورام ذات مستويات ERK5 العالية تميل إلى أن تكون أكثر حساسية لأدوية حجب GPX4، خاصة عندما تتبنى الخلايا حالة مسخيّة أكثر حركة وعدوانية. ثم انتقلوا إلى تجارب مخبرية باستخدام عدة خطوط خلوية من سرطان الثدي وسرطان عنق الرحم. عندما عولجت الخلايا بـ RSL3 لتحفيز الفيروبتوزيس، أبقت مركباتان موجهتان ضد ERK5، هما XMD8-92 وJWG-045، عدداً كبيرًا من الخلايا على قيد الحياة على نحو غير متوقع. لم تمنح مثبطات أخرى تستهدف نفس مسار الإشارة—مثبطات ERK5 الأحدث JWG-071 وBAY-885، ودواء يعمل خطوة إلى أعلى عند MEK5—مثل هذه الحماية. وفي كل الحالات تصرف الجزيء المعروف بمانع الفيروبتوزيس Ferrostatin-1 كما كان متوقعًا، مؤكدًا أن RSL3 كان بالفعل يقتل الخلايا عن طريق الفيروبتوزيس.
عندما لا يكون حجب الهدف هو السبب الحقيقي
لاختبار ما إذا كانت هذه الحماية تنطوي فعلاً على ERK5، قلل الباحثون أو أزالوا ERK5 تمامًا من عدة خطوط خلوية سرطانية باستخدام أدوات وراثية، بما في ذلك الحمض النووي الريبي صغير الشعرة والتحرير الجيني CRISPR. لو كان ERK5 ضروريًا للعمل المضاد للفيروبتوزيس لهذه الأدوية، لكان حذف ERK5 سيلغي الحماية. بدلاً من ذلك، استمرت XMD8-92 وJWG-045 في إنقاذ الخلايا من الموت الناتج عن RSL3 حتى عندما أصبح ERK5 بالكاد قابلاً للكشف أو غائبًا تمامًا. في المقابل، لم تُظهر JWG-071 وBAY-885 أي تأثير. كما استبعد الفريق هدفًا خارجيًا معروفًا وهو البروتين المرتبط بالكروماتين BRD4، لأن مثبطات BRD4 المنفصلة لم تقلد سلوك حجب الفيروبتوزيس. مجتمعة، أشارت هذه النتائج إلى وجود نشاط خارج الهدف لم يُعترف به سابقًا ومميّز لـ XMD8-92 وJWG-045.
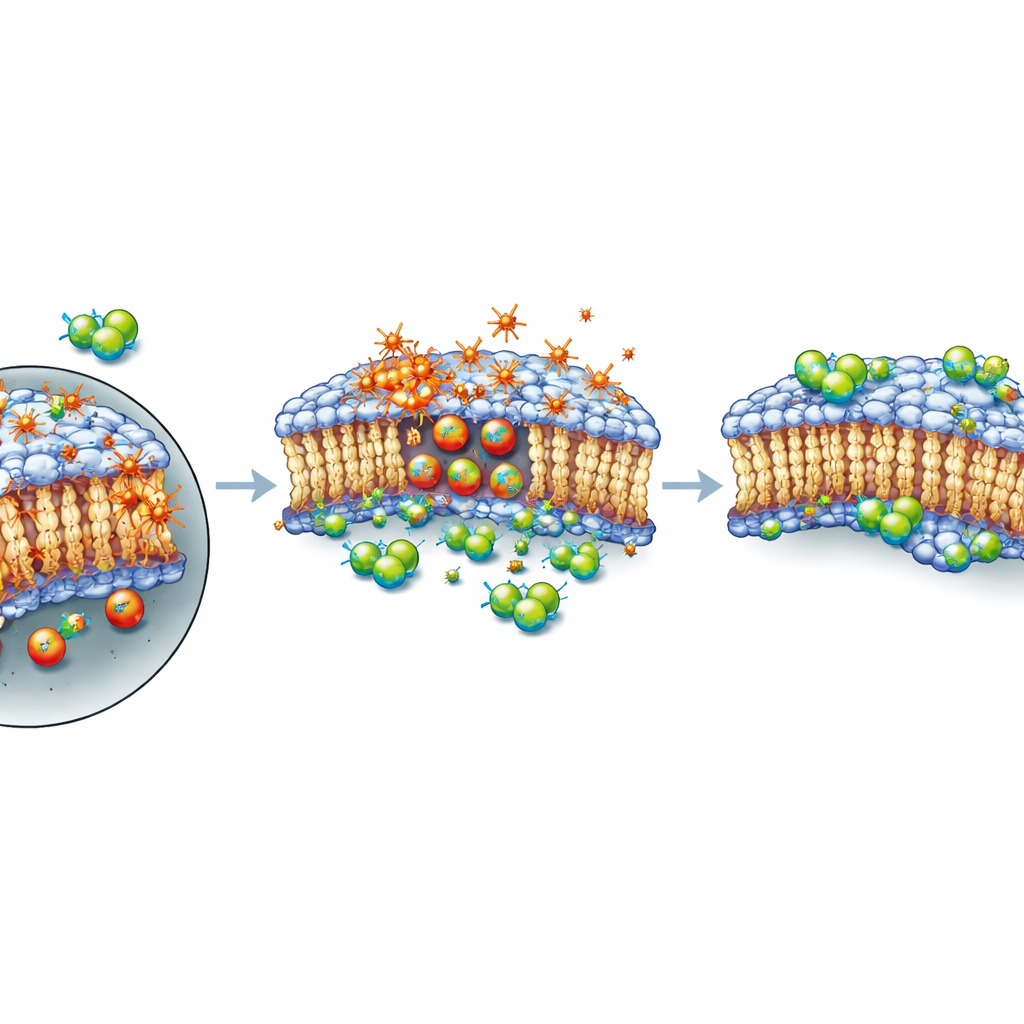
درع لجلد الخلية الخارجي، لا فرملة للضرر
سأل المؤلفون بعد ذلك كيف تتدخل هذه المركبات في عملية الموت. بتتبع نشاط الجينات على مدى عدة ساعات بعد علاج XMD8-92، رصدوا تغيرات متواضعة فقط في الجينات المعروفة المرتبطة بالفيروبتوزيس ولم يروا تغيرًا منسقًا واضحًا في إشارة الفيروبتوزيس الكلية. باستخدام صبغة فلورية تضيء الدهون المؤكسدة، أظهروا أن XMD8-92 لم يوقف تأكسد الدهون؛ إن أصاب الأمر زيادة في التأكسد عند تلقي الخلايا كل من RSL3 وXMD8-92. ومع ذلك بقيت الخلايا أكثر بقاءً. في تجارب مُؤقّتة بعناية، كانت فترة قصيرة من التعرض لـ RSL3 بمفردها كافية لربط مصير الخلايا، حتى بعد غسل الدواء. لكن إذا أضيف XMD8-92 بعد ذلك النبضة القصيرة، تعافت العديد من الخلايا. يقترح هذا النمط أن المركب لا يمنع الضرر الكيميائي الأولي؛ بل يبدو أنه يساعد في الحفاظ على غشاء البلازما أو إصلاحه، على الأقل مؤقتًا، بحيث تتحمّل الخلايا فترة من الإجهاد التأكسدي الشديد قبل أن تنهار في النهاية إذا استمر تراكم الضرر.
ما معنى هذا لبحوث السرطان وتصميم الأدوية
بالنسبة لغير المتخصصين، الرسالة الأساسية هي أن ليس كل الأدوية تتصرف كما توحي تسميتها. يظهر أن جزيئين مستخدمين على نطاق واسع لدراسة وثبط ERK5 يمتلكان تأثيرًا إضافيًا وقويًا: يمكنهما تأخير شكل من أشكال موت الخلايا الذي تدفعه الحديد ويتسبب في تمزق الأغشية، دون أن يوقفا الضرر الكيميائي الكامن. هذه الحماية خارج الهدف مهمة لسببين. أولاً، تحذر الباحثين من أن النتائج المستقاة باستخدام XMD8-92 وJWG-045 قد لا تعكس بدقة ما يحدث عند حجب ERK5 وحده. ثانيًا، تلمّح إلى وجود آليات يمكن الوصول إليها بالأدوية تدعم إصلاح الغشاء أثناء الإجهاد الشديد، والتي قد تُستغل يومًا ما لحماية الأنسجة السليمة في أمراض يخرج فيها الفيروبتوزيس عن السيطرة. في الوقت الحاضر، تؤكد هذه الدراسة الحاجة إلى إقران مثبطات أحدث وأكثر انتقائية مع أدوات وراثية عند استكشاف بيولوجيا ERK5، ومعاملة الارتباطات بين مستويات الجينات واستجابات الأدوية بحذر بدلاً من افتراض علاقة سبب ونتيجة مباشرة.
الاستشهاد: Zhang, W., Kan, K., Pidd, A.B. et al. XMD8-92 and JWG-045 exhibit anti-ferroptotic activities, independently of inhibiting ERK5. Sci Rep 16, 11337 (2026). https://doi.org/10.1038/s41598-026-42079-w
الكلمات المفتاحية: الفيروبتوزيس, مثبطات ERK5, سرطان الثدي, مسارات وفاة الخلايا, تأثيرات الدواء خارج الهدف