Clear Sky Science · it
XMD8-92 e JWG-045 mostrano attività anti-ferroptotiche, indipendentemente dall’inibire ERK5
Perché proteggere cellule tumorali morenti può comunque insegnarci molto
I ricercatori sul cancro stanno esplorando una sorprendente forma di morte cellulare chiamata ferroptosi, in cui ferro e lipidi danneggiati collaborano per perforare le membrane cellulari. Poiché molti tumori difficili da trattare sono particolarmente vulnerabili a questo processo, i farmaci che inducono la ferroptosi vengono testati come nuovo modo per uccidere le cellule tumorali. Questo studio si è proposto di esaminare se bloccare una proteina che promuove il cancro, ERK5, influenzi la risposta delle cellule del cancro al seno alla ferroptosi. Facendo ciò, i ricercatori hanno scoperto un colpo di scena inatteso: due composti ampiamente usati per bloccare ERK5 proteggono in realtà le cellule tumorali dalla morte ferroptotica attraverso una via completamente diversa.
Come una proteina di segnalazione dello stress incontra una via di morte insolita
ERK5 fa parte di una rete di segnalazione che aiuta le cellule a rispondere a segnali di crescita e a condizioni di stress. I tumori con alta attività di ERK5 spesso crescono più velocemente, si diffondono più facilmente e resistono ad altri farmaci mirati. Un filone di ricerca separato ha mostrato che un enzima protettivo chiamato GPX4, che normalmente rimuove i perossidi dannosi dalle membrane cellulari, è essenziale per prevenire la ferroptosi. Quando GPX4 è bloccata da composti come RSL3, i lipidi della membrana cellulare si ossidano, la membrana si deteriora progressivamente e la cellula muore in modo caratteristico e dipendente dal ferro. Poiché ERK5 può interagire fisicamente con GPX4, gli autori si sono chiesti se questa proteina di segnalazione dello stress potesse rendere le cellule tumorali più o meno sensibili alla ferroptosi.
Farmaci che aiutano e farmaci che non fanno nulla
Il gruppo ha prima analizzato grandi banche dati di linee cellulari tumorali e ha osservato che i tumori con alti livelli di ERK5 tendevano a essere più sensibili ai farmaci che bloccano GPX4, specialmente quando le cellule avevano adottato uno stato più mobile e aggressivo, il cosiddetto stato mesenchimale. Poi sono passati a esperimenti di laboratorio usando diverse linee cellulari di cancro al seno e della cervice. Quando hanno trattato le cellule con RSL3 per indurre la ferroptosi, due composti mirati a ERK5, XMD8-92 e JWG-045, inaspettatamente hanno mantenuto vitali molte cellule. Altri inibitori rivolti alla stessa via di segnalazione—i più recenti bloccanti di ERK5 JWG-071 e BAY-885, e un farmaco che agisce un gradino a monte su MEK5—non hanno offerto questa protezione. In tutti i casi, la molecola standard che blocca la ferroptosi, Ferrostatin-1, si è comportata come previsto, confermando che RSL3 stava effettivamente uccidendo le cellule tramite ferroptosi.
Quando bloccare un bersaglio non è davvero la ragione
Per verificare se questo effetto protettivo coinvolgesse davvero ERK5, i ricercatori hanno ridotto o eliminato completamente ERK5 in diverse linee cellulari tumorali usando strumenti genetici, tra cui RNA a forcina corta (shRNA) e editing genico CRISPR. Se ERK5 fosse stato essenziale per l’azione anti-ferroptotica di questi farmaci, allora eliminare ERK5 avrebbe dovuto abolire la protezione. Invece, XMD8-92 e JWG-045 hanno continuato a salvare le cellule dalla morte indotta da RSL3 anche quando ERK5 era appena rilevabile o completamente assente. Al contrario, JWG-071 e BAY-885 non hanno comunque mostrato alcun effetto. Il gruppo ha anche escluso un noto off-target, la proteina associata alla cromatina BRD4, perché inibitori separati di BRD4 non hanno imitato il comportamento che blocca la ferroptosi. Nel complesso, questi risultati indicano un’attività off-target precedentemente non riconosciuta, unica per XMD8-92 e JWG-045.
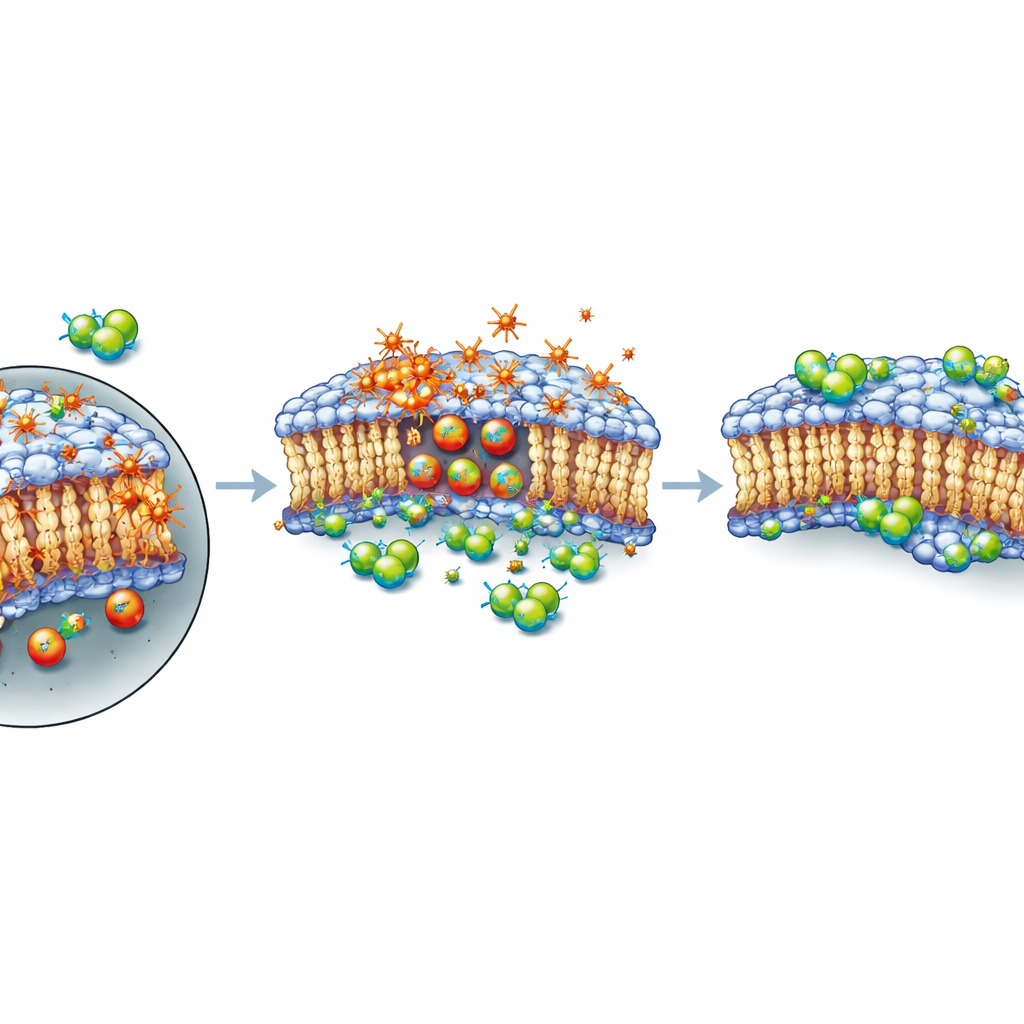
Uno scudo per la pelle esterna della cellula, non un freno al danno
Successivamente gli autori hanno indagato come questi composti intervenissero nel processo di morte. Monitorando l’attività genica per diverse ore dopo il trattamento con XMD8-92, hanno osservato solo spostamenti modesti nei geni noti correlati alla ferroptosi e nessun cambiamento chiaro e coordinato nella segnalazione complessiva della ferroptosi. Usando un colorante fluorescente che si accende sui lipidi ossidati, hanno mostrato che XMD8-92 non fermava la perossidazione lipidica; se non altro, l’ossidazione aumentava quando le cellule ricevevano sia RSL3 sia XMD8-92. Eppure le cellule sopravvivevano meglio. In esperimenti temporizzati con cura, una breve esposizione a RSL3 da sola era sufficiente a segnare il destino delle cellule, anche dopo che il farmaco era stato rimosso. Ma se XMD8-92 veniva aggiunto dopo quella breve pulsazione, molte cellule si riprendevano. Questo schema suggerisce che il composto non impedisca il danno chimico iniziale; invece sembrerebbe aiutare a mantenere o riparare la membrana plasmatica, almeno temporaneamente, permettendo alle cellule di resistere a un periodo di intenso stress ossidativo prima di soccombere eventualmente se il danno continua ad accumularsi.
Cosa significa per la ricerca sul cancro e la progettazione dei farmaci
Per i non specialisti, il messaggio principale è che non tutti i farmaci si comportano come suggerisce la loro etichetta. Due molecole ampiamente usate per studiare e inibire ERK5 si sono dimostrate avere un effetto aggiuntivo e potente: possono ritardare una forma di morte cellulare guidata dal ferro e caratterizzata dalla rottura della membrana senza realmente fermare il danno chimico sottostante. Questa protezione off-target è importante per due ragioni. Primo, mette in guardia i ricercatori che i risultati ottenuti con XMD8-92 e JWG-045 potrebbero non riflettere in modo affidabile cosa accade quando ERK5 è bloccato da solo. Secondo, suggerisce l’esistenza di meccanismi accessibili ai farmaci che rafforzano la riparazione della membrana durante stress estremo, i quali potrebbero un giorno essere sfruttati per proteggere i tessuti sani in malattie in cui la ferroptosi è fuori controllo. Per ora, il lavoro sottolinea la necessità di abbinare inibitori più nuovi e selettivi con strumenti genetici quando si esplora la biologia di ERK5, e di trattare le correlazioni tra livelli genici e risposte ai farmaci con cautela, invece di assumere una relazione di causa diretta.
Citazione: Zhang, W., Kan, K., Pidd, A.B. et al. XMD8-92 and JWG-045 exhibit anti-ferroptotic activities, independently of inhibiting ERK5. Sci Rep 16, 11337 (2026). https://doi.org/10.1038/s41598-026-42079-w
Parole chiave: ferroptosi, inibitori di ERK5, cancro al seno, vie di morte cellulare, effetti off-target dei farmaci