Clear Sky Science · sv
En förbättrad metod för att upptäcka diabetisk retinopati med optimerad djupinlärning
Varför det är viktigt att upptäcka ögonskador tidigt
Diabetes kan tyst skada de små blodkärlen längst bak i ögat och i slutändan leda till suddig syn eller till och med blindhet. Ögonläkare kan upptäcka detta tillstånd—kallat diabetisk retinopati—genom att granska detaljerade fotografier av näthinnan. Men med miljontals människor i riskzonen och för få specialister hinner många patienter aldrig genomgå screening i tid. Denna studie undersöker hur ett noggrant utformat artificiellt intelligenssystem kan läsa näthinnebilder mer exakt och pålitligt, och därigenom hjälpa till att upptäcka problem tidigt nog för att rädda synen.
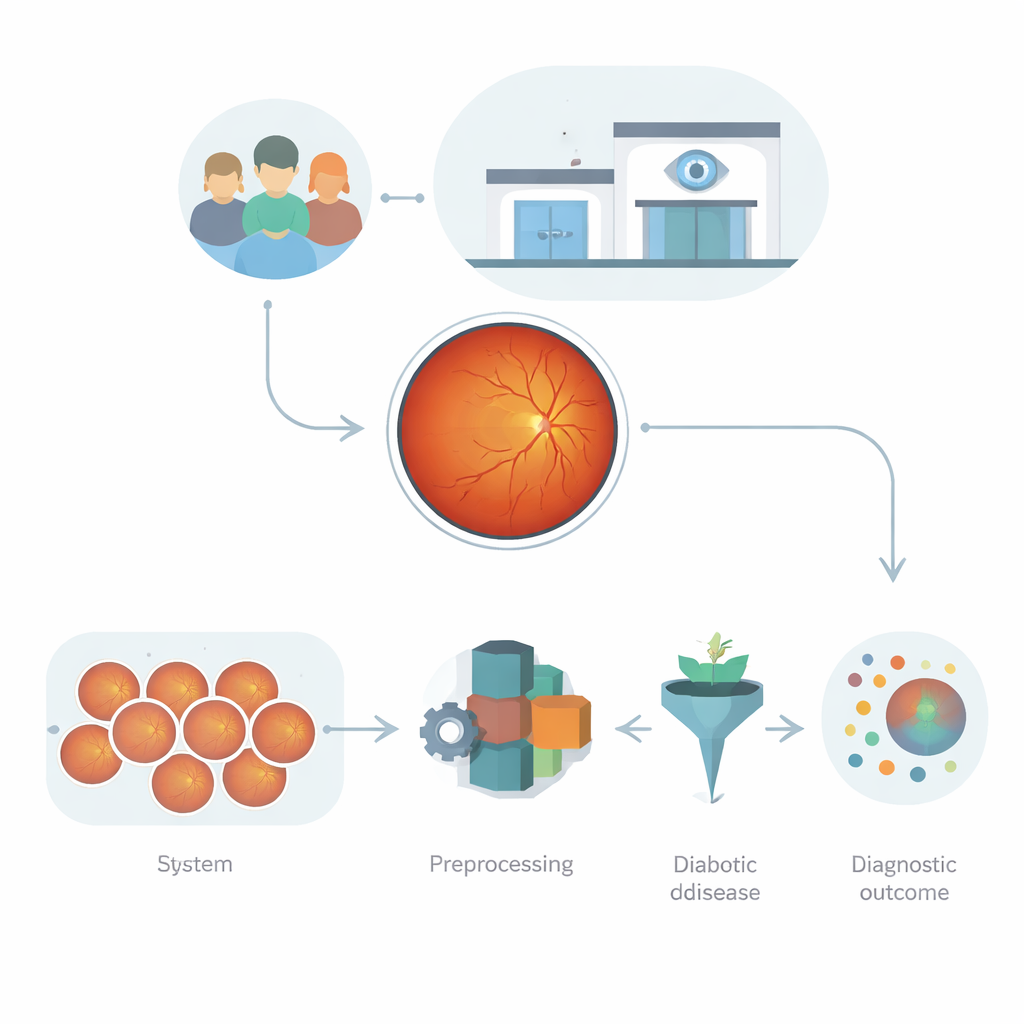
Ögonbilder som en dataguldgruva
Näthinnefotografier, så kallade fundus-bilder, är mycket mer än enkla snapshots. De fångar hur ljus absorberas, reflekteras och sprids i ögats lager och visar blodkärl, små läckor och ärr. Dessa mönster är rika på ledtrådar om diabetiska skador, men de är också komplexa: bilder varierar i ljusstyrka, skärpa, kameratyp och patientbakgrund. Tidigare datorprogram förlitade sig antingen på handgjorda mätningar som missar subtila förändringar, eller på djupinlärningsnätverk som kan vara kraftfulla men benägna att överanpassa sig, särskilt när bildkvalitet eller kliniska förhållanden skiljer sig. Utmaningen är att bygga ett automatiserat system som kan lära från dessa röriga, högdimensionella data utan att bli sprött eller oförutsägbart.
Att lära ett neuralt nätverk att se viktiga varningstecken
Författarna använder först en modern djupinlärningsmodell, EfficientNet‑B0, som en högkvalificerad ”funktionsutdragare” för varje näthinnebild. Istället för att låta läkare manuellt markera varje blödning eller fettansamling lär sig nätverket abstrakta visuella mönster som konsekvent förekommer i sjuka respektive friska ögon. För att göra systemet mer robust rengörs och standardiseras alla bilder: de skalas om, konverteras till gråskala för att fokusera på struktur istället för färg, och förbättras för att skärpa små fläckar och kärldetaljer. Gråskalebilderna omformas sedan till ett format som det förtränade nätverket kan hantera, och nätverkets sista lager finjusteras försiktigt så att dess interna filter reagerar starkt på näthinnestrukturer istället för vardagliga objekt.
Att låta en virtuell svärm välja de mest talande ledtrådarna
Även efter djupinlärning representeras varje bild av mer än tusen numeriska funktioner, många av dem redundanta. Att mata in alla dessa i en klassificerare saktar ner inlärningen och kan sudda ut skillnaderna mellan sjukdomsstadier. För att tackla detta använder teamet en naturinspirerad optimizer modellerad efter gräshoppers rörelser. I deras dynamiska gräshoppsoptimeringsalgoritm representerar varje ”gräshoppa” en annan delmängd av funktioner. Under många iterationer utforskar svärmen kombinationer, styrd av en balans mellan att ströva vida och att fokusera på lovande regioner. Avgörande är att styrparametrarna ändras över tid, vilket förhindrar att svärmen fastnar för tidigt. Resultatet är en mycket mindre uppsättning höginformativa funktioner—runt hundra istället för 1 280—som fortfarande kodar viktiga tecken såsom kluster av mikroaneurysm, områden med exsudat eller mönster av kärlsvullnad.
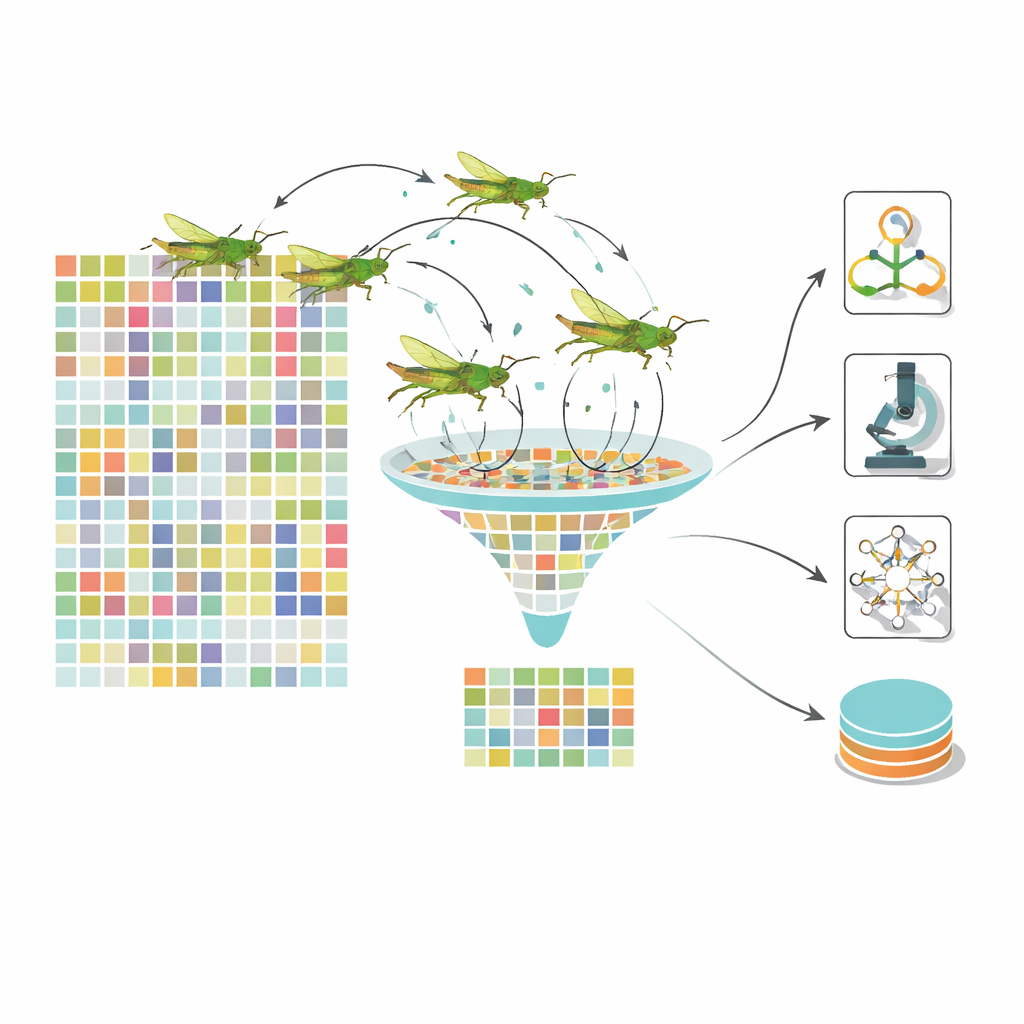
Många enkla åsikter ger en starkare diagnos
I stället för att lita på en enda modell använder systemet ett staplat ensemble av flera olika klassificerare. En supportvektormaskin, ett bayesianskt nätverk och ett beslutsträd får var och en den optimerade funktionsmängden och levererar en egen sannolikhet för att ett öga tillhör ett visst sjukdomsstadium. Dessa ”åsikter” kombineras sedan av en snabb gradientförstärkningsmetod kallad LightGBM, som lär sig hur man viktar varje basmodell beroende på situation. Denna flerskiktade design minskar risken att en enskild modells blindfläckar dominerar. Författarna testar sitt ramverk på stora publika dataset med näthinnebilder, inklusive de välkända EyePACS- och APTOS-samlingarna, och jämför det med ledande djupinlärningspipelines och andra bioinspirerade optimerare.
Hur väl systemet presterar i realistiska tester
Genom experimenten slår det dynamiska gräshopps–ensembleramverket konsekvent konkurrerande metoder. På nyckelbenchmarker når det omkring 94–95 % noggrannhet, ett högt F1‑värde (som balanserar missade fall och falska larm) och ett area under ROC‑kurvan på 0,96, vilket indikerar tydlig separation mellan friska och sjuka ögon. Det generaliserar också väl över olika tränings–testuppdelningar och ytterligare dataset, och bibehåller större delen av sin prestanda när bilder görs artificiellt brusigare eller förvrängda—förhållanden avsedda att efterlikna verklig klinisk variation. Däremot tenderar tidigare svärmalgoritmer med fasta inställningar att konvergera för snabbt, behålla fler redundanta funktioner och ge lägre känslighet och specificitet, särskilt på utmanande eller obalanserade data.
Vad detta betyder för patienter och kliniker
På vardagligt språk visar studien att kombinationen av ett modernt bildanalysnätverk med en smart funktionsurvals-svärm och ett team av enkla klassificerare kan producera en snabb, noggrann och relativt robust ”andra läsare” för diabetiska ögonsjukdomar. Ett sådant verktyg kommer inte att ersätta ögonläkare, men det kan hjälpa till att flagga riskpatienter tidigare, särskilt i upptagna eller underresurserade kliniker där specialister saknas. Författarna konstaterar att vidare validering på lokala sjukhusdata och fortsatt arbete med att minska beräkningskostnader fortfarande behövs, men deras fysikmedvetna, optimeringsdrivna angreppssätt för flyttar automatiserad screening närmare trovärdig, verklighetsnära användning.
Citering: Darwish, S.M., Milad, K.G. & Ibrahim, R.E.ED. An enhanced diabetic retinopathy detection approach using optimized deep learning technique. Sci Rep 16, 9825 (2026). https://doi.org/10.1038/s41598-026-41998-y
Nyckelord: diabetisk retinopati, retinal bildgivning, djupinlärning, urval av funktioner, medicinsk AI