Clear Sky Science · es
Un enfoque mejorado para la detección de la retinopatía diabética mediante una técnica de aprendizaje profundo optimizada
Por qué importa detectar el daño ocular de forma temprana
La diabetes puede dañar silenciosamente los pequeños vasos sanguíneos en la parte posterior del ojo, acabando en visión borrosa o incluso ceguera. Los oftalmólogos pueden detectar esta afección—llamada retinopatía diabética—examinando fotografías detalladas de la retina. Pero con millones de personas en riesgo y pocos especialistas, muchos pacientes no son examinados a tiempo. Este estudio explora cómo un sistema de inteligencia artificial cuidadosamente diseñado puede leer fotos retinianas con mayor precisión y fiabilidad, ayudando a detectar problemas lo suficientemente pronto como para salvar la vista.
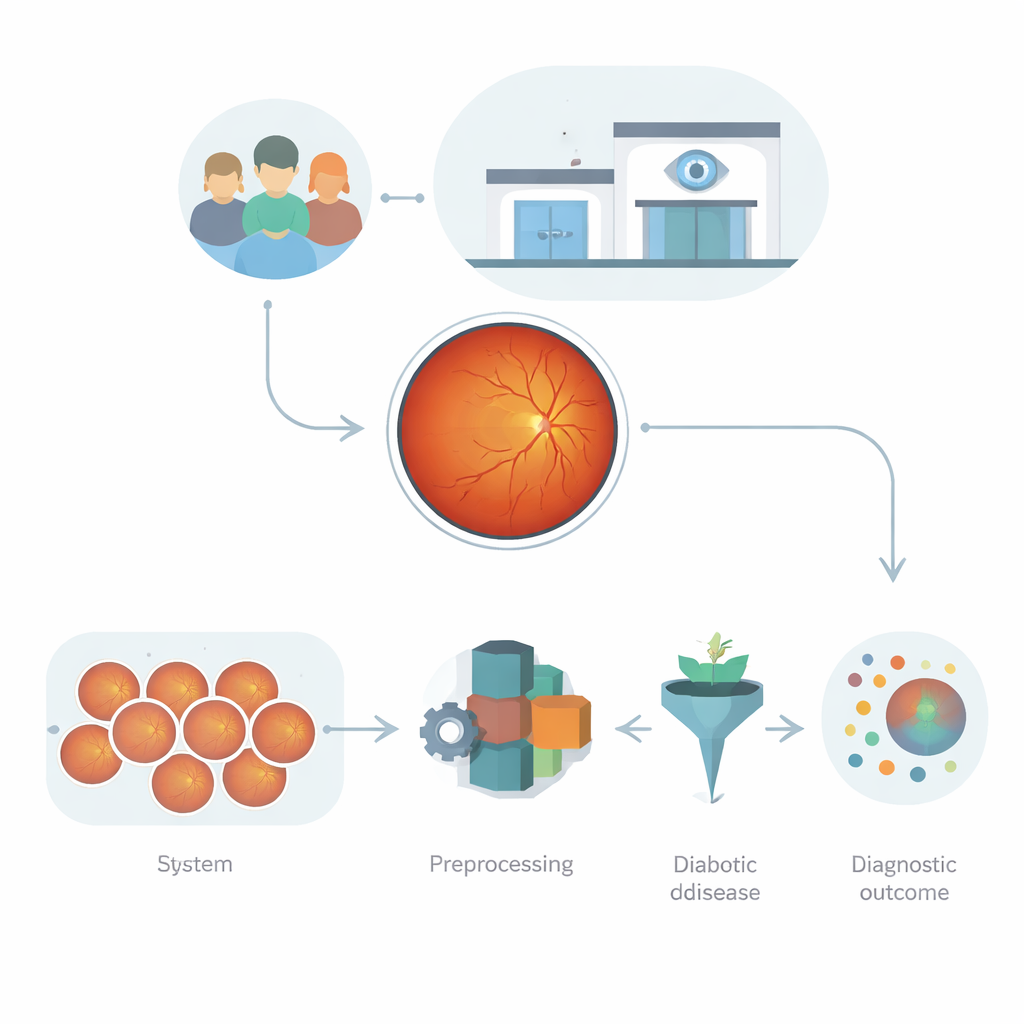
Las imágenes del ojo como mina de datos
Las fotografías retinianas, conocidas como imágenes de fondo de ojo, son mucho más que instantáneas simples. Captan cómo la luz se absorbe, refleja y dispersa en las capas del ojo, revelando vasos sanguíneos, pequeñas filtraciones y cicatrices. Estos patrones están llenos de pistas sobre el daño diabético, pero también son complejos: las imágenes varían en brillo, enfoque, tipo de cámara y el contexto del paciente. Los programas anteriores o bien dependían de mediciones diseñadas a mano, que no capturan cambios sutiles, o de redes de aprendizaje profundo que pueden ser potentes pero propensas al sobreajuste, especialmente cuando la calidad de imagen o el entorno clínico difieren. El reto es construir un sistema automatizado que aprenda de estos datos desordenados y de alta dimensionalidad sin volverse frágil o impredecible.
Enseñar a una red neuronal a ver las señales de aviso clave
Los autores usan primero un modelo moderno de aprendizaje profundo, EfficientNet‑B0, para actuar como un “extractor de características” altamente entrenado para cada imagen retiniana. En lugar de hacer que los médicos marquen manualmente cada hemorragia o depósito graso, la red aprende patrones visuales abstractos que aparecen de manera consistente en ojos enfermos frente a sanos. Para que el sistema sea más robusto, todas las imágenes se limpian y estandarizan: se redimensionan, se convierten a escala de grises para centrarse en la estructura en lugar del color, y se mejoran para afinar pequeños puntos y detalles de los vasos. Las imágenes en escala de grises se convierten luego a un formato que la red preentrenada puede manejar, y las capas finales de la red se ajustan suavemente para que sus filtros internos respondan con fuerza a estructuras retinianas en lugar de a objetos cotidianos.
Permitir que un enjambre virtual elija las pistas más reveladoras
Incluso después del aprendizaje profundo, cada imagen se representa mediante más de mil características numéricas, muchas de ellas redundantes. Alimentar todas estas a un clasificador ralentiza el aprendizaje y puede difuminar la distinción entre estadios de la enfermedad. Para abordar esto, el equipo recurre a un optimizador inspirado en la naturaleza modelado según el movimiento de las saltamontes. En su algoritmo dinámico de optimización por saltamontes, cada “saltamontes” representa un subconjunto distinto de características. A lo largo de muchas iteraciones, el enjambre explora combinaciones, guiado por un equilibrio entre vagar ampliamente y converger hacia regiones prometedoras. De forma crucial, los parámetros de control cambian con el tiempo, evitando que el enjambre se atasque demasiado pronto. El resultado es un conjunto mucho más pequeño de características altamente informativas—alrededor de cien en lugar de 1.280—que aún codifican signos importantes como agrupaciones de microaneurismas, parches de exudados o patrones de hinchazón vascular.
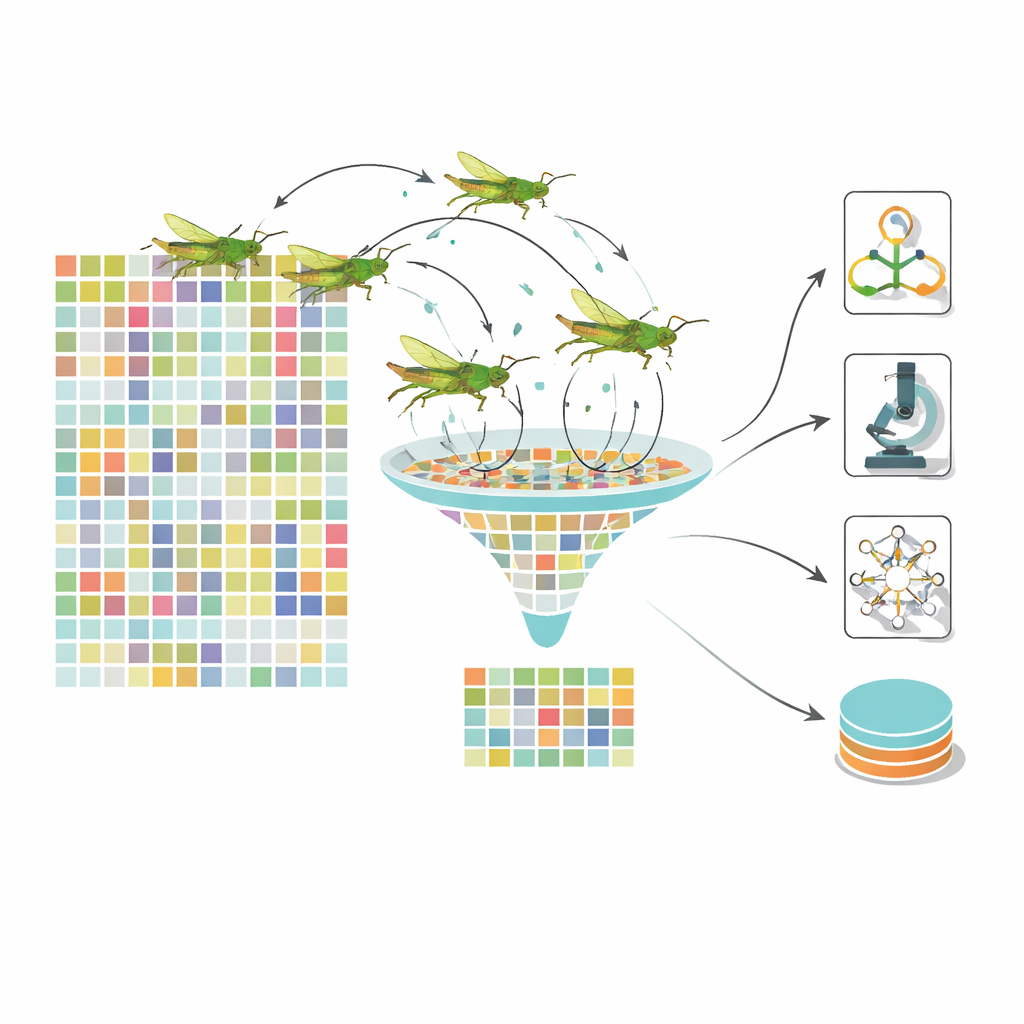
Muchas opiniones simples producen un diagnóstico más sólido
En lugar de confiar en un solo modelo, el sistema utiliza un ensamblado apilado de varios clasificadores diferentes. Una máquina de vectores de soporte, una red bayesiana y un árbol de decisión reciben el conjunto de características optimizado y emiten cada uno su propia probabilidad de que un ojo pertenezca a un determinado estadio de la enfermedad. Estas “opiniones” se combinan luego mediante un método rápido de boosting por gradiente llamado LightGBM, que aprende a ponderar cada modelo base según la situación. Este diseño en capas reduce la probabilidad de que los puntos ciegos de un único modelo dominen. Los autores prueban su marco en grandes conjuntos de datos públicos de imágenes retinianas, incluidas las colecciones ampliamente usadas EyePACS y APTOS, y lo comparan con las principales canalizaciones de aprendizaje profundo y otros optimizadores inspirados en la biología.
Qué tan bien funciona el sistema en pruebas similares al mundo real
En los experimentos, el marco dinámico de saltamontes y ensamblado supera de forma consistente a los métodos competidores. En puntos de referencia clave alcanza aproximadamente un 94–95 % de precisión, una alta puntuación F1 (que equilibra casos perdidos y falsas alarmas) y un área bajo la curva ROC de 0,96, lo que indica una fuerte separación entre ojos sanos y enfermos. También generaliza bien a través de distintas particiones de entrenamiento‑prueba y conjuntos de datos adicionales, y mantiene la mayor parte de su rendimiento cuando las imágenes se vuelven artificialmente más ruidosas o distorsionadas—condiciones pensadas para imitar la variabilidad en clínicas reales. En contraste, los algoritmos de enjambre anteriores con ajustes fijos tienden a converger demasiado pronto, conservar más características redundantes y ofrecer menor sensibilidad y especificidad, especialmente en datos desafiantes o desbalanceados.
Qué significa esto para pacientes y clínicas
En términos cotidianos, el estudio muestra que combinar una red moderna de análisis de imágenes con un enjambre inteligente de selección de características y un equipo de clasificadores sencillos puede producir un “segundo lector” rápido, preciso y comparativamente robusto para la enfermedad ocular diabética. Esta herramienta no reemplazará a los oftalmólogos, pero puede ayudar a señalar a los pacientes en riesgo más pronto, especialmente en clínicas saturadas o con pocos recursos donde los especialistas escasean. Los autores señalan que aún son necesarias validaciones adicionales con datos de hospitales locales y trabajo continuo para reducir el coste computacional, pero su enfoque consciente de la física y guiado por optimización acerca el cribado automatizado a un despliegue de confianza en el mundo real.
Cita: Darwish, S.M., Milad, K.G. & Ibrahim, R.E.ED. An enhanced diabetic retinopathy detection approach using optimized deep learning technique. Sci Rep 16, 9825 (2026). https://doi.org/10.1038/s41598-026-41998-y
Palabras clave: retinopatía diabética, imagenología retinal, aprendizaje profundo, selección de características, IA médica