Clear Sky Science · pl
Udoskonalone podejście do wykrywania retinopatii cukrzycowej z wykorzystaniem zoptymalizowanej techniki głębokiego uczenia
Dlaczego wczesne wykrycie uszkodzeń oka ma znaczenie
Cukrzyca może po cichu uszkadzać drobne naczynia krwionośne z tyłu oka, co ostatecznie prowadzi do zamazanego widzenia lub nawet ślepoty. Okuliści mogą wykryć ten stan — nazywany retinopatią cukrzycową — poprzez badanie szczegółowych zdjęć siatkówki. Jednak przy milionach osób zagrożonych i zbyt małej liczbie specjalistów wielu pacjentów nigdy nie zostaje przebadanych wystarczająco wcześnie. W badaniu tym analizuje się, jak starannie zaprojektowany system sztucznej inteligencji może czytać zdjęcia siatkówki dokładniej i bardziej niezawodnie, pomagając wykrywać problemy na tyle wcześnie, by ocalić wzrok.
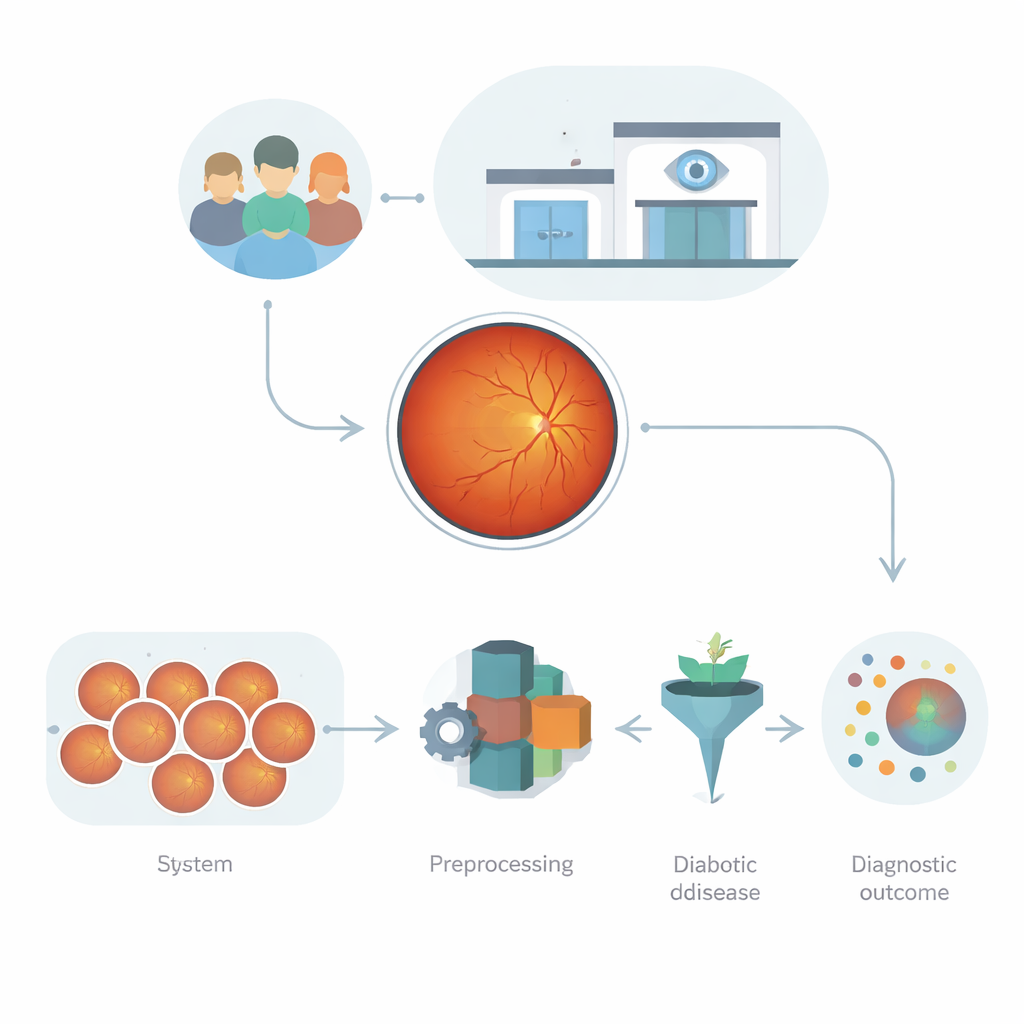
Zdjęcia oka jako kopalnia danych
Fotografie siatkówki, znane jako zdjęcia dna oka, to o wiele więcej niż zwykłe fotografie. Rejestrują, jak światło jest absorbowane, odbijane i rozpraszane przez warstwy oka, ujawniając naczynia krwionośne, drobne wycieki i blizny. Te wzorce są bogate w wskazówki dotyczące uszkodzeń cukrzycowych, ale są też złożone: obrazy różnią się jasnością, ostrością, typem aparatu i tłem pacjenta. Wcześniejsze programy komputerowe albo polegały na ręcznie opracowanych miarach, które pomijają subtelne zmiany, albo na sieciach głębokiego uczenia, które mogą być potężne, lecz podatne na przeuczenie, zwłaszcza gdy jakość obrazów lub warunki kliniczne się zmieniają. Wyzwanie polega na zbudowaniu zautomatyzowanego systemu, który potrafi uczyć się z tych chaotycznych, wysokowymiarowych danych, nie stając się kruchy ani nieprzewidywalny.
Nauczanie sieci neuronowej rozpoznawania kluczowych oznak
Autorzy najpierw wykorzystują nowoczesny model głębokiego uczenia, EfficientNet‑B0, jako wysoko wyszkolony „ekstraktor cech” dla każdego zdjęcia siatkówki. Zamiast każdorazowo prosić lekarzy o ręczne zaznaczanie krwotoków czy złogów tłuszczu, sieć uczy się abstrakcyjnych wzorców wizualnych, które konsekwentnie pojawiają się w oczach chorych i zdrowych. Aby zwiększyć odporność systemu, wszystkie obrazy są oczyszczane i standaryzowane: zmieniane jest ich rozmiar, konwertowane na skalę szarości, by skupić się na strukturze zamiast koloru, oraz wzmacniane, by wyostrzyć drobne plamki i szczegóły naczyń. Obrazy w skali szarości są następnie przekształcane do formatu, który obsłuży wstępnie wytrenowana sieć, a końcowe warstwy sieci są delikatnie dostrajane, tak aby jej wewnętrzne filtry silniej reagowały na struktury siatkówki zamiast na codzienne obiekty.
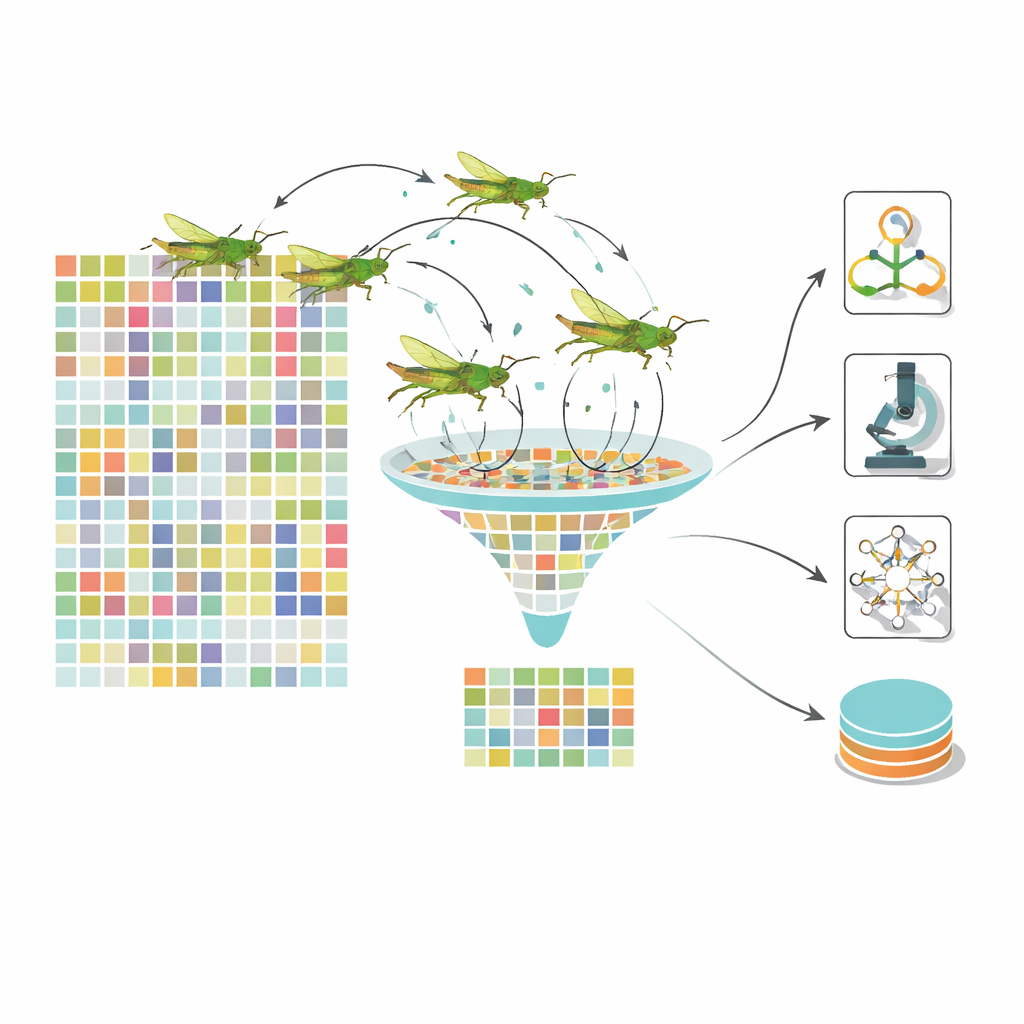
Puszczenie wirtualnego roju, by wybrał najbardziej wymowne wskazówki
Nawet po etapie głębokiego uczenia każde zdjęcie jest reprezentowane przez ponad tysiąc cech numerycznych, z których wiele jest redundantnych. Podawanie ich wszystkich klasyfikatorowi spowalnia uczenie i może rozmywać rozróżnienie między stadami choroby. Aby temu zaradzić, zespół sięga po optymalizator inspirowany naturą, wzorowany na ruchu pasikoników. W ich dynamicznym algorytmie optymalizacji pasikoników każdy „pasikonik” reprezentuje inny podzbiór cech. W wielu iteracjach rój bada kombinacje, kierując się balansem między szerokim eksplorowaniem a zawężaniem obiecujących obszarów. Kluczowe jest to, że parametry sterujące zmieniają się w czasie, co zapobiega zbyt wczesnemu ugrzęźnięciu roju. W rezultacie otrzymuje się znacznie mniejszy zestaw wysoce informatywnych cech — około stu zamiast 1 280 — które nadal kodują ważne oznaki, takie jak skupiska mikroaneuryzmów, plamy wysięków czy wzory obrzęku naczyń.
Wiele prostych opinii daje silniejszą diagnozę
Zamiast polegać na pojedynczym modelu, system wykorzystuje składowy zestaw (stacked ensemble) kilku różnych klasyfikatorów. Maszyna wektorów nośnych (SVM), sieć bayesowska i drzewo decyzyjne każdy otrzymują zoptymalizowany zestaw cech i generują własne prawdopodobieństwo przypisania oka do danego stadium choroby. Te „opnie” są następnie łączone przez szybki algorytm boostingowy zwany LightGBM, który uczy się, jak ważyć każdy model bazowy w zależności od sytuacji. Taka wielowarstwowa konstrukcja zmniejsza ryzyko, że luki jednego modelu zdominują wynik. Autorzy testują swoje rozwiązanie na dużych publicznych zbiorach zdjęć siatkówki, w tym szeroko używanych kolekcjach EyePACS i APTOS, i porównują je z czołowymi potokami głębokiego uczenia oraz innymi optymalizatorami inspirowanymi biologicznie.
Jak system radzi sobie w testach przypominających rzeczywistość
W eksperymentach ramy oparte na dynamicznym roju pasikoników i ensemble konsekwentnie przewyższają metody konkurencyjne. Na kluczowych benchmarkach osiągają około 94–95% dokładności, wysoki wynik F1 (równoważący przypadki przeoczone i fałszywe alarmy) oraz pole pod krzywą ROC rzędu 0,96, co wskazuje na silne rozdzielenie między oczami zdrowymi a chorymi. System dobrze uogólnia na różne podziały trening‑test i dodatkowe zbiory danych, a także zachowuje większość swojej wydajności, gdy obrazy są sztucznie zaszumione lub zniekształcone — warunki mające naśladować zmienność w rzeczywistej klinice. Dla porównania wcześniejsze algorytmy rojowe o stałych ustawieniach skłaniają się ku zbyt wczesnej konwergencji, utrzymują więcej cech redundantnych i dają niższą czułość oraz specyficzność, szczególnie na trudnych lub niezrównoważonych danych.
Co to oznacza dla pacjentów i placówek
Mówiąc prosto, badanie pokazuje, że połączenie nowoczesnej sieci analizy obrazu ze sprytnym rojowym wyborem cech i zespołem prostych klasyfikatorów może dać szybkie, dokładne i stosunkowo odporne „drugie oko” w wykrywaniu chorób siatkówki związanych z cukrzycą. Takie narzędzie nie zastąpi okulistów, ale może pomóc wcześniej wskazać pacjentów zagrożonych, zwłaszcza w zatłoczonych lub słabo wyposażonych placówkach, gdzie brakuje specjalistów. Autorzy zaznaczają, że nadal potrzebna jest dalsza walidacja na danych lokalnych szpitali oraz prace nad redukcją kosztu obliczeniowego, ale ich podejście uwzględniające fizykę obrazowania i optymalizację przybliża automatyczne przesiewy do zaufanego wdrożenia w rzeczywistych warunkach.
Cytowanie: Darwish, S.M., Milad, K.G. & Ibrahim, R.E.ED. An enhanced diabetic retinopathy detection approach using optimized deep learning technique. Sci Rep 16, 9825 (2026). https://doi.org/10.1038/s41598-026-41998-y
Słowa kluczowe: retinopatia cukrzycowa, obrazowanie siatkówki, głębokie uczenie, selekcja cech, medyczna sztuczna inteligencja