Clear Sky Science · ru
Улучшенный метод обнаружения диабетической ретинопатии с применением оптимизированных методов глубокого обучения
Почему важно обнаруживать повреждения глаза на ранней стадии
Диабет может незаметно повреждать мельчайшие кровеносные сосуды в задней части глаза, в конечном счёте приводя к затуманиванию зрения или даже слепоте. Офтальмологи могут выявить это состояние — называемое диабетической ретинопатией — при изучении детальных фотографий сетчатки. Но при миллионах людей в группе риска и недостатке специалистов многие пациенты не проходят своевременный скрининг. В этом исследовании изучается, как тщательно спроектированная система искусственного интеллекта может читать снимки сетчатки более точно и надёжно, помогая выявлять проблемы достаточно рано, чтобы сохранить зрение.
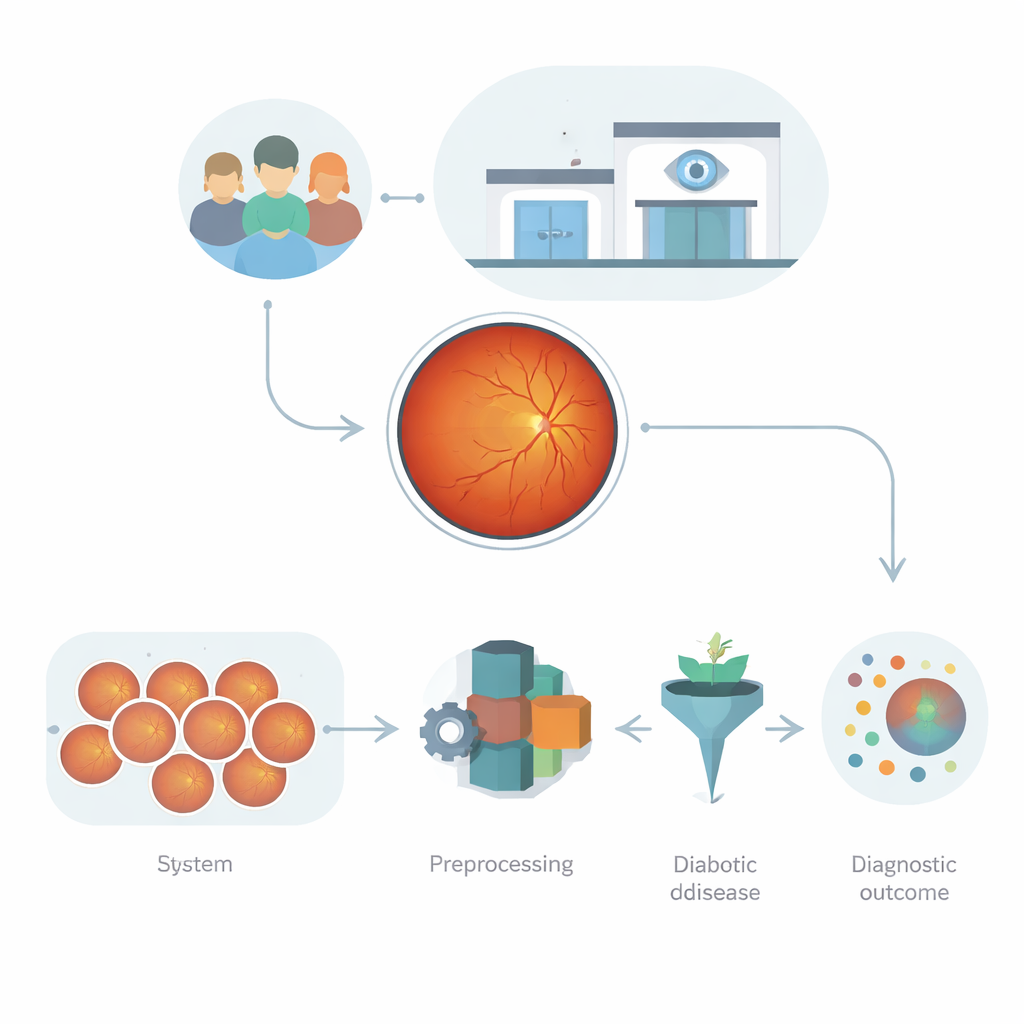
Фотографии глаза как источник данных
Фотографии сетчатки, известные как фундус‑изображения, — это куда больше, чем простые снимки. Они фиксируют, как свет поглощается, отражается и рассеивается слоями глаза, показывая сосуды, микропроникновения и рубцы. Эти паттерны содержат множество подсказок о диабетическом повреждении, но они также сложны: изображения различаются по яркости, резкости, типу камеры и фону пациента. Ранние компьютерные решения опирались либо на вручную разработанные измерения, которые не улавливают тонкие изменения, либо на нейросети глубокого обучения, которые мощны, но склонны к переобучению, особенно когда качество изображений или клинические условия отличаются. Задача состоит в том, чтобы построить автоматизированную систему, способную учиться на этих шумных, высокоразмерных данных, не становясь хрупкой или непредсказуемой.
Обучение нейросети распознавать ключевые признаки
Авторы сначала используют современную модель глубокого обучения EfficientNet‑B0 в роли высококлассного «извлекателя признаков» для каждого снимка сетчатки. Вместо того чтобы заставлять врачей вручную отмечать каждое кровоизлияние или жировое отложение, сеть изучает абстрактные визуальные паттерны, которые последовательно встречаются в больных и здоровых глазах. Чтобы повысить устойчивость системы, все изображения очищаются и стандартизуются: их изменяют по размеру, переводят в оттенки серого, чтобы сосредоточиться на структуре, а не на цвете, и улучшают, чтобы подчеркнуть мелкие пятна и детали сосудов. Затем изображения в оттенках серого преобразуют в формат, с которым справится предобученная сеть, и последние слои сети аккуратно дообучают, чтобы внутренние фильтры сильнее реагировали на структуры сетчатки, а не на бытовые объекты.
Позволить виртуальному рою выбрать самые информативные признаки
Даже после глубокого обучения каждое изображение представлено более чем тысячей числовых признаков, многие из которых избыточны. Подавать всё это в классификатор замедляет обучение и может размывать границы между стадиями болезни. Чтобы решить эту проблему, команда обращается к оптимизатору, вдохновлённому природой и моделирующему движение саранчи. В их динамическом алгоритме оптимизации саранчи каждая «саранча» представляет собой разный поднабор признаков. На протяжении многих итераций рой исследует комбинации, балансируя между широким поиском и сосредоточением на перспективных областях. Важно, что управляющие параметры меняются со временем, не давая рою преждевременно застрять. В результате получается значительно меньший набор высокоинформативных признаков — примерно сто вместо 1 280 — которые при этом кодируют важные признаки, такие как скопления микроаневризм, участки экссудатов или узоры расширения сосудов.
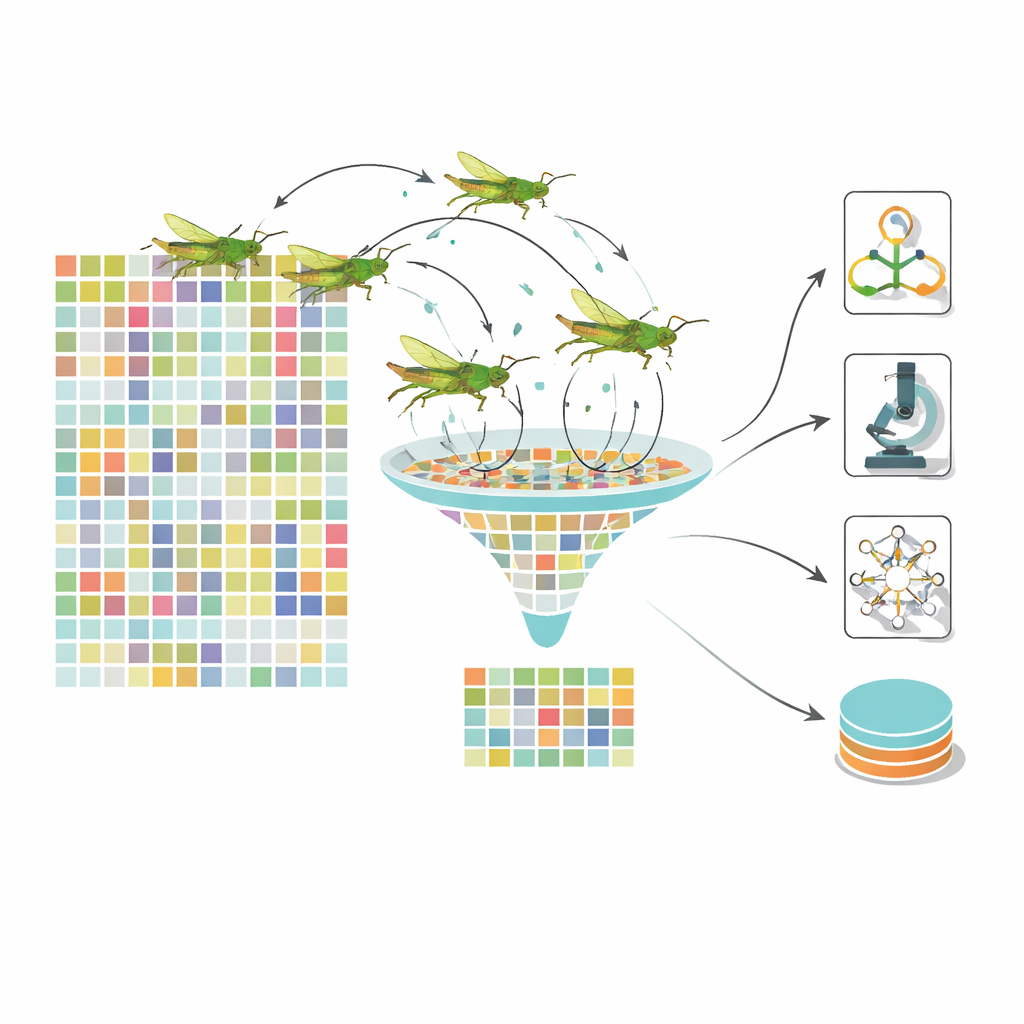
Множество простых мнений дают более точный диагноз
Вместо того чтобы полагаться на одну модель, система использует составной ансамбль из нескольких разных классификаторов. Метод опорных векторов, байесовская сеть и решающее дерево получают оптимизированный набор признаков и выдают собственную вероятность принадлежности глаза к той или иной стадии болезни. Эти «мнения» затем комбинирует быстрый градиентный бустинг LightGBM, который учится взвешивать каждый базовый классификатор в зависимости от ситуации. Такая многослойная архитектура снижает вероятность того, что слепые зоны одной модели будут доминировать. Авторы тестируют свою систему на крупных общедоступных наборах данных снимков сетчатки, включая широко используемые коллекции EyePACS и APTOS, и сравнивают её с передовыми конвейерами глубокого обучения и другими био‑вдохновлёнными оптимизаторами.
Насколько хорошо система работает в приближённых к реальности тестах
В экспериментах динамический рой‑ансамбль последовательно превосходит конкурирующие методы. По ключевым метрикам он достигает примерно 94–95% точности, высокого F1‑score (баланс пропущенных случаев и ложных тревог) и площади под ROC‑кривой около 0,96, что указывает на чёткое разделение здоровых и поражённых глаз. Система также хорошо обобщает результаты на разных разбиениях на обучающую и тестовую выборки и на дополнительных наборах данных, причём сохраняет большую часть производительности, когда изображения искусственно зашумлены или искажены — условия, имитирующие клиническую вариативность. Для сравнения, ранние алгоритмы роя с фиксированными настройками склонны к преждевременной сходимости, сохраняют больше избыточных признаков и показывают более низкую чувствительность и специфичность, особенно на сложных или несбалансированных данных.
Что это значит для пациентов и клиник
Проще говоря, исследование показывает, что сочетание современной сети для анализа изображений с «умным» отбором признаков с помощью роя и набором простых классификаторов может дать быстрый, точный и относительно устойчивый «второй читатель» для диагностики диабетических поражений глаз. Такой инструмент не заменит офтальмологов, но может помочь быстрее отсеять пациентов с риском, особенно в загруженных или плохо оснащённых клиниках, где специалистов мало. Авторы отмечают, что необходима дополнительная валидация на локальных больничных данных и дальнейшая работа по снижению вычислительных затрат, но их подход, учитывающий физику изображения и ориентированный на оптимизацию, приближает автоматизированный скрининг к надёжному применению в реальной клинической практике.
Цитирование: Darwish, S.M., Milad, K.G. & Ibrahim, R.E.ED. An enhanced diabetic retinopathy detection approach using optimized deep learning technique. Sci Rep 16, 9825 (2026). https://doi.org/10.1038/s41598-026-41998-y
Ключевые слова: диабетическая ретинопатия, ретинальная визуализация, глубокое обучение, отбор признаков, медицинский ИИ