Clear Sky Science · nl
Een verbeterde detectiemethode voor diabetische retinopathie met geoptimaliseerde deep‑learningtechniek
Waarom het vroeg ontdekken van oogschade belangrijk is
Diabetes kan geruisloos de kleine bloedvaten aan de achterkant van het oog beschadigen, wat uiteindelijk leidt tot wazig zien of zelfs blindheid. Oogartsen kunnen deze aandoening — diabetische retinopathie genoemd — opsporen door gedetailleerde foto’s van het netvlies te bekijken. Maar met miljoenen mensen die risico lopen en te weinig specialisten, worden veel patiënten niet op tijd gescreend. Deze studie onderzoekt hoe een zorgvuldig ontworpen kunstmatig‑intelligentiesysteem retinafoto’s nauwkeuriger en betrouwbaarder kan lezen, zodat problemen vroeg genoeg worden gedetecteerd om het gezichtsvermogen te redden.
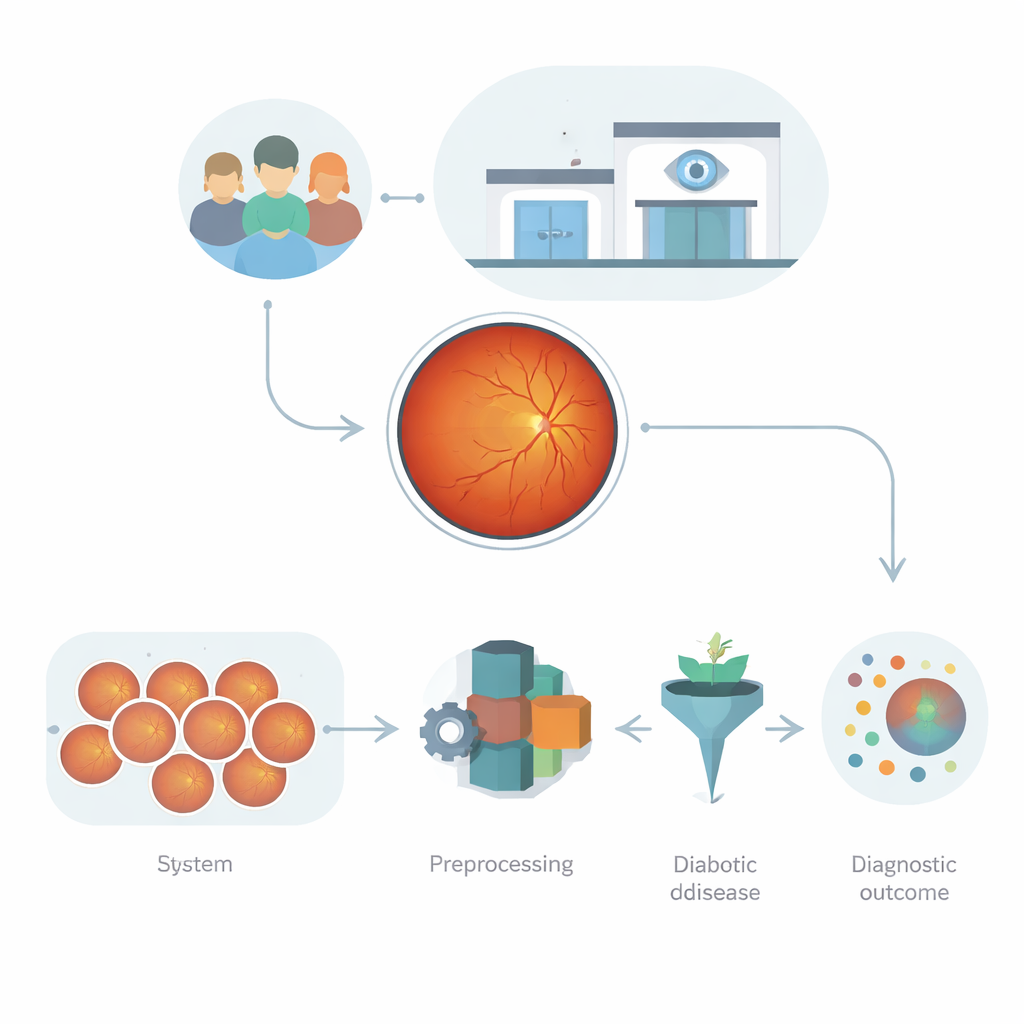
Oogfoto’s als een datagoudmijn
Retina‑foto’s, bekend als fundusbeelden, zijn veel meer dan simpele snapshots. Ze leggen vast hoe licht wordt geabsorbeerd, gereflecteerd en verstrooid door de lagen van het oog, en tonen bloedvaten, kleine lekken en littekens. Deze patronen zitten vol aanwijzingen over diabetische schade, maar ze zijn ook complex: beelden variëren in helderheid, scherpte, cameratype en patiëntachtergrond. Eerdere computerprogramma’s vertrouwden óf op handgemaakte metingen die subtiele veranderingen missen, óf op deep‑learningnetwerken die krachtig kunnen zijn maar vatbaar voor overfitting, zeker wanneer de beeldkwaliteit of klinische omstandigheden verschillen. De uitdaging is een geautomatiseerd systeem te bouwen dat kan leren van deze rommelige, hoog‑dimensionale data zonder kwetsbaar of onvoorspelbaar te worden.
Een neuraal netwerk trainen om sleutelwaarschuwingen te zien
De auteurs gebruiken eerst een modern deep‑learningmodel, EfficientNet‑B0, als een hoogopgeleide “feature‑extractor” voor elk retinabeeld. In plaats van artsen iedere bloeding of vetafzetting handmatig te laten markeren, leert het netwerk abstracte visuele patronen die consequent voorkomen in zieke versus gezonde ogen. Om het systeem robuuster te maken, worden alle beelden opgeschoond en gestandaardiseerd: ze worden van formaat veranderd, naar grijswaarden geconverteerd om te focussen op structuur in plaats van kleur, en geoptimaliseerd om kleine vlekjes en vaatdetails te verscherpen. De grijswaardenbeelden worden vervolgens omgezet naar een formaat dat het vooraf getrainde netwerk kan verwerken, en de laatste lagen van het netwerk worden voorzichtig bijgesteld zodat de interne filters sterker reageren op retinastructuren in plaats van alledaagse objecten.
Een virtuele zwerm laat de meest veelzeggende aanwijzingen kiezen
Zelfs na deep learning wordt elk beeld gerepresenteerd door meer dan duizend numerieke kenmerken, waarvan veel redundante informatie bevatten. Al deze kenmerken in een classifier stoppen vertraagt het leren en kan het onderscheid tussen ziektefasen vervagen. Om dit aan te pakken, gebruikt het team een natuurgeïnspireerde optimizer gebaseerd op de beweging van sprinkhanen. In hun dynamische grasshopper‑optimalisatiealgoritme vertegenwoordigt elke “sprinkhaan” een andere subset van kenmerken. Over veel iteraties verkent de zwerm combinaties, gestuurd door een balans tussen breed rondzwerven en inzoomen op veelbelovende regio’s. Cruciaal is dat de controlegegevens in de loop van de tijd veranderen, waardoor de zwerm niet te vroeg vastloopt. Het resultaat is een veel kleinere set sterk informatieve kenmerken — ongeveer honderd in plaats van 1.280 — die toch belangrijke tekenen coderen zoals clusters van microaneurysmata, vlekken met exsudaten of patronen van vaatzwelling.
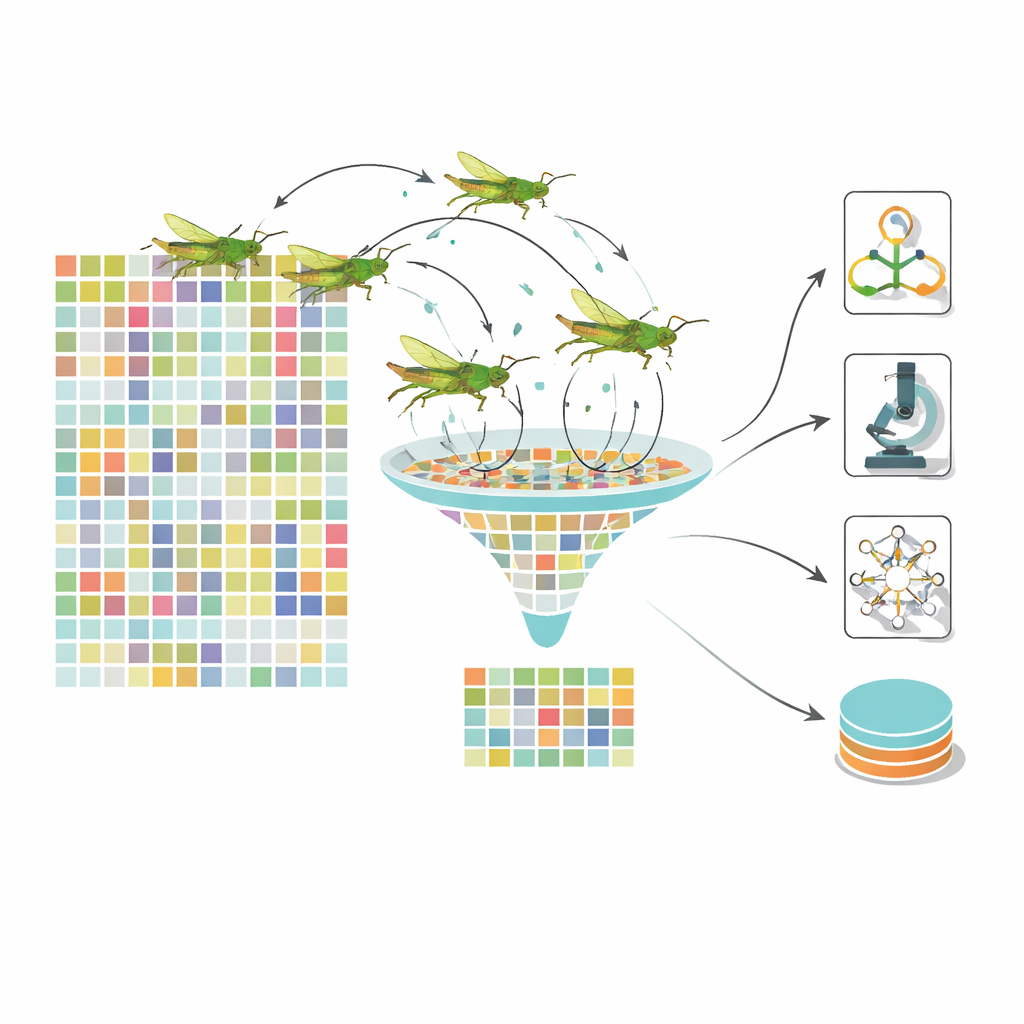
Veelkleurige, eenvoudige meningen leveren een sterkere diagnose
In plaats van op één model te vertrouwen, gebruikt het systeem een gestapeld ensemble van meerdere verschillende classifiers. Een support vector machine, een Bayesiaans netwerk en een beslisboom ontvangen elk de geoptimaliseerde kenmerken en geven hun eigen waarschijnlijkheid dat een oog in een bepaalde ziektefase valt. Deze “meningen” worden vervolgens gecombineerd door een snelle gradient‑boostingmethode genaamd LightGBM, die leert hoe elk basismodel gewogen moet worden afhankelijk van de situatie. Dit gelaagde ontwerp verkleint de kans dat de blinde vlekken van één model domineren. De auteurs testen hun raamwerk op grote openbare datasets met retinabeelden, waaronder de veelgebruikte EyePACS‑ en APTOS‑collecties, en vergelijken het met toonaangevende deep‑learningpipelines en andere bio‑geïnspireerde optimalisatoren.
Hoe goed het systeem presteert in realistische tests
In de experimenten overtreft het dynamische grasshopper‑ensemble consequent concurrerende methoden. Op belangrijke benchmarks bereikt het ongeveer 94–95% nauwkeurigheid, een hoge F1‑score (die gemiste gevallen en valse alarmen in balans brengt) en een area under the ROC‑curve van 0,96, wat wijst op een sterke scheiding tussen gezonde en zieke ogen. Het generaliseert ook goed over verschillende train–test‑splits en aanvullende datasets, en behoudt het grootste deel van zijn prestatie wanneer beelden kunstmatig rumoeriger of vervormd worden — condities die bedoeld zijn om de variabiliteit in echte klinieken na te bootsen. Ter vergelijking: eerdere zwermalgoritmen met vaste instellingen hebben de neiging te vroeg te convergeren, houden meer redundante kenmerken aan en leveren lagere sensitiviteit en specificiteit, vooral bij uitdagende of ongebalanceerde data.
Wat dit betekent voor patiënten en klinieken
In eenvoudige woorden toont de studie aan dat het combineren van een modern beeldanalyset netwerk met een slimme kenmerk‑selecterende zwerm en een team van eenvoudige classifiers een snel, nauwkeurig en relatief robuust “tweede lezer” voor diabetische oogaandoeningen kan opleveren. Zo’n hulpmiddel zal oogartsen niet vervangen, maar kan helpen risicopatiënten eerder te signaleren, vooral in drukke of onderbedeelde klinieken waar specialisten schaars zijn. De auteurs merken op dat verdere validatie op lokale ziekenhuisgegevens en voortgezet werk aan het verlagen van rekenkosten nog nodig zijn, maar hun fysica‑bewuste, optimalisatiegestuurde aanpak brengt geautomatiseerde screening dichter bij betrouwbare, real‑world inzetbaarheid.
Bronvermelding: Darwish, S.M., Milad, K.G. & Ibrahim, R.E.ED. An enhanced diabetic retinopathy detection approach using optimized deep learning technique. Sci Rep 16, 9825 (2026). https://doi.org/10.1038/s41598-026-41998-y
Trefwoorden: diabetische retinopathie, retina‑beeldvorming, deep learning, kenmerkselectie, medische AI