Clear Sky Science · sv
Ökad uttryckning av IL-32γ i endotelceller främjar rekrytering av makrofager och inflammatorisk progress i ateroskleros
Varför denna forskning är viktig för hjärthälsan
Ateroskleros — igentäppning och förhårdnad av artärerna — är den underliggande orsaken till de flesta hjärtinfarkter och stroke. Vi vet att kolesterol, särskilt i sin skadade form, och kronisk inflammation driver sjukdomen, men hur dessa två krafter kommunicerar inom blodkärlen håller man fortfarande på att utröna. Denna studie fokuserar på en relativt okänd inflammatorisk budbärare kallad IL‑32γ och visar hur den hjälper till att förvandla stressade kärlbeklädnadsceller till kraftfulla magnetiska och förstärkande signaler för skadliga immunceller, vilket potentiellt öppnar en ny väg för att dämpa artärinflammation vid dess källa.
En närmare titt på igentäppta artärer
Artärerna är beklädda av ett tunt lager endotelceller som normalt bildar en jämn, skyddande barriär mellan blodet och kärlväggen. När nivåerna av "det onda" kolesterolet är höga smiter vissa av dessa partiklar under detta lager och blir oxiderade — kemiskt skadade varianter kända som Ox‑LDL. Detta oxiderade kolesterol irriterar endotelcellerna, gör dem läckiga och klibbiga och lockar till sig immunceller som kallas monocyter, vilka omvandlas till makrofager som slukar fett. Med tiden bygger dessa fettfyllda celler, tillsammans med ärrvävnad, upp plack som plötsligt kan brista och blockera blodflödet till hjärtat eller hjärnan. 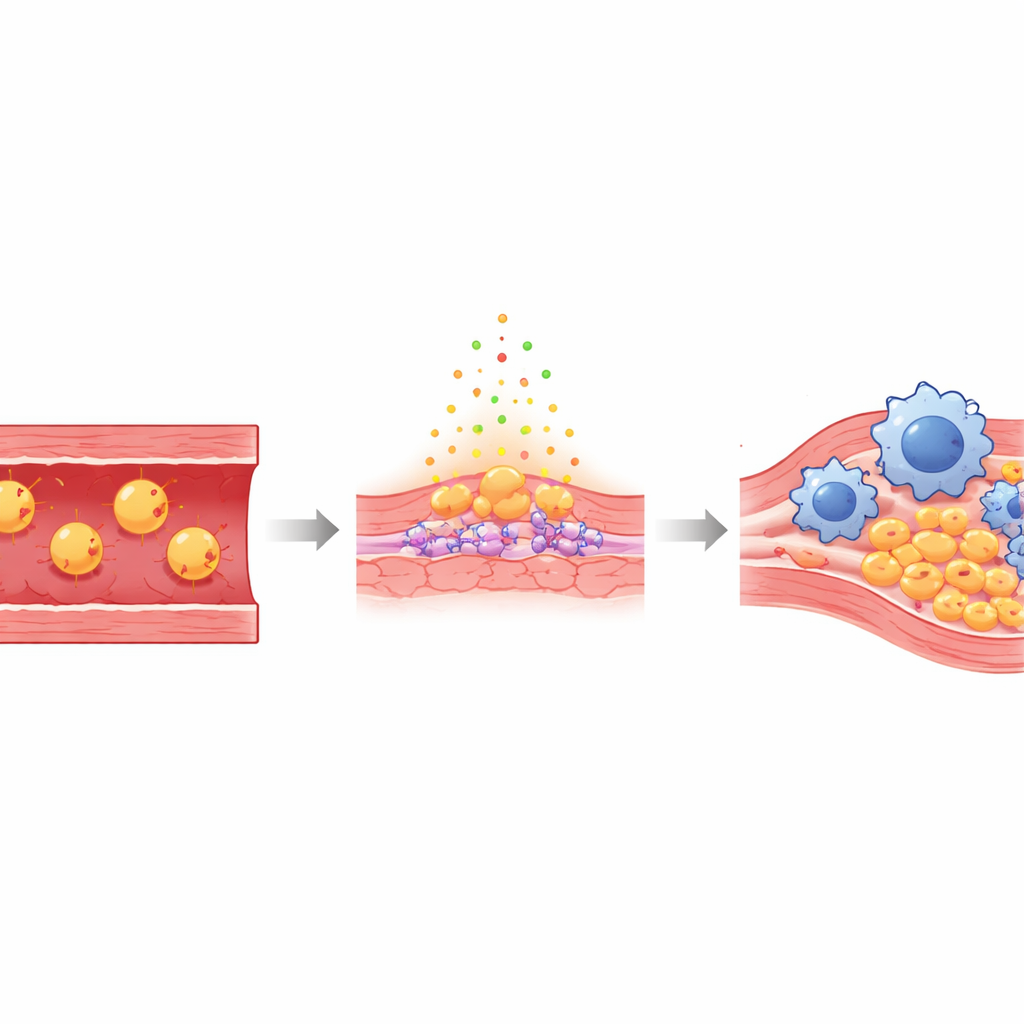
Den inflammatoriska budbäraren i mitten
Forskarna fokuserade på IL‑32, ett inflammatoriskt protein som finns i flera former, där IL‑32γ anses vara den mest aktiva. De mätte först olika IL‑32‑varianter i blod från personer med ateroskleros och hos friska frivilliga. Endast IL‑32γ var tydligt förhöjt hos patienterna, både på gen- och proteinnivå, vilket antyder att det kan vara särskilt kopplat till kärlsjukdom. Därefter exponerade de mänskliga endotelceller för Ox‑LDL i laboratoriet. Under denna stress ökade cellerna kraftigt produktion och frisättning av IL‑32γ, medan andra IL‑32‑former knappt förändrades. Samtidigt försämrades cellernas förmåga att växa, migrera och bilda nya kärl-liknande strukturer, och de ökade uttrycket av molekyler som hjälper till att fånga förbipasserande immunceller — klassiska tecken på endotelial dysfunktion.
Hur kärlceller driver makrofager mot ett skadligt tillstånd
För att se vad detta betydde för immuncellernas beteende samodlade teamet Ox‑LDL‑behandlade endotelceller med makrofager i ett Transwell-system som låter cellerna kommunicera via lösliga signaler. Makrofager exponerade för stressade endotelceller skiftade mot ett starkt proinflammatoriskt "M1"‑mönster: de visade ytmarkörer för ett angreppsaktigt tillstånd, producerade mer inflammatoriska ämnen som TNF‑α och IL‑1β, och migrerade lättare mot endotelplanet. När forskarna blockerade en nyckelomkopplare inne i endotelcellerna, NF‑κB‑vägen, dämpade de både IL‑32γ‑frisättning och detta M1‑skifte. Neutralisering av IL‑32γ i sig gav en liknande effekt, med minskade inflammatoriska markörer och begränsad makrofagmigration, vilket pekar på IL‑32γ som en central mellanhand.
Inzoomning på signalvägen
Forskarna frågade sedan om IL‑32γ kunde verka direkt på makrofager och via vilken bana. Tillsats av renat IL‑32γ till makrofager, utan några endotelceller närvarande, var tillräckligt för att driva dem mot M1‑tillståndet och öka deras rörelseförmåga. Detta svar var beroende av en annan molekylär kaskad inne i cellerna, p38 MAPK‑vägen: när ett p38‑blockerande läkemedel tillsattes slutade IL‑32γ att öka inflammatoriska gener, cytokinfrisättning eller migration. 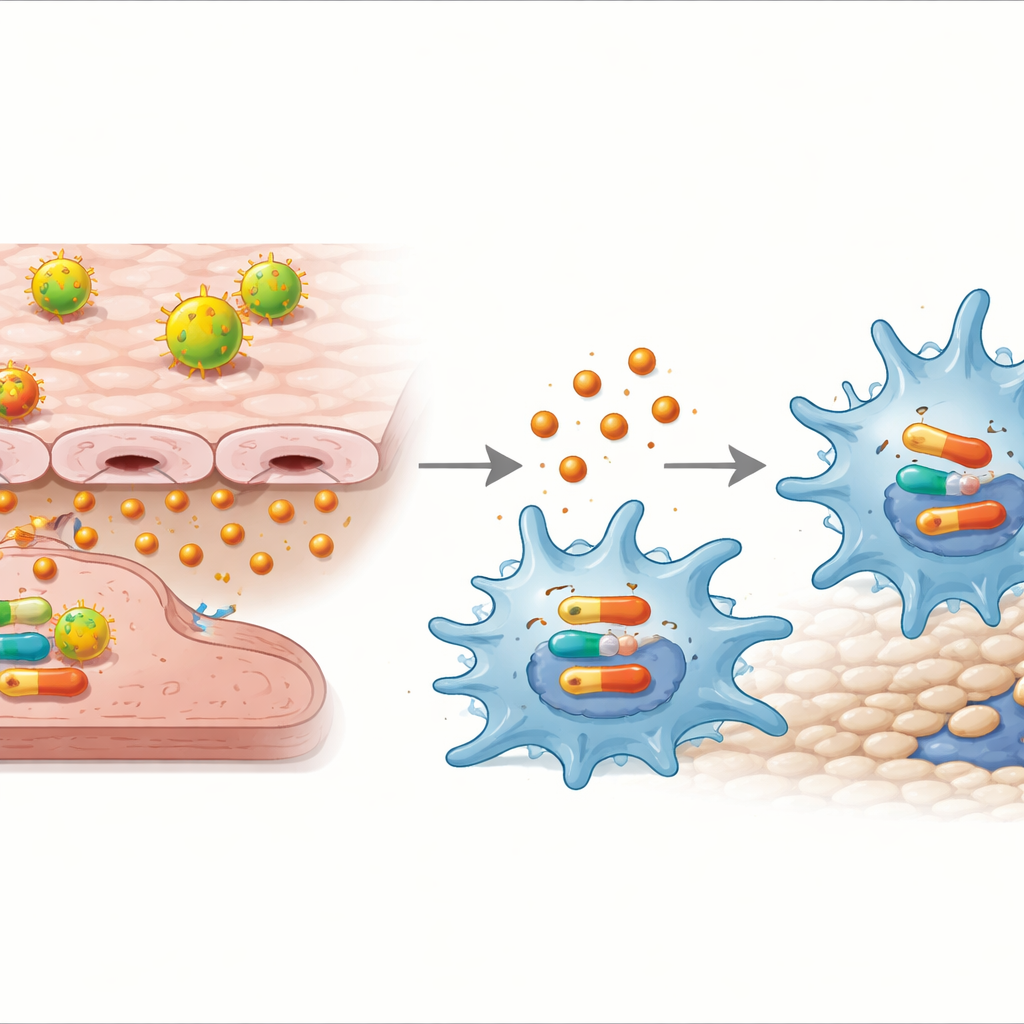
Vad som händer i levande artärer
Slutligen testade teamet banan i möss genetiskt benägna att utveckla ateroskleros och som gavs en västerländsk fettrik diet. Möss som injicerades med IL‑32γ utvecklade större artärplack, visade mer makrofagansamling i dessa plack och hade högre blodnivåer av inflammatoriska molekyler — trots liknande kolesterolnivåer jämfört med kontroller. När p38‑vägen blockerades i dessa djur sjönk plackstorlek, makrofagackumulering och inflammation tillbaka mot baslinjen. Detta innebär att IL‑32γ kan påskynda placktillväxt i levande artärer främst genom att öka inflammatorisk signalering, inte genom att förändra blodlipider.
Vad allt detta betyder för framtida behandlingar
Tillsammans skisserar arbetet en händelsekedja: oxiderat kolesterol irriterar kärlets beklädnad, dessa celler svarar genom att frisätta IL‑32γ, och IL‑32γ i sin tur driver närliggande makrofager in i ett aggressivt, plackfrämjande läge via p38‑signalering. Genom att identifiera IL‑32γ som en nyckellänk mellan skadade endotelceller och överaktiva immunceller pekar studien på en ny terapeutisk ansats: istället för att enbart sänka kolesterol kan framtida läkemedel också rikta in sig på IL‑32γ eller dess p38‑väg för att dämpa inflammation inne i artärväggarna och bromsa, eller möjligen vända, aterosklerosens utveckling.
Citering: Yang, Z., Liu, M., Shi, Y. et al. Upregulation of IL-32γ in endothelial cells promotes macrophage recruitment and inflammatory progression in atherosclerosis. Sci Rep 16, 11262 (2026). https://doi.org/10.1038/s41598-026-40151-z
Nyckelord: ateroskleros, endotelceller, makrofagpolarisering, inflammation, IL-32 gamma