Clear Sky Science · fr
Suralimentation en IL-32γ dans les cellules endothéliales favorise le recrutement des macrophages et la progression inflammatoire de l’athérosclérose
Pourquoi cette recherche compte pour la santé cardiaque
L’athérosclérose — l’obstruction et le durcissement des artères — est la cause principale de la plupart des infarctus et des AVC. Nous savons que le cholestérol, en particulier sous ses formes oxydées, et l’inflammation chronique favorisent cette maladie, mais la manière dont ces deux facteurs communiquent au sein des vaisseaux sanguins reste à élucider. Cette étude se concentre sur un messager inflammatoire peu connu, l’IL‑32γ, et montre comment il transforme des cellules endothéliales stressées en véritables aimants et amplificateurs pour des cellules immunitaires nocives, ouvrant potentiellement une nouvelle voie pour apaiser l’inflammation artérielle à sa source.
Un examen détaillé des artères obstruées
Les artères sont tapissées d’une mince couche de cellules endothéliales qui forment normalement une barrière lisse et protectrice entre le sang et la paroi vasculaire. Lorsque les niveaux de « mauvais » cholestérol sont élevés, certaines particules se glissent sous cet endothélium et s’oxydent — des formes chimiquement altérées appelées Ox‑LDL. Ce cholestérol oxydé irrite les cellules endothéliales, les rendant perméables et adhésives, et attire des cellules immunitaires appelées monocytes, qui se différencient en macrophages capables d’engloutir les lipides. Avec le temps, ces cellules engorgées de graisse, accompagnées de tissu cicatriciel, forment des plaques susceptibles de se rompre brusquement, obstruant le flux sanguin vers le cœur ou le cerveau. 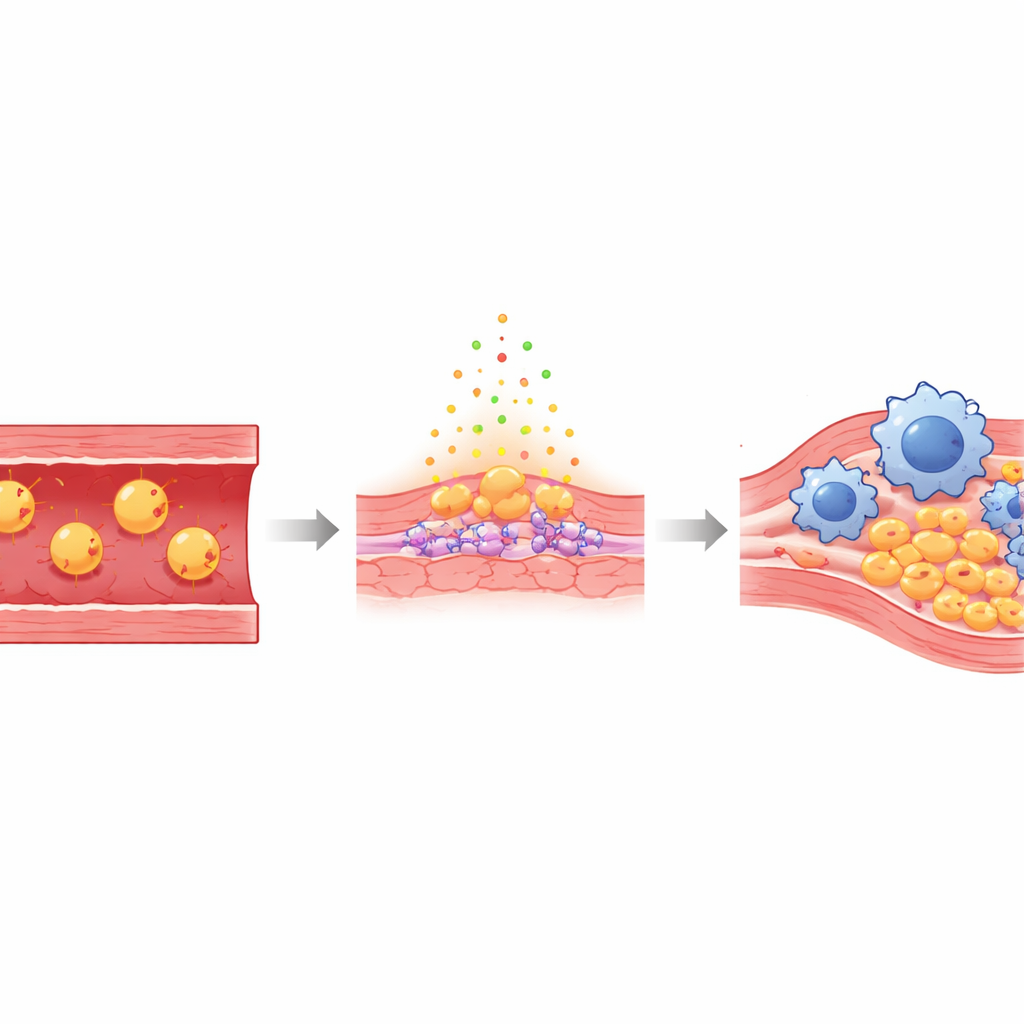
Le messager inflammatoire au centre
Les chercheurs se sont intéressés à l’IL‑32, une protéine inflammatoire qui existe en plusieurs isoformes, l’IL‑32γ étant considérée comme la plus active. Ils ont d’abord mesuré les différents variants d’IL‑32 dans le sang de patients atteints d’athérosclérose et de volontaires sains. Seule l’IL‑32γ était nettement augmentée chez les patients, tant au niveau de l’ARN que de la protéine, ce qui suggère un lien spécifique avec la maladie artérielle. Ils ont ensuite exposé des cellules endothéliales humaines à l’Ox‑LDL en culture. Sous ce stress, les cellules augmentaient fortement la production et la libération d’IL‑32γ, alors que les autres formes d’IL‑32 changeaient peu. Simultanément, ces cellules voyaient leur capacité à proliférer, migrer et former de nouvelles structures vasculaires réduite, et elles amplifiaient l’expression de molécules favorisant l’adhérence des cellules immunitaires circulantes — signes classiques de dysfonction endothéliale.
Comment les cellules vasculaires poussent les macrophages vers un état néfaste
Pour évaluer l’impact sur le comportement immunitaire, l’équipe a co‑cultivé des cellules endothéliales traitées par Ox‑LDL avec des macrophages dans un système Transwell permettant la communication par signaux solubles. Les macrophages exposés à des endothéliums stressés basculaient vers un profil fortement pro‑inflammatoire « M1 » : ils exprimaient des marqueurs de surface associés à un état d’attaque, produisaient davantage de médiateurs inflammatoires comme le TNF‑α et l’IL‑1β, et migraient plus volontiers vers la couche endothéliale. Lorsque les chercheurs ont bloqué un commutateur clé à l’intérieur des cellules endothéliales, la voie NF‑κB, ils ont réduit à la fois la libération d’IL‑32γ et cette polarisation M1. Neutraliser directement l’IL‑32γ produisait un effet similaire, diminuant les marqueurs inflammatoires et limitant la mobilité des macrophages, ce qui désigne l’IL‑32γ comme un intermédiaire central.
Zoom sur la chaîne de signalisation
Les scientifiques ont ensuite vérifié si l’IL‑32γ pouvait agir directement sur les macrophages et par quelle voie. L’ajout d’IL‑32γ purifié aux macrophages, sans cellules endothéliales, suffisait à les orienter vers l’état M1 et à augmenter leur mobilité. Cette réponse dépendait d’un autre relais moléculaire intracellulaire, la voie p38 MAPK : lorsqu’un inhibiteur de p38 était ajouté, l’IL‑32γ n’augmentait plus l’expression des gènes inflammatoires, la libération de cytokines ni la migration. 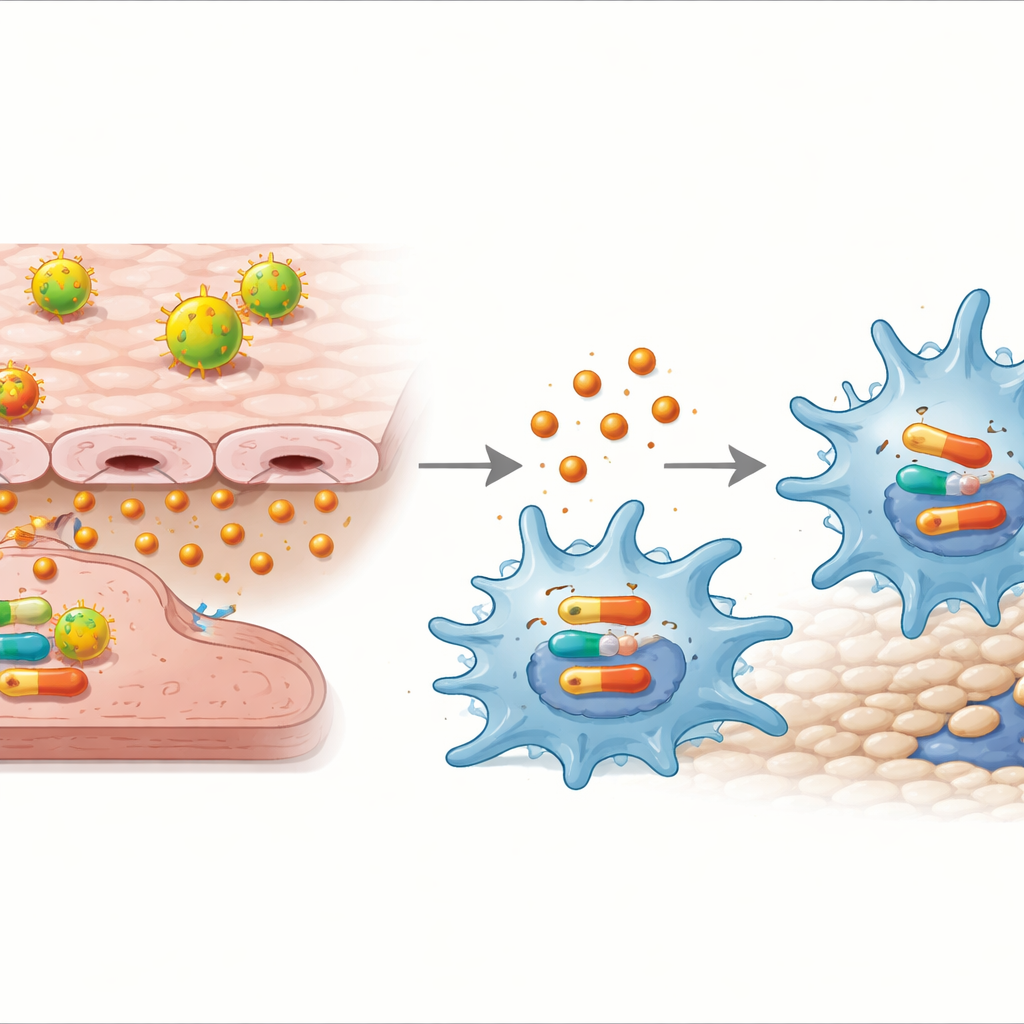
Ce qui se passe dans les artères vivantes
Enfin, l’équipe a testé la voie chez des souris génétiquement prédisposées à l’athérosclérose et alimentées avec un régime riche en graisses de type occidental. Les souris injectées avec de l’IL‑32γ développaient des plaques artérielles plus volumineuses, une accumulation plus importante de macrophages dans ces plaques, et des taux sanguins plus élevés de molécules inflammatoires — malgré des niveaux de cholestérol comparables aux témoins. Lorsque la voie p38 était bloquée chez ces animaux, la taille des plaques, l’accumulation de macrophages et l’inflammation retombaient vers les valeurs de base. Cela indique que l’IL‑32γ peut accélérer la croissance des plaques in vivo principalement en intensifiant la signalisation inflammatoire, et non en modifiant les lipides sanguins.
Ce que cela implique pour les traitements futurs
Dans l’ensemble, ce travail décrit une chaîne d’événements : le cholestérol oxydé irrite l’endothélium, ces cellules répondent en libérant de l’IL‑32γ, et l’IL‑32γ pousse les macrophages voisins vers un mode agressif qui favorise la formation de plaques via la signalisation p38. En identifiant l’IL‑32γ comme un lien clé entre cellules endothéliales lésées et cellules immunitaires hyperactives, l’étude suggère un angle thérapeutique nouveau : au‑delà de simplement abaisser le cholestérol, des médicaments ciblant l’IL‑32γ ou sa voie p38 pourraient atténuer l’inflammation au sein de la paroi artérielle et ralentir, voire inverser, la progression de l’athérosclérose.
Citation: Yang, Z., Liu, M., Shi, Y. et al. Upregulation of IL-32γ in endothelial cells promotes macrophage recruitment and inflammatory progression in atherosclerosis. Sci Rep 16, 11262 (2026). https://doi.org/10.1038/s41598-026-40151-z
Mots-clés: athérosclérose, cellules endothéliales, polarisation des macrophages, inflammation, IL-32 gamma