Clear Sky Science · pl
Nasilenie IL-32γ w komórkach śródbłonka sprzyja rekrutacji makrofagów i postępowi zapalenia w miażdżycy
Dlaczego to badanie ma znaczenie dla zdrowia serca
Miażdżyca — zatkanie i stwardnienie tętnic — jest główną przyczyną większości zawałów serca i udarów. Wiemy, że cholesterol, zwłaszcza w swojej uszkodzonej postaci, oraz przewlekłe zapalenie napędzają tę chorobę, ale sposób, w jaki te dwie siły komunikują się wewnątrz naczyń krwionośnych, nie jest jeszcze w pełni poznany. Badanie to skupia się na mało znanym przekaźniku zapalnym o nazwie IL‑32γ i pokazuje, jak pomaga on przekształcać zestresowane komórki wyściełające naczynia w silne magnesy i wzmacniacze dla szkodliwych komórek układu odpornościowego, co potencjalnie otwiera nowe możliwości łagodzenia zapalenia w ścianie tętnic u jego źródła.
Bliższe spojrzenie na zatkane tętnice
Tętnice wyścieła cienka warstwa komórek śródbłonka, które zwykle tworzą gładką, ochronną barierę między krwią a ścianą naczynia. Gdy poziomy „złego” cholesterolu są wysokie, niektóre cząsteczki przedostają się pod tę warstwę i ulegają utlenieniu — chemicznie uszkodzone formy znane jako Ox‑LDL. Ten utleniony cholesterol podrażnia komórki śródbłonka, czyniąc je nieszczelnymi i bardziej lepkimi, oraz przyciąga komórki odpornościowe zwane monocytami, które przekształcają się w makrofagi pochłaniające tłuszcz. Z czasem te naładowane tłuszczem komórki wraz z tkanką bliznowatą gromadzą się w blaszki, które mogą nagle pęknąć, blokując przepływ krwi do serca lub mózgu. 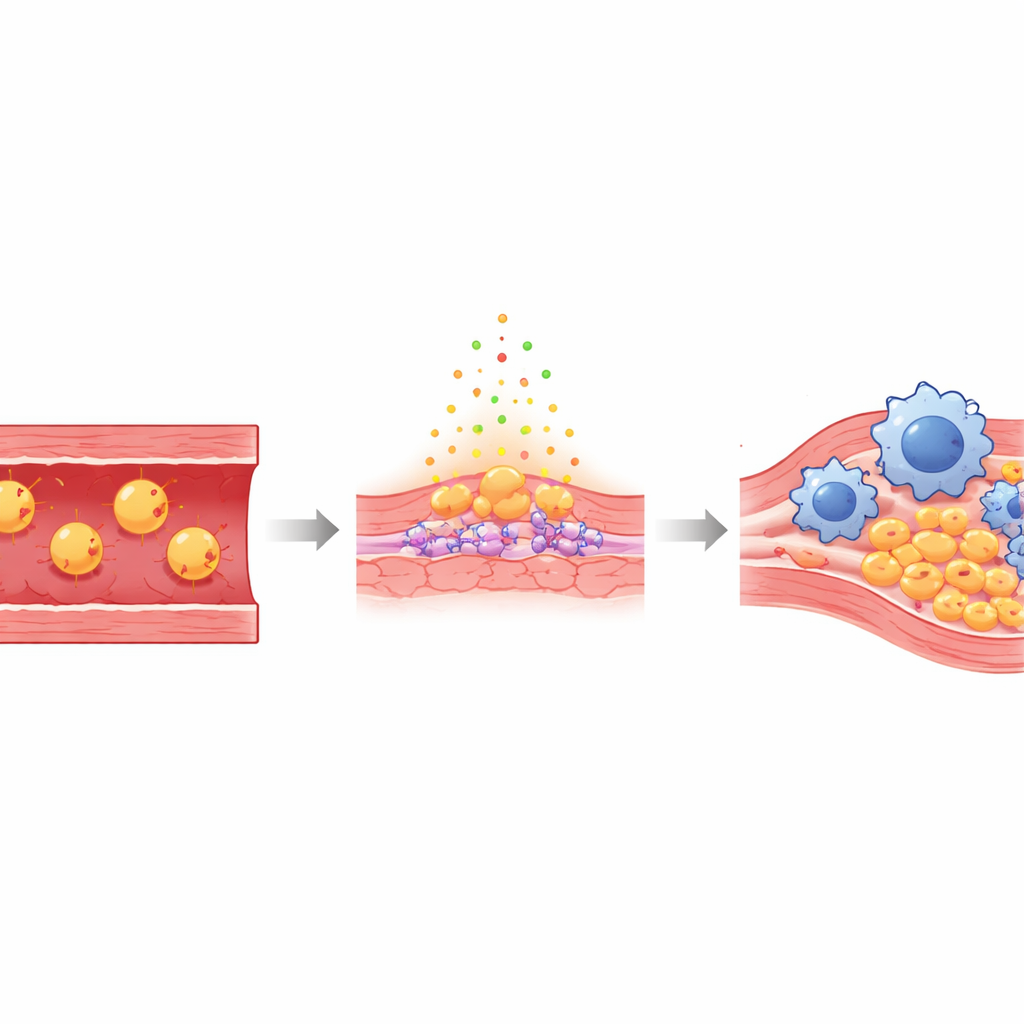
Przekaźnik zapalny pośrodku
Naukowcy skoncentrowali się na IL‑32, białku zapalnym występującym w kilku formach, z IL‑32γ uważanym za najbardziej aktywną odmianę. Najpierw zmierzyli różne warianty IL‑32 we krwi osób z miażdżycą i u zdrowych ochotników. Tylko IL‑32γ była wyraźnie podwyższona u pacjentów, zarówno na poziomie genu, jak i białka, co sugeruje jej szczególne powiązanie z chorobą tętnic. Następnie w warunkach laboratoryjnych poddali ludzkie komórki śródbłonka działaniu Ox‑LDL. Pod tym stresem komórki gwałtownie zwiększyły produkcję i wydzielanie IL‑32γ, podczas gdy inne formy IL‑32 zmieniały się niewiele. Jednocześnie komórki miały mniejszą zdolność do proliferacji, migracji i tworzenia struktur podobnych do naczyń oraz zwiększyły ekspresję cząsteczek ułatwiających przyłączanie się przemieszczających się komórek odpornościowych — klasyczne oznaki dysfunkcji śródbłonka.
Jak komórki naczyniowe skłaniają makrofagi do szkodliwego stanu
Aby sprawdzić, co to oznacza dla zachowania komórek odpornościowych, zespół hodował wspólnie komórki śródbłonka traktowane Ox‑LDL z makrofagami w układzie Transwell, który pozwalał komórkom komunikować się za pomocą sygnałów rozpuszczalnych. Makrofagi eksponowane na zestresowane komórki śródbłonka przesunęły się w stronę silnie prozapalnego fenotypu „M1”: wykazywały markery powierzchniowe związane z trybem ataku, produkowały więcej substancji zapalnych, takich jak TNF‑α i IL‑1β, i bardziej skłonnie migrowały w kierunku warstwy śródbłonka. Gdy badacze zablokowali kluczowy przełącznik w komórkach śródbłonka — szlak NF‑κB — zmniejszyli zarówno wydzielanie IL‑32γ, jak i to przesunięcie w kierunku M1. Zneutralizowanie samego IL‑32γ miało podobny efekt, redukując markery zapalenia i hamując ruchliwość makrofagów, co wskazuje na IL‑32γ jako centralny ogniwowy przekaźnik.
Zbliżenie na łańcuch sygnalizacyjny
Naukowcy zapytali następnie, czy IL‑32γ może działać bezpośrednio na makrofagi i jaką drogą. Dodanie oczyszczonego IL‑32γ do makrofagów, bez obecności komórek śródbłonka, wystarczyło, by przesunąć je w stan M1 i zwiększyć ich migrację. Ta odpowiedź zależała od innej kaskady molekularnej w komórkach — szlaku p38 MAPK: gdy dodano lek blokujący p38, IL‑32γ przestała wzmacniać geny zapalne, uwalnianie cytokin i migrację. 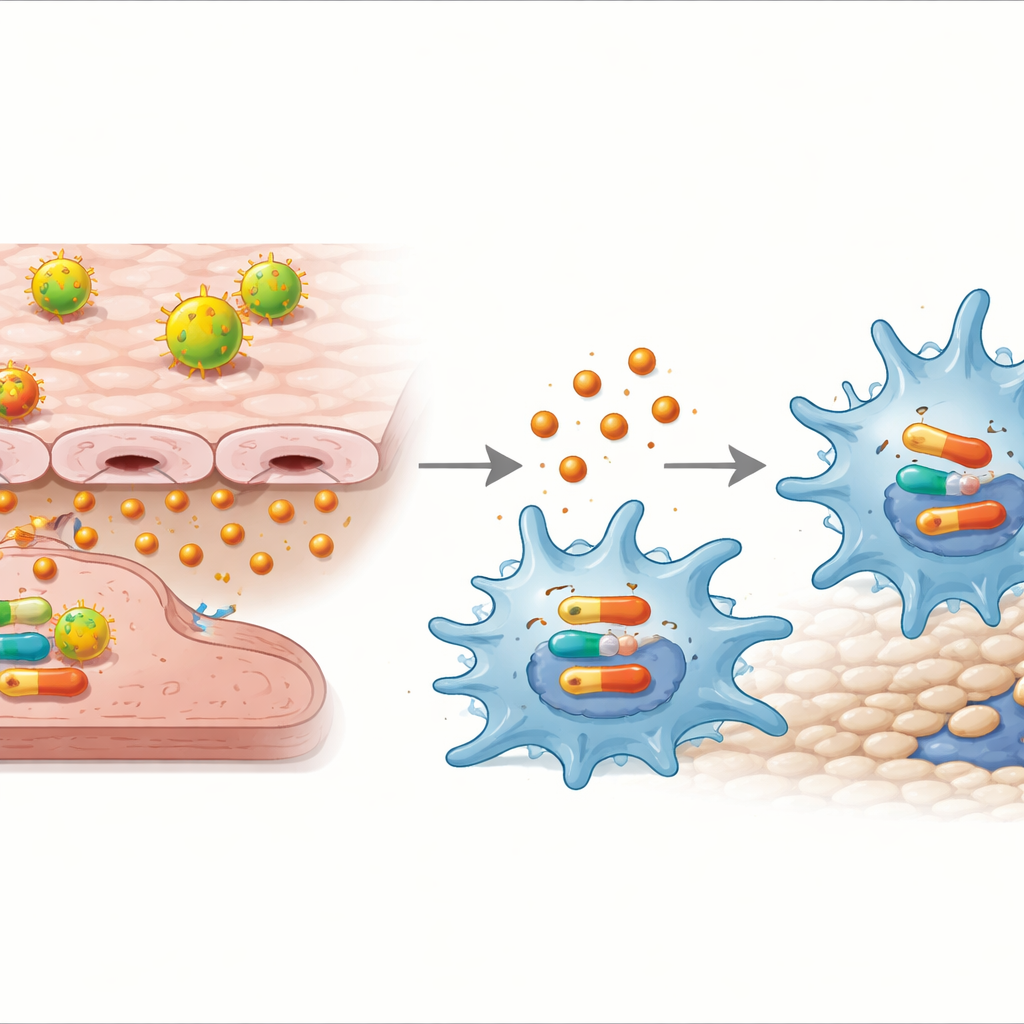
Co dzieje się w żywych tętnicach
Na koniec zespół przetestował ten szlak u myszy genetycznie podatnych na miażdżycę i karmionych dietą wysokotłuszczową w stylu zachodnim. Myszy otrzymujące zastrzyki IL‑32γ wytworzyły większe blaszki miażdżycowe, wykazały większe nagromadzenie makrofagów wewnątrz tych blaszek i miały wyższe poziomy cząsteczek zapalnych we krwi — pomimo podobnych poziomów cholesterolu w porównaniu z grupą kontrolną. Gdy u tych zwierząt zablokowano szlak p38, rozmiar blaszek, akumulacja makrofagów i zapalenie wróciły w kierunku wartości wyjściowych. Oznacza to, że IL‑32γ może przyspieszać wzrost blaszek w żywych tętnicach głównie poprzez zwiększanie sygnalizacji zapalnej, a nie przez zmianę poziomów lipidów we krwi.
Co to wszystko oznacza dla przyszłych terapii
Podsumowując, praca ta przedstawia łańcuch zdarzeń: utleniony cholesterol podrażnia wyściółkę naczyń, komórki te reagują wydzielając IL‑32γ, a IL‑32γ z kolei napędza pobliskie makrofagi do agresywnego, sprzyjającego blaszkom trybu poprzez sygnalizację p38. Identyfikacja IL‑32γ jako kluczowego ogniwa między uszkodzonymi komórkami śródbłonka a nadaktywnością komórek odpornościowych sugeruje nowy kąt terapeutyczny: zamiast jedynie obniżać poziom cholesterolu, przyszłe leki mogłyby również celować w IL‑32γ lub jego szlak p38, aby ostudzić zapalenie wewnątrz ściany tętnic i spowolnić lub potencjalnie odwrócić postęp miażdżycy.
Cytowanie: Yang, Z., Liu, M., Shi, Y. et al. Upregulation of IL-32γ in endothelial cells promotes macrophage recruitment and inflammatory progression in atherosclerosis. Sci Rep 16, 11262 (2026). https://doi.org/10.1038/s41598-026-40151-z
Słowa kluczowe: miażdżyca, komórki śródbłonka, polaryzacja makrofagów, zapalnie, IL-32 gamma