Clear Sky Science · he
הגברה של IL-32γ בתאי אנדותל מקדמת גיוס מאקרופאגים והתקדמות דלקתית באטרוסקלרוזיס
מדוע המחקר הזה חשוב לבריאות הלב
אטרוסקלרוזיס — סתימת והקשחת העורקים — הוא הגורם השורשי לרוב התקפי הלב והשבץ. ידוע לנו כי כולסטרול, במיוחד בצורתו המושחתת, ודלקת כרונית שניהם מדרבנים את המחלה, אך כיצד שני הכוחות הללו מתקשרים בתוך כלי הדם עדיין לא מובן במלואו. המחקר הזה מתמקד בין היתר בשליח דלקתי פחות מוכר בשם IL‑32γ ומראה כיצד הוא מסייע להפוך תאי השקף (האנדותל) הלחוצים למגנטים ומגברים חזקים עבור תאי מערכת החיסון המזיקים, מה שיכול לפתוח נתיב חדש לשיכוך דלקת עורקי מהשורש.
מבט מקרוב על עורקים סתומים
העורקים מצופים בשכבה דקה של תאי אנדותל שבדרך כלל יוצרים מחסום חלק ומגן בין הדם לדופן הכלי. כאשר רמות ה"כולסטרול הרע" גבוהות, חלק מהחלקיקים הללו חודרים מתחת לשכבה זו והתחמצנו — גרסאות כימיות פגומות הידועות כ‑Ox‑LDL. הכולסטרול המחומצן הזה מגרה את תאי האנדותל, גורם להם להיות דולפים ודביקים, ומושך תאים חיסוניים שנקראים מונוציטים, שהופכים למאקרופאגים הסופגים שומנים. עם הזמן תאים העמוסים בשומן, יחד עם רקמת צלקת, מצטברים ליצירת פלאקים שיכולים להתפרק בפתאומיות ולחסום את זרימת הדם ללב או למוח. 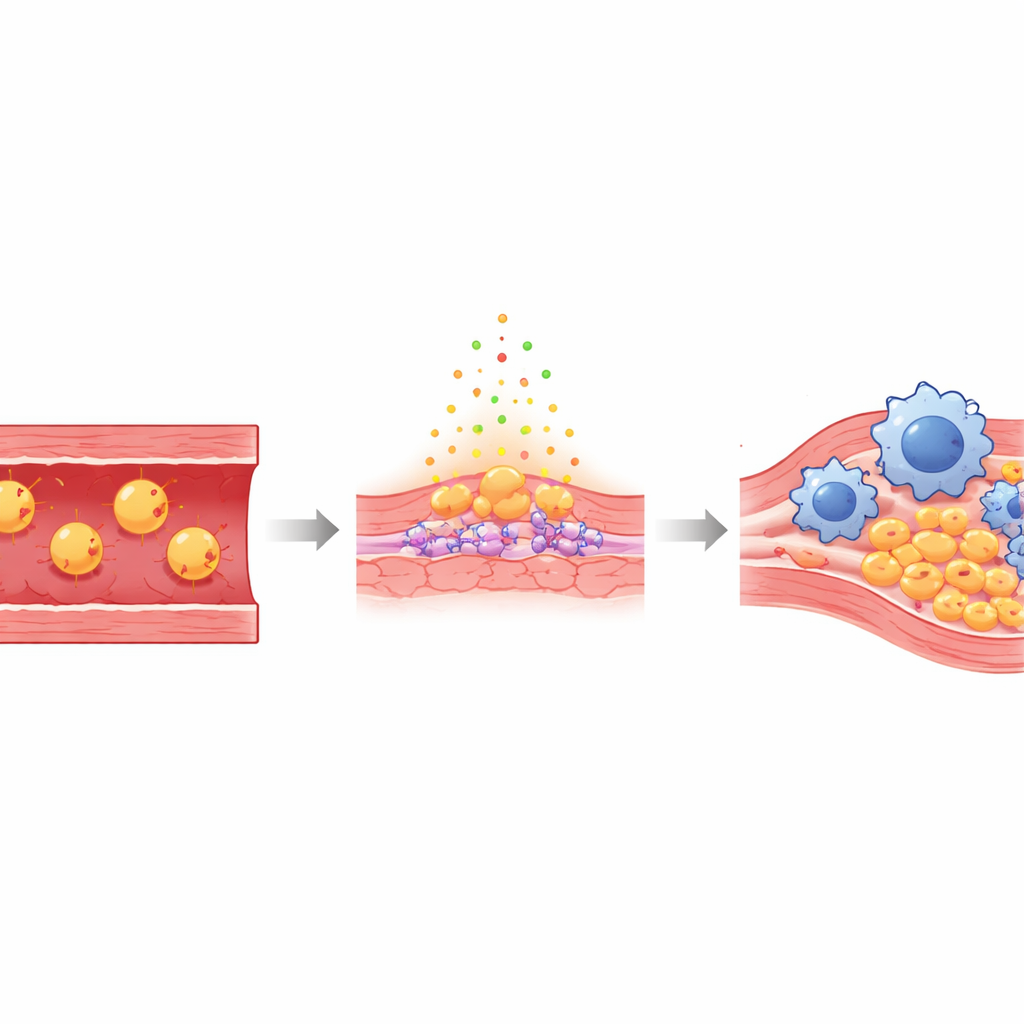
השליח הדלקתי במרכז
החוקרים התמקדו ב‑IL‑32, חלבון דלקתי הקיים במספר צורות; IL‑32γ נחשב לפעיל ביותר. הם מדדו תחילה וריאנטים שונים של IL‑32 בדם מאנשים עם אטרוסקלרוזיס ומתנדבים בריאים. רק IL‑32γ נמצא גבוה באופן בולט בחולים, הן ברמת הגן והן ברמת החלבון, מה שמרמז על קשר ספציפי למחלת העורקים. לאחר מכן החשיפו תאי אנדותל אנושיים ל‑Ox‑LDL במעבדה. תחת הלחץ הזה, התאים הגבירו בחדות את ייצור ושחרור IL‑32γ, בעוד שצורות אחרות של IL‑32 כמעט שלא השתנו. במקביל, יכולתם של התאים לגדול, להגר ולהרכיב מבנים דמויי כלי דם ירדה, והם הגבירו מולקולות שמסייעות לתפוס תאי חיסון עוברים — סימנים קלאסיים של תפקוד לקוי של האנדותל.
כיצד תאי הכלי דוחפים מאקרופאגים למצב מזיק
כדי לראות מה משמעות הדבר להתנהגות החיסון, הצוות תרבת תאי אנדותל שטופלו ב‑Ox‑LDL יחד עם מאקרופאגים במערכת Transwell שמאפשרת תקשורת דרך אותות מסיסים. מאקרופאגים שנחשפו לתאי אנדותל לחוצים נוטו לדפוס פרו‑דלקתי חזק של "M1": הם הוצגו עם סמני שטח המקושרים למצב התקפי, ייצרו יותר גורמים דלקתיים כמו TNF‑α ו‑IL‑1β ונעו ביתר קלות לעבר שכבת האנדותל. כאשר החוקרים חסמו מתג מרכזי בתוך תאי האנדותל, מסלול NF‑κB, הם הקטינו גם את שחרור IL‑32γ וגם את הנטייה למצב M1. נטרול של IL‑32γ עצמה השיג אפקט דומה, הוריד סמני דלקת ועיכב תזוזת מאקרופאגים, מה שמצביע על IL‑32γ כגורם מתווך מרכזי.
התמקדות בשרשרת האיתות
האחראים בדקו האם IL‑32γ יכול לפעול ישירות על מאקרופאגים ובאיזה מסלול. הוספת IL‑32γ טהור למאקרופאגים, ללא תאי אנדותל נוכחים, הספיקה לדחוף אותם למצב M1 ולהגביר את תנועתם. תגובה זו היתה תלויה ברליי מולקולרי אחר בתוך התאים — מסלול p38 MAPK: כאשר הוסף תרופה שחוסמת p38, IL‑32γ לא הגביר עוד גנים דלקתיים, שחרור ציטוקינים או הגירה. 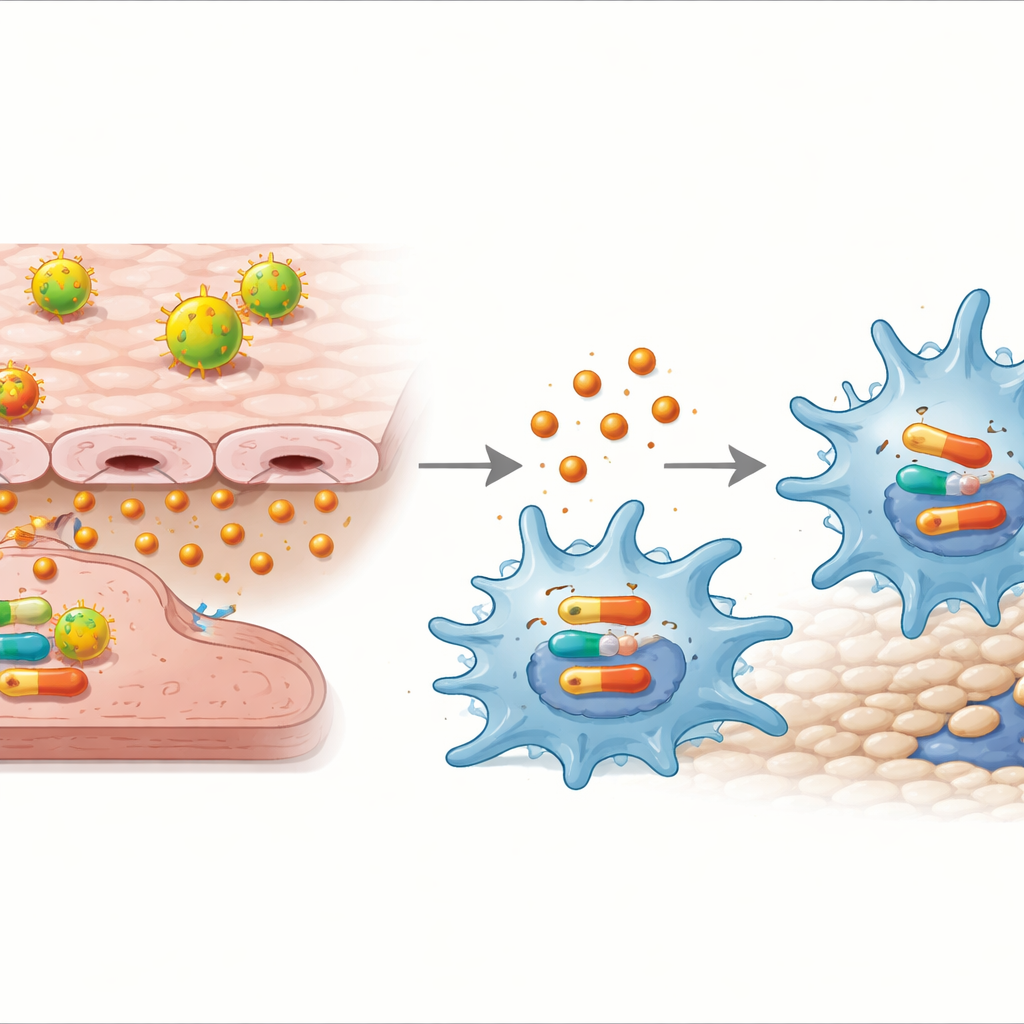
מה קורה בעורקים חיים
לבסוף, הצוות בדק את המסלול בעכברים הנוטים גנטית לאטרוסקלרוזיס והאוכלים דיאטה עתירת שומן בסגנון מערבי. עכברים שקיבלו הזרקות של IL‑32γ פיתחו פלאקים עורקיים גדולים יותר, הראו הצטברות מאקרופאגים רבה יותר בתוך הפלאקים והיו להם רמות דם גבוהות יותר של מולקולות דלקתיות — על אף שרמות הכולסטרול היו דומות לשלו של קבוצת הביקורת. כאשר נחסם מסלול ה‑p38 בבעלי החיים הללו, גודל הפלאק, הצטברות המאקרופאגים והדלקת ירדו חזרה לכיוון הבסיס. משמעות הדבר היא ש‑IL‑32γ יכול להאיץ את גידול הפלאק בעורקים החיים בעיקר על ידי הגברה של איתות דלקתי, ולא על ידי שינוי השומנים בדם.
מה המשמעות לעתיד הטיפולים
בהתבוננות כוללת, העבודה מציירת שרשרת של אירועים: כולסטרול מחומצן מגרה את שכבת הכלי, תאים אלה משיבים בשחרור IL‑32γ, ו‑IL‑32γ מעורר מאקרופאגים סמוכים למצב תוקפני שמקדם פלאקים דרך איתות p38. בזיהוי IL‑32γ כקישור מפתח בין תאי אנדותל פגועים ותאים חיסוניים פעילים מדי, המחקר מציע זווית טיפולית חדשה: במקום רק להוריד כולסטרול, תרופות עתידיות עשויות גם למקד את IL‑32γ או את מסלול p38 כדי לקרר את הדלקת בתוך דופנות העורקים ולהאט, או אולי להפוך, התקדמות האטרוסקלרוזיס.
ציטוט: Yang, Z., Liu, M., Shi, Y. et al. Upregulation of IL-32γ in endothelial cells promotes macrophage recruitment and inflammatory progression in atherosclerosis. Sci Rep 16, 11262 (2026). https://doi.org/10.1038/s41598-026-40151-z
מילות מפתח: אטרוסקלרוזיס, תאי אנדותל, הסתיידות מאקרופאגים, דלקת, IL-32 גמא