Clear Sky Science · ru
Повышенная экспрессия IL-32γ в эндотелиальных клетках способствует привлечению макрофагов и прогрессированию воспаления при атеросклерозе
Почему это исследование важно для здоровья сердца
Атеросклероз — закупорка и ожесточение артерий — является основной причиной большинства инфарктов и инсультов. Известно, что холестерин, особенно в повреждённой форме, и хроническое воспаление содействуют развитию этого заболевания, но то, как эти два фактора взаимодействуют внутри сосудов, ещё полностью не выяснено. В этом исследовании внимание концентрируется на малоизвестном провоспалительном медиаторе IL‑32γ: показано, как он превращает стрессированные клетки внутренней оболочки сосудов в мощные «магниты» и усилители для вредоносных иммунных клеток, что открывает возможную новую стратегию для подавления артериального воспаления у его источника.
Ближе к сути: что происходит в закупоренных артериях
Артерии выстланы тонким слоем эндотелиальных клеток, которые обычно образуют гладкий защитный барьер между кровью и стенкой сосуда. При высоком уровне «плохого» холестерина некоторые частицы проникают под этот слой и окисляются — превращаясь в химически повреждённые формы, известные как Ox‑LDL. Этот окисленный холестерин раздражает эндотелий: клетки становятся проницаемыми и липкими, привлекая иммунные клетки — моноциты, которые превращаются в макрофаги и поглощают жир. Со временем эти жиронасыщенные клетки вместе с рубцовой тканью накапливаются в виде бляшек, которые могут внезапно разорваться и перекрыть приток крови к сердцу или мозгу. 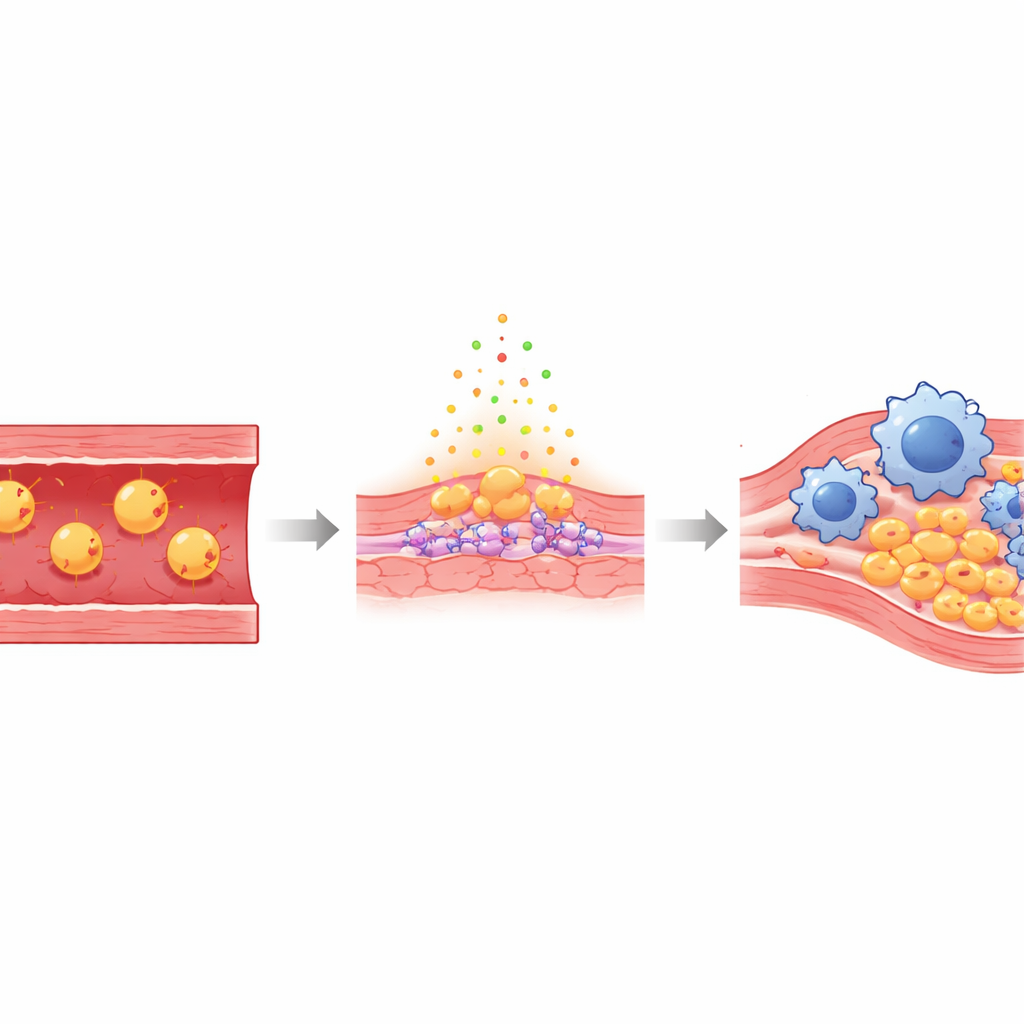
Провоспалительный медиатор в центре внимания
Исследователи сосредоточились на IL‑32 — воспалительном белке, существующем в нескольких вариантах, при этом IL‑32γ считается наиболее активной формой. Сначала они измеряли уровни различных вариантов IL‑32 в крови у людей с атеросклерозом и у здоровых добровольцев. Только IL‑32γ оказалась явно повышенной у пациентов как на уровне гена, так и на уровне белка, что указывает на её возможную связь с заболеванием артерий. Затем человеческие эндотелиальные клетки в лаборатории подвергали воздействию Ox‑LDL. Под таким стрессом клетки резко увеличивали производство и выделение IL‑32γ, тогда как другие варианты IL‑32 почти не менялись. Одновременно клетки теряли способность к пролиферации, миграции и формированию сосудистых структур и усиливали экспрессию молекул, захватывающих проходящие иммунные клетки — классические признаки дисфункции эндотелия.
Как клетки сосуда направляют макрофагов в вредоносное состояние
Чтобы выяснить, что это означает для поведения иммунных клеток, команда совместно культивировала эндотелий, обработанный Ox‑LDL, с макрофагами в системе Transwell, где клетки обмениваются растворимыми сигналами. Макрофаги, подвергшиеся влиянию стрессированных эндотелиальных клеток, смещались в ярко выраженный провоспалительный «M1»-профиль: они проявляли поверхностные маркеры, связанные с атакующим состоянием, вырабатывали больше провоспалительных молекул, таких как TNF‑α и IL‑1β, и активнее мигрировали к эндотелию. Блокировка ключевого переключателя внутри эндотелиоцитов — пути NF‑κB — подавляла и выделение IL‑32γ, и сдвиг в сторону M1. Нейтрализация самой IL‑32γ давала похожий эффект: снижение воспалительных маркеров и уменьшение подвижности макрофагов, что указывает на роль IL‑32γ как центрального посредника.
Вглубь сигнализации
Учёные затем проверили, может ли IL‑32γ действовать непосредственно на макрофаги и каким путём. Добавление очищенной IL‑32γ к макрофагам без присутствия эндотелиоцитов было достаточно, чтобы направить их в состояние M1 и увеличить их подвижность. Эта реакция зависела от другого клеточного каскада — пути p38 MAPK: при добавлении блокады p38 IL‑32γ переставала усиливать экспрессию провоспалительных генов, выделение цитокинов и миграцию. 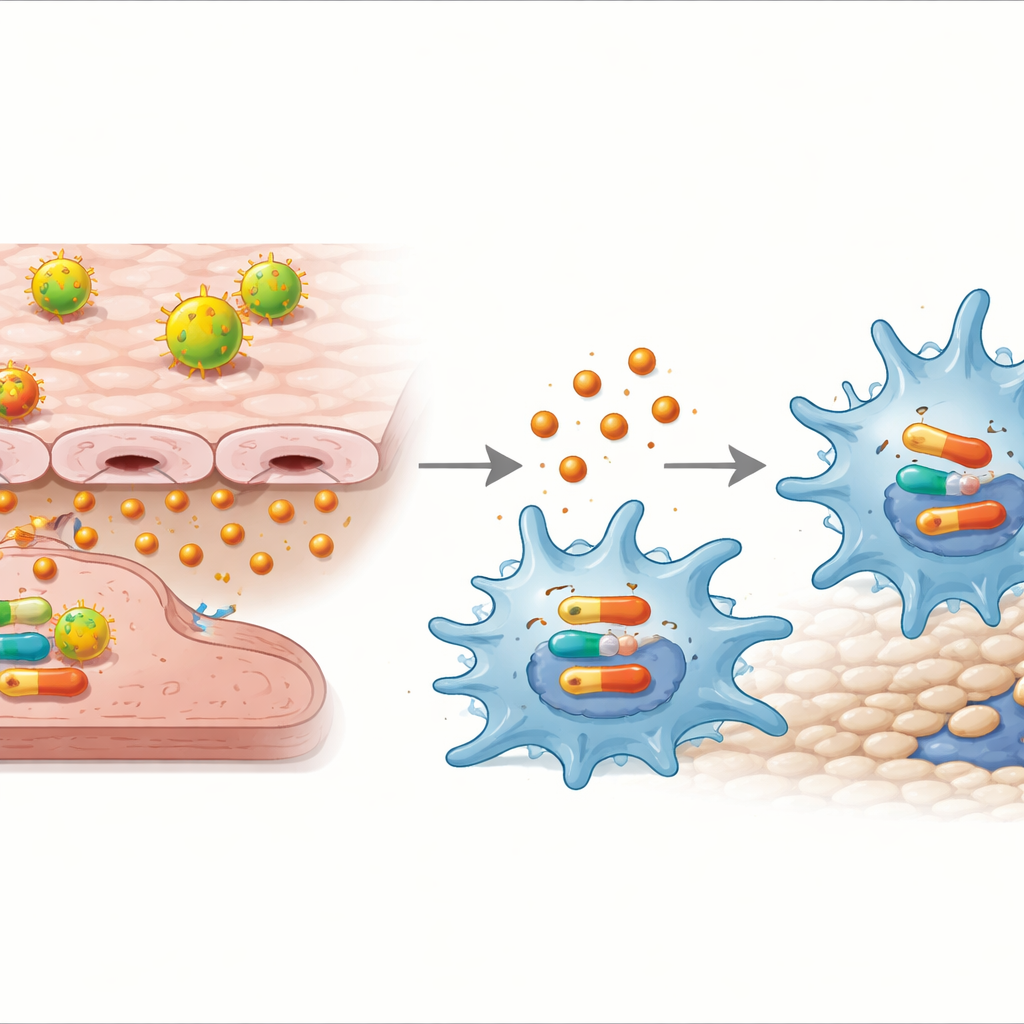
Что происходит в живых артериях
Наконец, команда протестировала этот путь у мышей, генетически предрасположенных к атеросклерозу, которых кормили западной диетой с высоким содержанием жиров. У мышей, которым вводили IL‑32γ, образовывались более крупные артериальные бляшки, в них накапливалось больше макрофагов, а в крови повышались уровни воспалительных молекул — несмотря на сопоставимые уровни холестерина по сравнению с контрольной группой. При блокировании пути p38 у этих животных размер бляшек, накопление макрофагов и воспаление снижались почти до исходных значений. Это означает, что IL‑32γ ускоряет рост бляшек в живых артериях преимущественно за счёт усиления воспалительной сигнализации, а не изменения липидного профиля крови.
Что это значит для будущих терапий
В совокупности работа описывает последовательность событий: окисленный холестерин раздражает внутреннюю оболочку сосудов, эти клетки отвечают выделением IL‑32γ, а IL‑32γ, в свою очередь, переводит соседних макрофагов в агрессивный, способствующий формированию бляшек режим через сигнальный путь p38. Идентификация IL‑32γ как ключевого звена между повреждённым эндотелием и сверхактивными иммунными клетками предлагает новый терапевтический подход: помимо снижения холестерина, будущие препараты могли бы нацеливаться на IL‑32γ или его путь p38, чтобы охладить воспаление в стенках артерий и замедлить или, возможно, обратить вспять прогрессирование атеросклероза.
Цитирование: Yang, Z., Liu, M., Shi, Y. et al. Upregulation of IL-32γ in endothelial cells promotes macrophage recruitment and inflammatory progression in atherosclerosis. Sci Rep 16, 11262 (2026). https://doi.org/10.1038/s41598-026-40151-z
Ключевые слова: атеросклероз, эндотелиальные клетки, поляризация макрофагов, воспаление, IL-32 гамма