Clear Sky Science · es
Regulación al alza de IL-32γ en células endoteliales promueve el reclutamiento de macrófagos y la progresión inflamatoria en la aterosclerosis
Por qué esta investigación importa para la salud cardiaca
La aterosclerosis —obstrucción y endurecimiento de las arterias— es la causa raíz de la mayoría de los infartos y los accidentes cerebrovasculares. Sabemos que el colesterol, especialmente en sus formas dañadas, y la inflamación crónica impulsan esta enfermedad, pero todavía se está investigando cómo dialogan ambas fuerzas dentro de los vasos sanguíneos. Este estudio se centra en un mensajero inflamatorio poco conocido llamado IL‑32γ y muestra cómo ayuda a convertir a las células que recubren los vasos en potentes imanes y amplificadores para células inmunitarias dañinas, lo que podría abrir una nueva vía para calmar la inflamación arterial en su origen.
Una mirada más cercana a las arterias obstruidas
Las arterias están revestidas por una delgada capa de células endoteliales que normalmente forman una barrera protectora y lisa entre la sangre y la pared vascular. Cuando los niveles de colesterol «malo» son altos, algunas de estas partículas se infiltran por debajo de este revestimiento y se oxidan: versiones químicamente dañadas conocidas como Ox‑LDL. Este colesterol oxidado irrita a las células endoteliales, volviéndolas permeables y pegajosas, y atrae a células inmunitarias llamadas monocitos, que se transforman en macrófagos que engullen grasa. Con el tiempo, estas células cargadas de lípidos, junto con tejido cicatricial, se acumulan en placas que pueden romperse de forma súbita, bloqueando el flujo sanguíneo hacia el corazón o el cerebro. 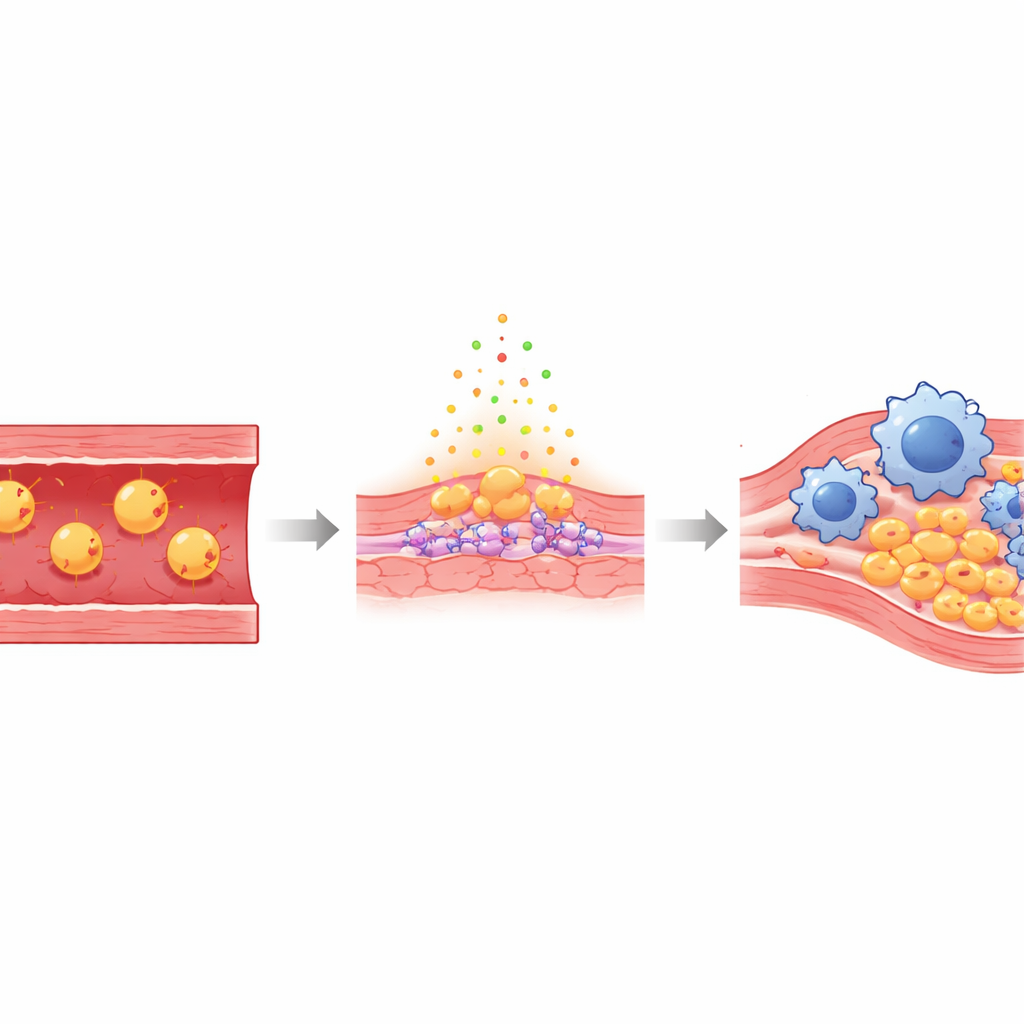
El mensajero inflamatorio en el centro
Los investigadores se centraron en IL‑32, una proteína inflamatoria que existe en varias formas, siendo IL‑32γ considerada la más activa. Primero midieron diferentes variantes de IL‑32 en sangre de personas con aterosclerosis y de voluntarios sanos. Solo IL‑32γ estaba claramente aumentada en los pacientes, tanto a nivel génico como proteico, lo que sugiere que podría estar especialmente ligada a la enfermedad arterial. Luego expusieron células endoteliales humanas a Ox‑LDL en el laboratorio. Bajo este estrés, las células aumentaron de forma pronunciada la producción y liberación de IL‑32γ, mientras que otras variantes de IL‑32 cambiaron muy poco. Al mismo tiempo, las células perdieron capacidad para proliferar, migrar y formar nuevas estructuras similares a vasos, y además incrementaron moléculas que favorecen la adhesión de células inmunitarias circulantes: signos clásicos de disfunción endotelial.
Cómo las células vasculares empujan a los macrófagos hacia un estado dañino
Para ver qué significaba esto para el comportamiento inmune, el equipo co-cultivó células endoteliales tratadas con Ox‑LDL junto con macrófagos en un sistema Transwell que permite la comunicación mediante señales solubles. Los macrófagos expuestos a células endoteliales estresadas se desplazaron hacia un patrón fuertemente proinflamatorio «M1»: mostraron marcadores de superficie asociados con un modo agresivo, produjeron más sustancias inflamatorias como TNF‑α e IL‑1β, y migraron con mayor facilidad hacia la capa endotelial. Cuando los investigadores bloquearon un interruptor clave dentro de las células endoteliales, la vía NF‑κB, redujeron tanto la liberación de IL‑32γ como este sesgo hacia M1. Neutralizar IL‑32γ tuvo un efecto similar, disminuyendo marcadores inflamatorios y frenando el movimiento de los macrófagos, lo que señala a IL‑32γ como un intermediario central.
Acercándose a la cadena de señalización
Los científicos preguntaron entonces si IL‑32γ podría actuar directamente sobre los macrófagos y por qué ruta. Añadir IL‑32γ purificada a macrófagos, sin presencia de células endoteliales, fue suficiente para empujarlos hacia el estado M1 y aumentar su migración. Esta respuesta dependió de otra vía molecular dentro de las células, la vía p38 MAPK: cuando se añadió un fármaco bloqueador de p38, IL‑32γ dejó de estimular genes inflamatorios, la liberación de citocinas y la migración. 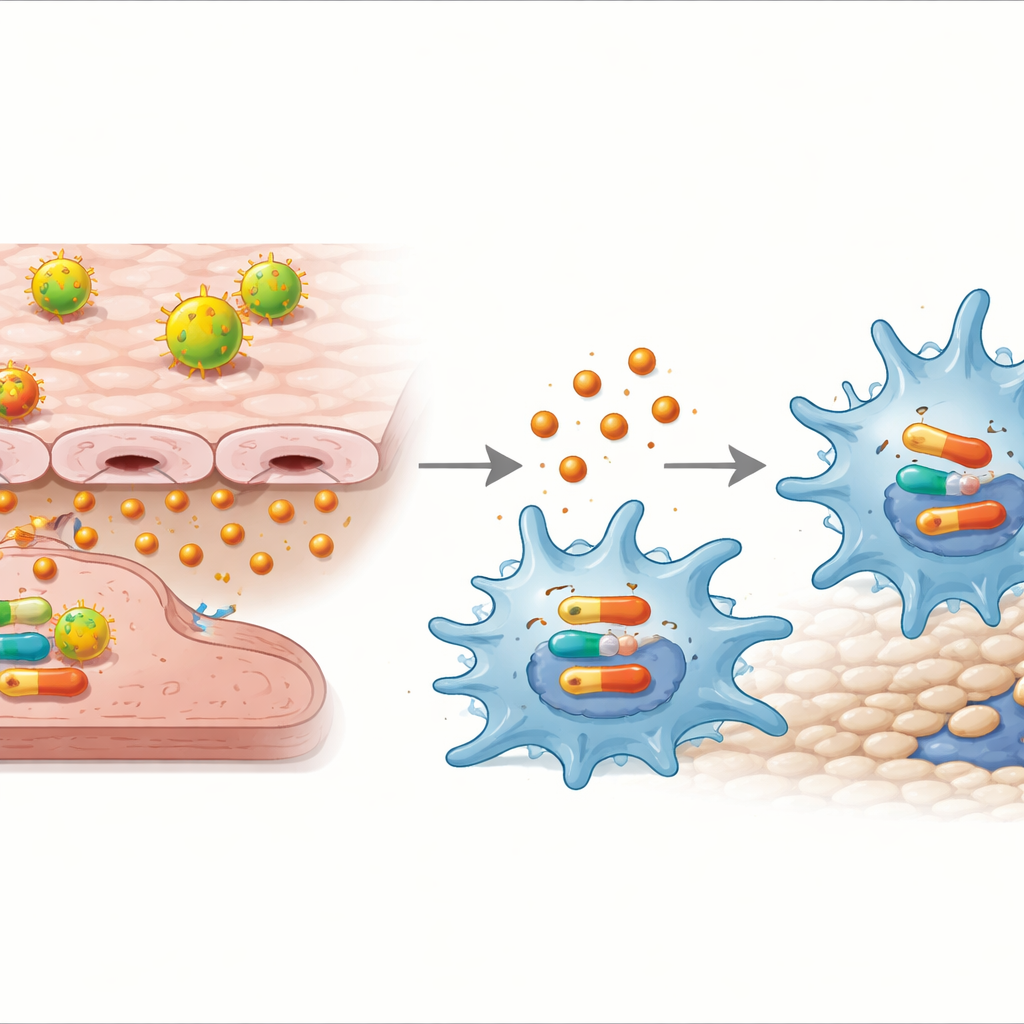
Qué ocurre en arterias vivas
Finalmente, el equipo probó la vía en ratones genéticamente propensos a la aterosclerosis y alimentados con una dieta rica en grasas al estilo occidental. Los ratones inyectados con IL‑32γ desarrollaron placas arteriales más grandes, mostraron mayor acumulación de macrófagos dentro de esas placas y tuvieron niveles sanguíneos más altos de moléculas inflamatorias, pese a presentar niveles de colesterol similares a los controles. Cuando se bloqueó la vía p38 en estos animales, el tamaño de las placas, la acumulación de macrófagos y la inflamación descendieron hacia los valores de referencia. Esto indica que IL‑32γ puede acelerar el crecimiento de placas en arterias vivas principalmente al potenciar la señalización inflamatoria, y no por alterar los lípidos sanguíneos.
Qué significa todo esto para tratamientos futuros
En conjunto, este trabajo describe una cadena de eventos: el colesterol oxidado irrita el revestimiento vascular, esas células responden liberando IL‑32γ, y IL‑32γ a su vez induce a los macrófagos cercanos a un modo agresivo que promueve la placa a través de la señalización p38. Al identificar a IL‑32γ como un eslabón clave entre las células endoteliales dañadas y las células inmunitarias sobreactivadas, el estudio sugiere un nuevo ángulo terapéutico: en lugar de limitarse a reducir el colesterol, los fármacos futuros podrían también dirigirse a IL‑32γ o a su vía p38 para enfriar la inflamación dentro de las paredes arteriales y frenar, o posiblemente revertir, la progresión de la aterosclerosis.
Cita: Yang, Z., Liu, M., Shi, Y. et al. Upregulation of IL-32γ in endothelial cells promotes macrophage recruitment and inflammatory progression in atherosclerosis. Sci Rep 16, 11262 (2026). https://doi.org/10.1038/s41598-026-40151-z
Palabras clave: aterosclerosis, células endoteliales, polarización de macrófagos, inflamación, IL-32 gamma