Clear Sky Science · it
Upregulation of IL-32γ nelle cellule endoteliali promuove il reclutamento dei macrofagi e la progressione infiammatoria nell’aterosclerosi
Perché questa ricerca è importante per la salute del cuore
L’aterosclerosi—l’intasamento e l’indurimento delle arterie—è la causa principale della maggior parte degli infarti e degli ictus. Sappiamo che il colesterolo, specialmente nella sua forma danneggiata, e l’infiammazione cronica guidano questa malattia, ma i meccanismi con cui queste due forze comunicano all’interno dei vasi sanguigni sono ancora in fase di studio. Questo lavoro si concentra su un mediatore infiammatorio poco conosciuto chiamato IL‑32γ e mostra come contribuisca a trasformare le cellule che rivestono i vasi in potenti calamite e amplificatori per cellule immunitarie dannose, aprendo potenzialmente una nuova via per calmare l’infiammazione arteriosa alla sua fonte.
Uno sguardo più ravvicinato alle arterie intasate
Le arterie sono rivestite da un sottile strato di cellule endoteliali che normalmente formano una barriera liscia e protettiva tra il sangue e la parete vascolare. Quando i livelli di colesterolo “cattivo” sono elevati, alcune di queste particelle si infilano sotto questo rivestimento e vengono ossidate—forme chimicamente danneggiate note come Ox‑LDL. Questo colesterolo ossidato irrita le cellule endoteliali, rendendole più permeabili e aderenti, e richiama cellule immunitarie chiamate monociti, che si trasformano in macrofagi e fagocitano i lipidi. Col tempo, queste cellule impregnate di grasso, insieme al tessuto cicatriziale, accumulano placche che possono improvvisamente rompersi, bloccando il flusso sanguigno al cuore o al cervello. 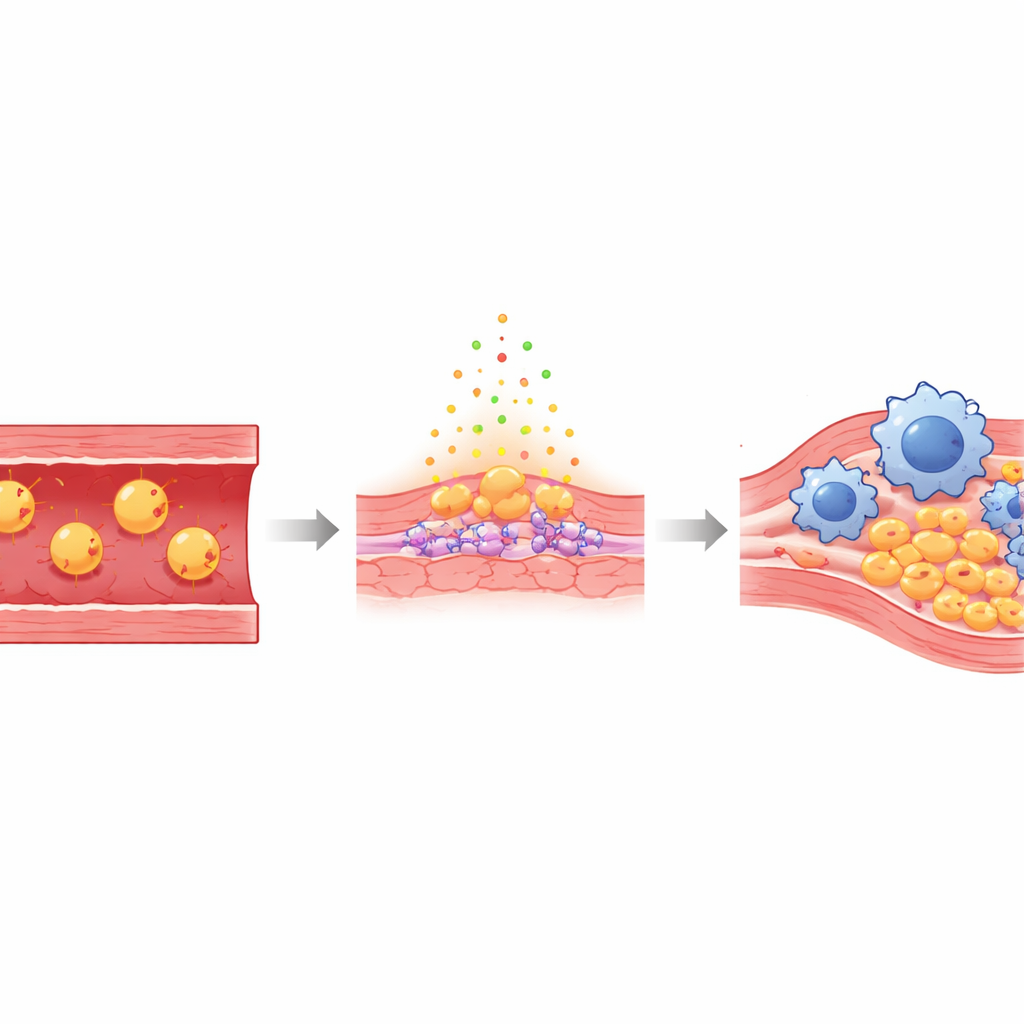
Il mediatore infiammatorio al centro
I ricercatori si sono concentrati su IL‑32, una proteina infiammatoria che esiste in diverse isoforme, con IL‑32γ considerata la più attiva. Hanno prima misurato le diverse varianti di IL‑32 nel sangue di persone con aterosclerosi e di volontari sani. Solo IL‑32γ risultava chiaramente aumentata nei pazienti, sia a livello genico che proteico, suggerendo un legame specifico con la malattia arteriosa. Hanno poi esposto cellule endoteliali umane a Ox‑LDL in laboratorio. Sotto questo stress, le cellule aumentarono drasticamente la produzione e il rilascio di IL‑32γ, mentre le altre forme di IL‑32 cambiarono poco. Allo stesso tempo, le cellule persero capacità di proliferare, migrare e formare nuove strutture simili a vasi, e incrementarono molecole che favoriscono l’adesione delle cellule immunitarie di passaggio—segni classici di disfunzione endoteliale.
Come le cellule vascolari spingono i macrofagi verso uno stato nocivo
Per capire cosa implicasse ciò per il comportamento immunitario, il gruppo ha co‑coltivato cellule endoteliali trattate con Ox‑LDL insieme a macrofagi in un sistema Transwell che permette la comunicazione tramite segnali solubili. I macrofagi esposti alle cellule endoteliali stressate si polarizzarono verso un marcato fenotipo pro‑infiammatorio “M1”: presentarono marcatori di superficie associati a uno stato di attacco, produssero più sostanze infiammatorie come TNF‑α e IL‑1β e migrarono più facilmente verso lo strato endoteliale. Quando i ricercatori bloccarono un interruttore chiave all’interno delle cellule endoteliali, la via NF‑κB, attenuarono sia il rilascio di IL‑32γ sia questa polarizzazione M1. Neutralizzare direttamente IL‑32γ ebbe un effetto simile, riducendo i marcatori infiammatori e limitando la mobilità dei macrofagi, indicando IL‑32γ come un mediatore centrale.
Un zoom sulla catena di segnalazione
Gli scienziati hanno poi indagato se IL‑32γ potesse agire direttamente sui macrofagi e tramite quale via. Aggiungere IL‑32γ purificata ai macrofagi, in assenza di cellule endoteliali, fu sufficiente per indurli nello stato M1 e aumentare la loro migrazione. Questa risposta dipendeva da un altro circuito molecolare interno alle cellule, la via p38 MAPK: quando fu aggiunto un farmaco inibitore di p38, IL‑32γ non aumentò più l’espressione dei geni infiammatori, il rilascio di citochine né la migrazione. 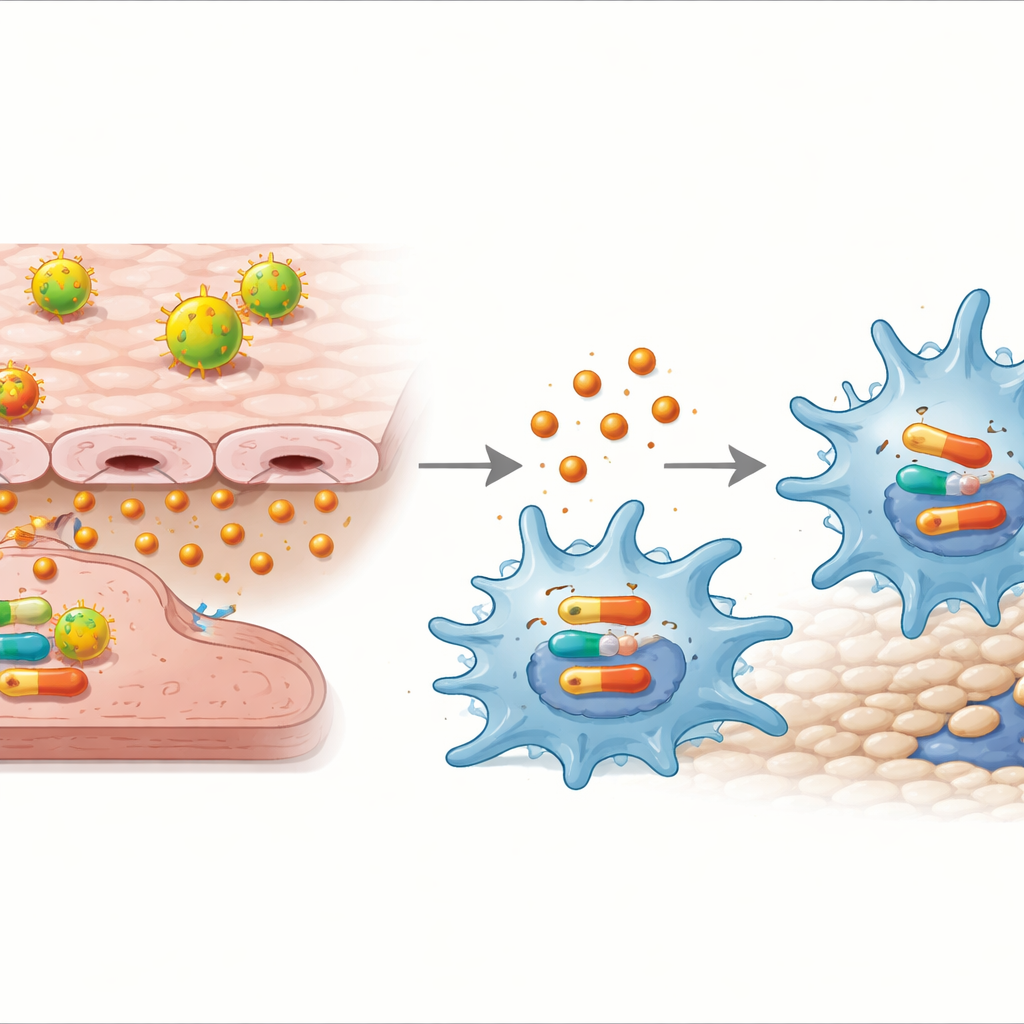
Cosa accade nelle arterie vive
Infine, il gruppo ha testato la via nelle topi geneticamente predisposti all’aterosclerosi e nutriti con una dieta ricca di grassi in stile occidentale. I topi iniettati con IL‑32γ svilupparono placche arteriose più grandi, mostrarono un maggiore accumulo di macrofagi all’interno di quelle placche e avevano livelli ematici più alti di molecole infiammatorie—nonostante livelli di colesterolo simili rispetto ai controlli. Quando la via p38 fu bloccata in questi animali, la dimensione delle placche, l’accumulo di macrofagi e l’infiammazione diminuirono verso i valori di base. Ciò indica che IL‑32γ può accelerare la crescita delle placche nelle arterie viventi principalmente aumentando la segnalazione infiammatoria, non modificando i lipidi ematici.
Cosa significa tutto questo per i trattamenti futuri
Nel complesso, questo lavoro delinea una catena di eventi: il colesterolo ossidato irrita il rivestimento vascolare, quelle cellule rispondono rilasciando IL‑32γ, e IL‑32γ a sua volta induce i macrofagi vicini in uno stato aggressivo che promuove la placca attraverso la segnalazione p38. Identificando IL‑32γ come un anello chiave tra le cellule endoteliali danneggiate e le cellule immunitarie iperattive, lo studio suggerisce un nuovo approccio terapeutico: invece di limitarsi ad abbassare il colesterolo, farmaci futuri potrebbero anche mirare a IL‑32γ o alla sua via p38 per raffreddare l’infiammazione all’interno delle pareti arteriose e rallentare, o possibilmente invertire, la progressione dell’aterosclerosi.
Citazione: Yang, Z., Liu, M., Shi, Y. et al. Upregulation of IL-32γ in endothelial cells promotes macrophage recruitment and inflammatory progression in atherosclerosis. Sci Rep 16, 11262 (2026). https://doi.org/10.1038/s41598-026-40151-z
Parole chiave: aterosclerosi, cellule endoteliali, polarizzazione dei macrofagi, infiammazione, IL-32 gamma