Clear Sky Science · sv
DeepStackVEGF — ett stacking-ensemble djupinlärningsramverk för prognos av vaskulär endotelial tillväxtfaktor
Varför det spelar roll att förutsäga en läkningssignal
Våra kroppar är beroende av ett protein som kallas vaskulär endotelial tillväxtfaktor, eller VEGF, för att bilda nya blodkärl. Denna signal är avgörande för att läka sår, reparera ben och stödja normal utveckling — men cancer utnyttjar den också för att mata tumörer och sprida sig i kroppen. Att mäta och karaktärisera VEGF i laboratoriet är tidskrävande och kostsamt. Denna studie introducerar DeepStack-VEGF, en kraftfull datormodell som snabbt kan förutsäga om ett givet protein beter sig som VEGF, vilket potentiellt kan påskynda läkemedelsupptäckt och precisionsmedicin.
Från bänk i labbet till bärbar dator
Traditionellt använder forskare sofistikerade tekniker som kristallografi, NMR och vävnadsfärgning för att studera VEGF. Dessa metoder avslöjar molekylens struktur och plats, men kräver specialutrustning och tid. Samtidigt innehåller stora offentliga databaser nu miljontals proteinsekvenser vars funktioner bara delvis är kända. Författarna såg en möjlighet: istället för att först odla kristaller eller genomföra komplexa experiment, varför inte låta datorer sålla igenom proteinsekvenser och flagga dem som sannolikt uppträder som VEGF? DeepStack-VEGF är designad som ett snabbt, skalbart verktyg för just detta — att omvandla råa proteintecken till meningsfulla förutsägelser.
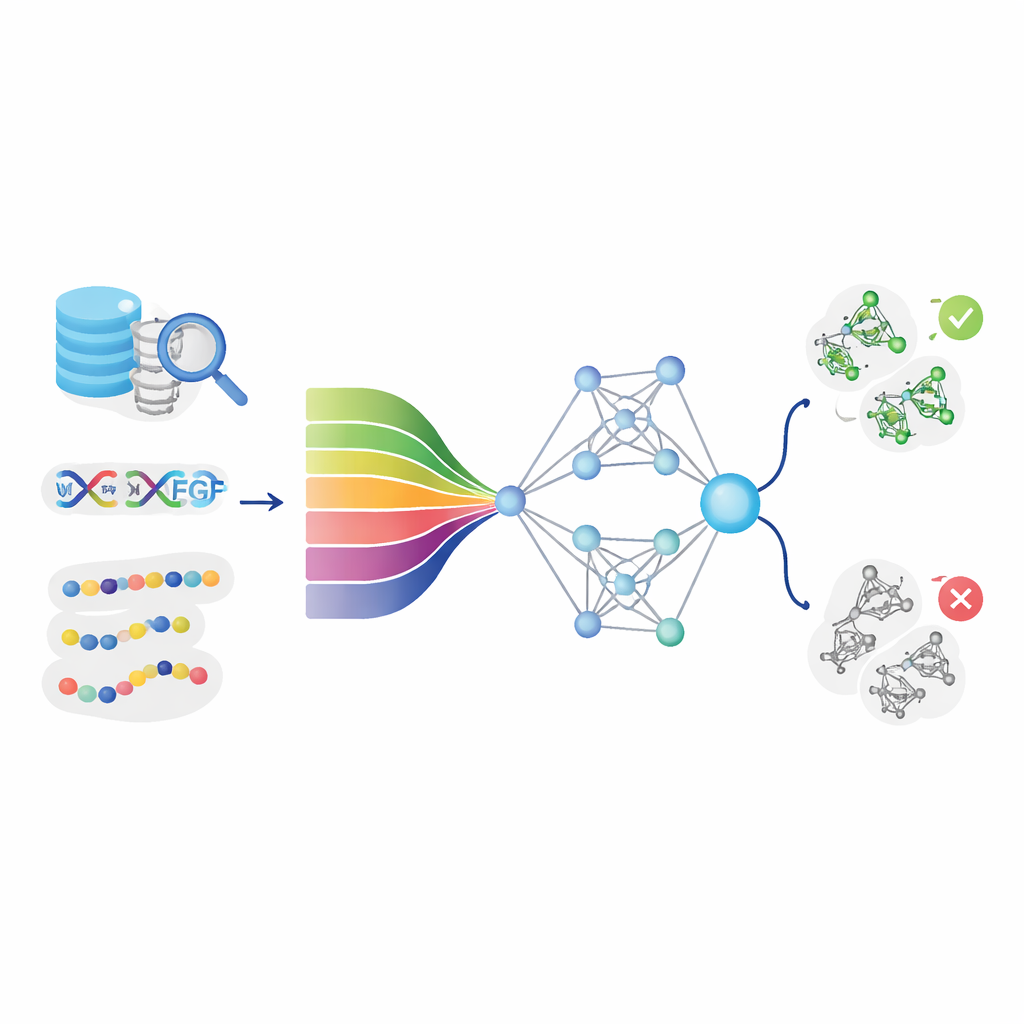
Att lära datorer läsa proteinets ”språk”
Kärn idén bakom DeepStack-VEGF är att en proteins sekvens innehåller dolda mönster som ger ledtrådar till dess beteende. Teamet samlade tusentals VEGF- och icke-VEGF-proteiner från stora databaser och rensade noggrant bort nära duplikat. De beskrev varje protein ur många vinklar. Vissa egenskaper fångade grundläggande kemi, som hur oljiga eller laddade olika positioner är. Andra sammanfattade hur ofta vissa par eller tripletter av byggstenar förekommer, eller hur kedjan sannolikt veckas till helixar och skivor. Avgörande använde modellen också moderna ”protein-språkmodeller” — artificiella intelligenssystem som, likt språkverktyg för text, lär sig djupa mönster från miljontals naturliga proteinsekvenser och omvandlar varje sekvens till ett rikt numeriskt fingeravtryck.
Förening av många synsätt till ett beslut
Att enkelt stapla tusentals numeriska egenskaper kan introducera brus, så forskarna använde en selektionsmetod som behåller endast de mest informativa signalerna. Dessa förfinade egenskaper matades sedan in i tre olika djupinlärningsmoduler, var och en med en distinkt specialitet. En modell var särskilt bra på att följa långdistansmönster längs sekvensen, en annan fångade lokala strukturella motiv och deras relationer, och en tredje använde en spel-liknande generator–kritiker-uppsättning för att berika och regularisera data. Ovanpå dessa lärde ett ”meta”-lager sig hur deras utdata bäst kombineras och bildade DeepStack-VEGF-ensemblen. Denna flerskiktade strategi speglar hur en expertpanel, där varje medlem har olika träning, kan väga in innan ett gemensamt uttalande fattas.
Kontroll av noggrannhet och att öppna svart låda
För att testa sitt system använde författarna rigorös korsvalidering och en oberoende testmängd. Över flera mått på noggrannhet överträffade DeepStack-VEGF var och en av sina komponentmodeller och två tidigare state-of-the-art VEGF-prediktorer. Den slutliga versionen klassificerade korrekt VEGF-liknande proteiner i klart över nio av tio fall, med färre falsklarm än konkurrerande metoder. Teamet tillämpade också en förklaringsmetod som uppskattar hur mycket varje indataegenskap skjuter ett beslut mot ”VEGF” eller ”inte VEGF”. Denna analys visade att de inlärda protein-språkfing eravtrycken bidrog med största delen av den prediktiva kraften, medan traditionella kemi- och strukturbaserade egenskaper lade till finmaskig detalj och stabilitet.
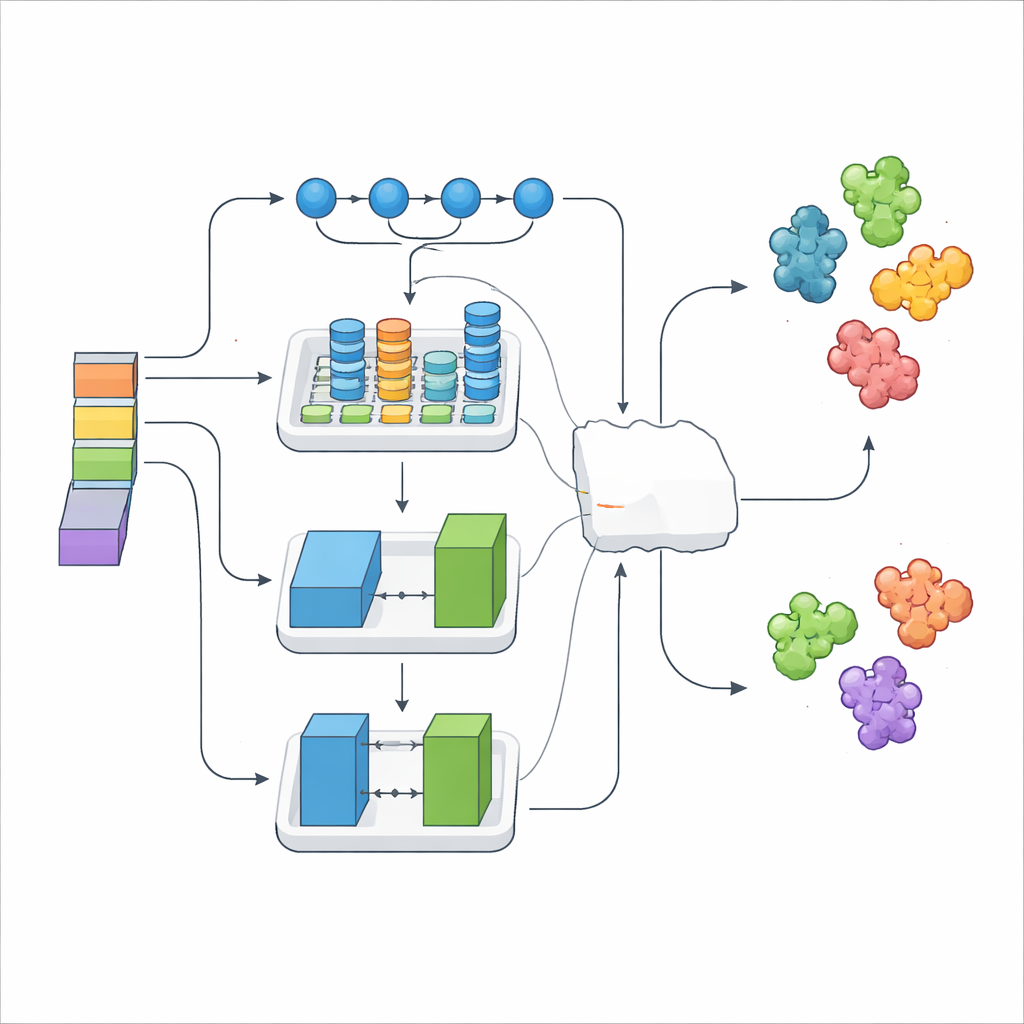
Vad detta betyder för medicin och forskning
För icke-specialister kan DeepStack-VEGF ses som en högt tränad mönsterigenkännare för en central läkningssignal i kroppen. Istället för att vänta på mödosamma experiment kan forskare nu mata in proteinsekvenser i modellen för att snabbt uppskatta om de beter sig som VEGF. Denna kapacitet kan hjälpa till att begränsa kandidater för nya cancer- eller ögonsjukdomsbehandlingar, vägleda designen av anti-angiogena läkemedel och stödja bredare proteinforskning. Även om varje lovande förutsägelse fortfarande kräver laboratoriebekräftelse, flyttar verktyg som DeepStack-VEGF en del av upptäcktsarbetet från bänken till datorn, vilket potentiellt gör framtida terapier snabbare och billigare att utveckla.
Citering: Ali, F., Khalid, M., Algarni, A. et al. DeepStackVEGF a stacking ensemble deep learning framework for vascular endothelial growth factor prediction. Sci Rep 16, 13035 (2026). https://doi.org/10.1038/s41598-026-40134-0
Nyckelord: VEGF-prediktion, angiogenes, djupinlärning inom biologi, protein-språkmodeller, läkemedelsupptäckt