Clear Sky Science · pl
DeepStackVEGF — metoda ensemble stacking w głębokim uczeniu do przewidywania czynnika wzrostu śródbłonka naczyniowego
Dlaczego przewidywanie sygnału gojenia się ma znaczenie
Nasze ciało zależy od białka zwanego czynnikiem wzrostu śródbłonka naczyniowego, czyli VEGF, aby tworzyć nowe naczynia krwionośne. Ten sygnał jest niezbędny do gojenia ran, naprawy kości i prawidłowego rozwoju — raka jednak przechwytuje ten mechanizm, by odżywiać guzy i rozprzestrzeniać się po organizmie. Mierzenie i charakterystyka VEGF w laboratorium jest czasochłonne i kosztowne. W tym badaniu przedstawiono DeepStack-VEGF, wydajny model komputerowy, który potrafi szybko przewidzieć, czy dane białko zachowuje się jak VEGF, co może przyspieszyć odkrywanie leków i medycynę spersonalizowaną.
Z ławy laboratoryjnej na laptop
Tradycyjnie badacze wykorzystują zaawansowane techniki, takie jak krystalografia, NMR czy barwienia tkankowe, aby badać VEGF. Metody te ujawniają strukturę i lokalizację cząsteczki, ale wymagają wyspecjalizowanego sprzętu i czasu. Równocześnie ogromne publiczne bazy danych zawierają dziś miliony sekwencji białek, których funkcje są tylko częściowo poznane. Autorzy dostrzegli szansę: zamiast najpierw hodować kryształy czy przeprowadzać złożone eksperymenty, dlaczego nie pozwolić komputerom przesiewać sekwencji białkowych i wskazywać tych, które prawdopodobnie działają jak VEGF? DeepStack-VEGF został zaprojektowany jako szybkie, skalowalne narzędzie do robienia właśnie tego — przekształcania surowych liter białkowych w sensowne predykcje.
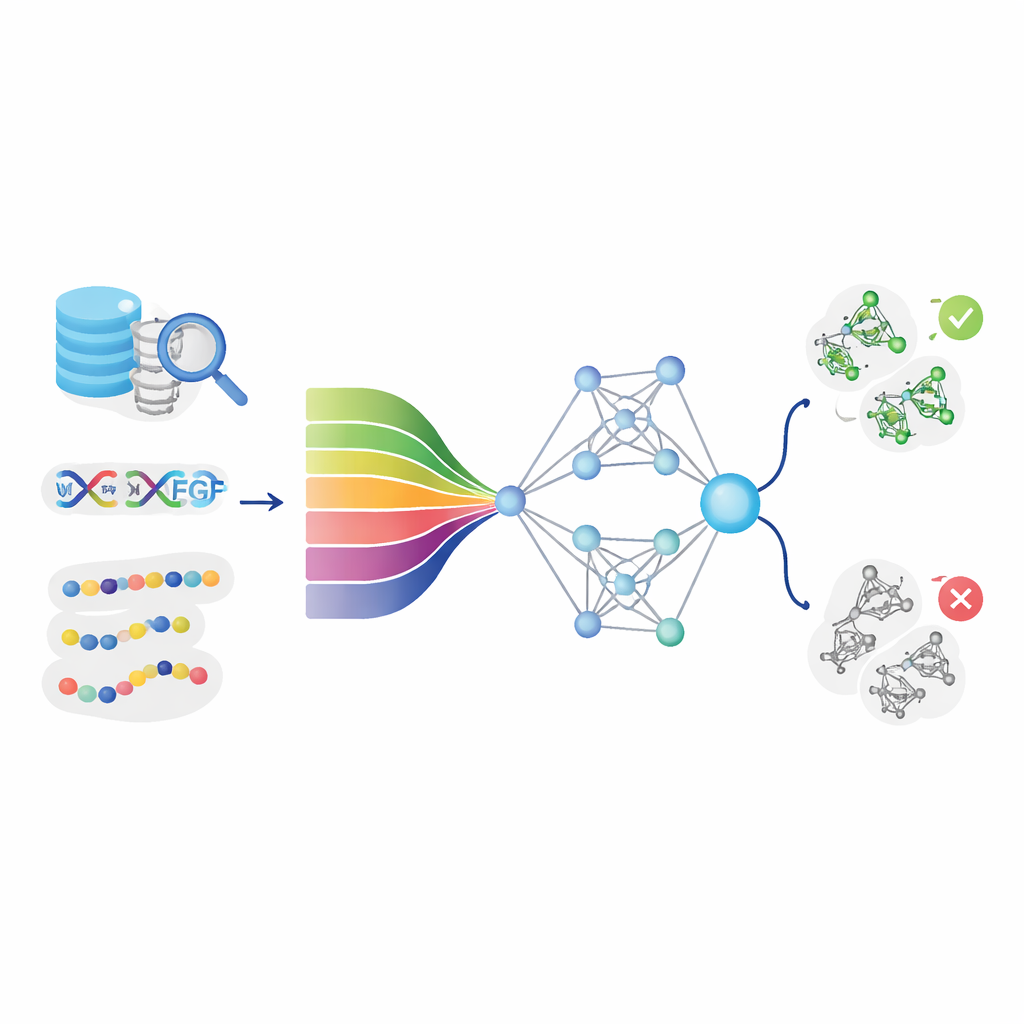
Nauka komputerów czytania „języka” białek
Główny pomysł DeepStack-VEGF polega na tym, że sekwencja białka zawiera ukryte wzorce wskazujące na jego zachowanie. Zespół zebrał tysiące białek VEGF i nie-VEGF z głównych baz danych i starannie oczyścił dane, aby uniknąć niemalowych duplikatów. Następnie opisali każde białko z wielu perspektyw. Niektóre cechy odzwierciedlały podstawowe właściwości chemiczne, takie jak hydrofobowość czy ładunek w różnych pozycjach. Inne podsumowywały częstość występowania określonych par lub trójek aminokwasów albo przewidywały, jak łańcuch będzie się składał w helisy i beta-kartki. Co istotne, model wykorzystał także nowoczesne „modele języka białkowego” — systemy sztucznej inteligencji, które podobnie jak narzędzia językowe dla tekstu uczą się głębokich wzorców z milionów naturalnych sekwencji białkowych i przekształcają każdą z nich w bogaty numeryczny odcisk palca.
Łączenie różnych punktów widzenia w jedną decyzję
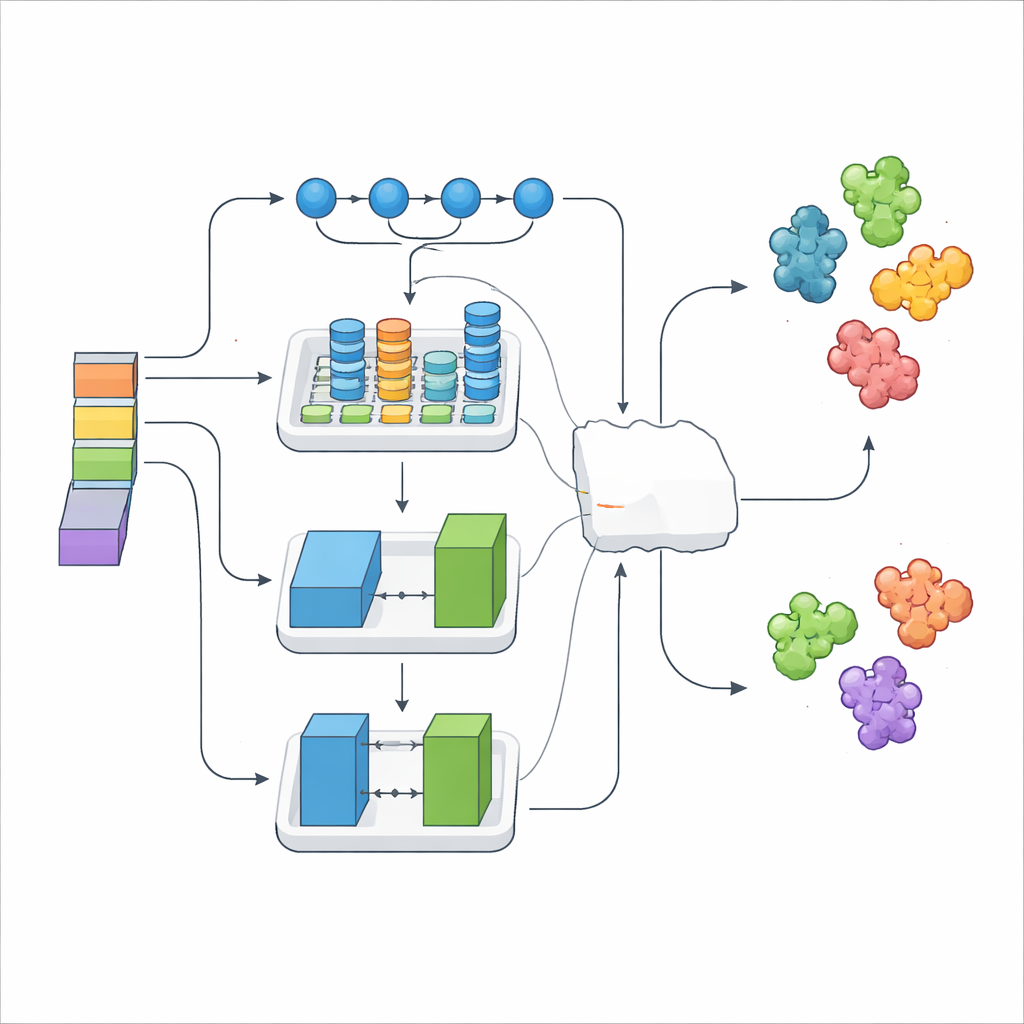
Proste zestawienie tysięcy cech liczbowych może wprowadzać szum, dlatego badacze zastosowali metodę selekcji utrzymującą tylko najbardziej informacyjne sygnały. Te wyselekcjonowane cechy przekazano następnie do trzech różnych modułów głębokiego uczenia, z których każdy miał odrębną specjalizację. Jeden model świetnie wychwytywał wzorce rozciągające się na długich odległościach w sekwencji, inny uchwycił lokalne motywy strukturalne i ich relacje, a trzeci używał konfiguracji generator–krytyk podobnej do gry, by wzbogacić i uregularyzować dane. Na szczycie tych modeli warstwa „meta” nauczyła się, jak najlepiej łączyć ich wyniki, tworząc zespół DeepStack-VEGF. Ta wielowarstwowa strategia przypomina panel ekspertów, z których każdy wnosi inną wiedzę przed podjęciem wspólnego rozstrzygnięcia.
Sprawdzanie dokładności i otwieranie czarnej skrzynki
Aby przetestować system, autorzy zastosowali rygorystyczną walidację krzyżową i niezależny zbiór testowy. W różnych miarach dokładności DeepStack-VEGF przewyższał każdy z jego komponentów oraz dwie wcześniejsze, najlepsze w swojej klasie metody przewidywania VEGF. Ostateczna wersja poprawnie klasyfikowała białka podobne do VEGF w zdecydowanie ponad dziewięciu na dziesięć przypadków, przy mniejszej liczbie fałszywych alarmów niż konkurencyjne podejścia. Zespół zastosował też metodę wyjaśniania, która szacuje, jak bardzo każda cecha wejściowa przesuwa decyzję w stronę „VEGF” lub „nie VEGF”. Analiza ta wykazała, że najwięcej mocy predykcyjnej dostarczały wyuczone odciski z modeli języka białkowego, podczas gdy tradycyjne cechy oparte na chemii i strukturze dodawały szczegółów i stabilności.
Co to oznacza dla medycyny i badań
Dla czytelników niebędących specjalistami DeepStack-VEGF można uznać za wysoko wyszkolony rozpoznawacz wzorców dla kluczowego sygnału gojenia w organizmie. Zamiast czekać na mozolne eksperymenty, naukowcy mogą teraz wprowadzać sekwencje białkowe do modelu, aby szybko oszacować, czy zachowują się jak VEGF. Ta możliwość może pomóc zawęzić kandydatów do nowych terapii przeciwnowotworowych lub na choroby oczu, ukierunkować projektowanie leków antyangiogennych i wspierać szersze badania nad białkami. Chociaż każda obiecująca predykcja nadal wymaga potwierdzenia w laboratorium, narzędzia takie jak DeepStack-VEGF przenoszą część pracy odkrywczej z ławy laboratoryjnej na komputer, co może przyspieszyć i obniżyć koszty rozwijania przyszłych terapii.
Cytowanie: Ali, F., Khalid, M., Algarni, A. et al. DeepStackVEGF a stacking ensemble deep learning framework for vascular endothelial growth factor prediction. Sci Rep 16, 13035 (2026). https://doi.org/10.1038/s41598-026-40134-0
Słowa kluczowe: predykcja VEGF, angiogeneza, głębokie uczenie w biologii, modele języka białkowego, odkrywanie leków