Clear Sky Science · es
DeepStackVEGF, un marco de aprendizaje profundo tipo stacking para la predicción del factor de crecimiento endotelial vascular
Por qué importa predecir una señal de curación
Nuestros cuerpos dependen de una proteína llamada factor de crecimiento endotelial vascular, o VEGF, para formar nuevos vasos sanguíneos. Esta señal es esencial para la cicatrización de heridas, la reparación ósea y el desarrollo normal, pero los cánceres también la secuestran para abastecer tumores y diseminarse por el organismo. Medir y caracterizar el VEGF en el laboratorio es lento y costoso. Este estudio presenta DeepStack-VEGF, un potente modelo informático capaz de predecir rápidamente si una proteína dada se comporta como VEGF, lo que podría acelerar el descubrimiento de fármacos y la medicina de precisión.
Del banco de laboratorio al portátil
Tradicionalmente, los investigadores emplean técnicas sofisticadas como cristalografía, RMN y tinción de tejidos para estudiar el VEGF. Estos métodos revelan la estructura y la localización de la molécula, pero requieren equipamiento especializado y tiempo. Al mismo tiempo, gigantescas bases de datos públicas contienen ahora millones de secuencias proteicas cuya función solo se conoce parcialmente. Los autores vieron una oportunidad: en lugar de primero crecer cristales o realizar experimentos complejos, ¿por qué no dejar que los ordenadores examinen las secuencias proteicas y señalen aquellas que probablemente actúen como VEGF? DeepStack-VEGF fue diseñado como una herramienta rápida y escalable para hacer exactamente eso: convertir letras proteicas en predicciones significativas.
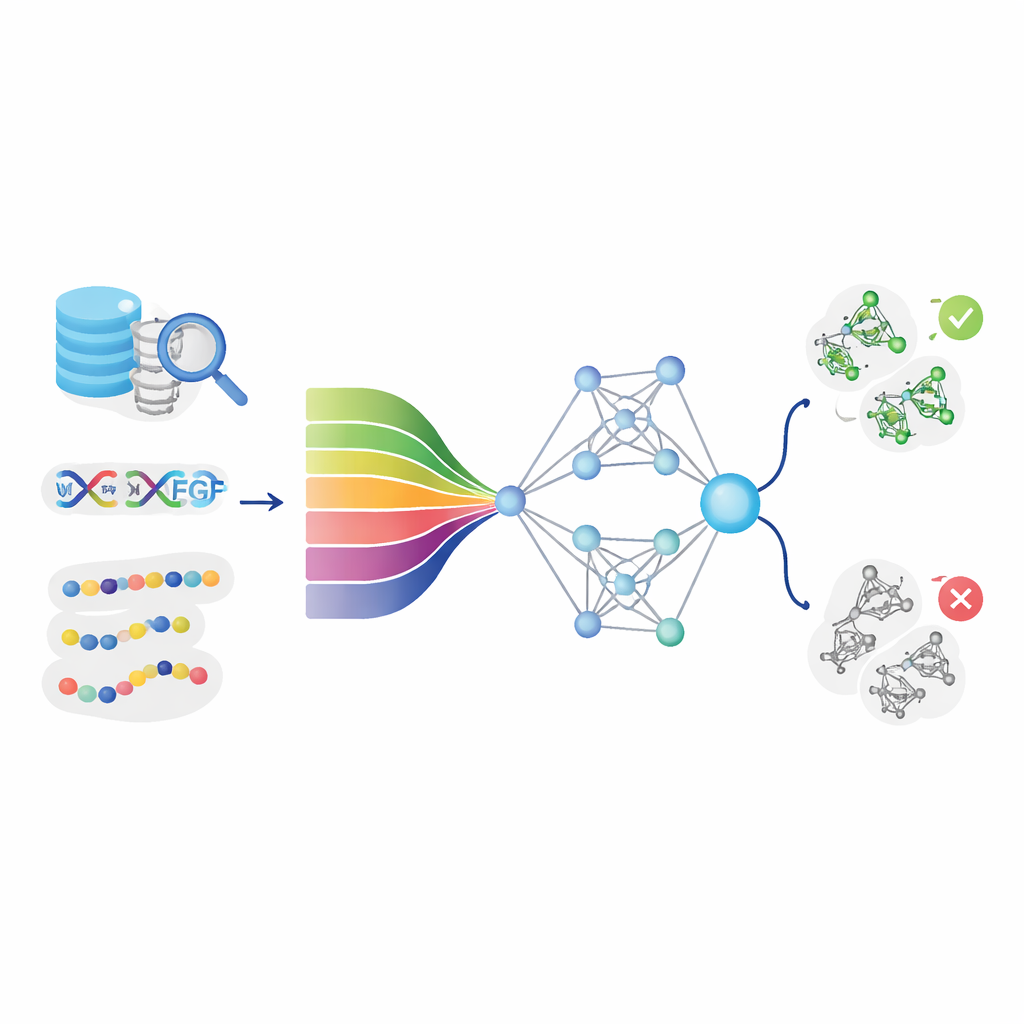
Enseñar a los ordenadores a leer el “lenguaje” de las proteínas
La idea central de DeepStack-VEGF es que la secuencia de una proteína contiene patrones ocultos que indican su comportamiento. El equipo recopiló miles de proteínas VEGF y no-VEGF de bases de datos principales y limpió cuidadosamente los datos para evitar casi duplicados. Después describieron cada proteína desde múltiples ángulos. Algunas características capturaron química básica, como la hidrofobicidad o la carga en distintas posiciones. Otras resumieron la frecuencia de ciertos pares o tripletes de bloques constructores, o cómo es probable que la cadena se pliegue en hélices y láminas. De forma crucial, el modelo también utilizó modernos “modelos de lenguaje de proteínas”: sistemas de inteligencia artificial que, como las herramientas de lenguaje para texto, aprenden patrones profundos a partir de millones de secuencias naturales de proteínas y convierten cada una en una rica huella numérica.
Unir muchos puntos de vista en una sola decisión
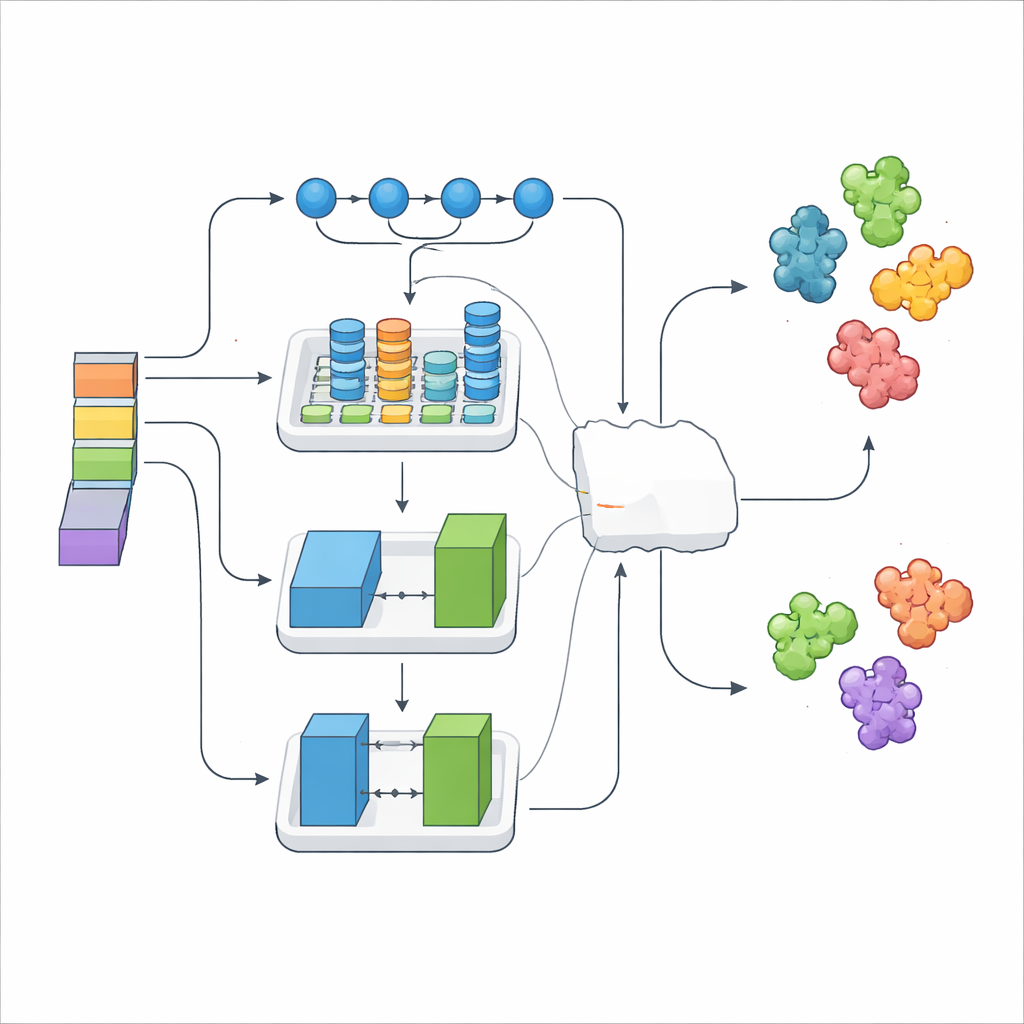
Apilar simplemente miles de características numéricas puede introducir ruido, por lo que los investigadores emplearon un método de selección que conserva solo las señales más informativas. Estas características refinadas se alimentaron a tres módulos distintos de aprendizaje profundo, cada uno con una especialidad diferente. Un modelo destacó en trazar patrones de largo alcance a lo largo de la secuencia, otro capturó motivos estructurales locales y sus relaciones, y un tercero utilizó una configuración tipo generador–crítico para enriquecer y regularizar los datos. Encima de estos, una capa “meta” aprendió a combinar mejor sus salidas, formando el ensamblaje DeepStack-VEGF. Esta estrategia por capas refleja cómo un panel de expertos, cada uno con distinto entrenamiento, podría opinar antes de llegar a una conclusión conjunta.
Comprobar la exactitud y abrir la caja negra
Para evaluar su sistema, los autores usaron una validación cruzada rigurosa y un conjunto de prueba independiente. En múltiples medidas de precisión, DeepStack-VEGF superó a cada uno de sus modelos componentes y a dos predictores de VEGF de vanguardia anteriores. Su versión final clasificó correctamente proteínas de tipo VEGF en mucho más de nueve de cada diez casos, con menos falsas alarmas que los enfoques competidores. El equipo también aplicó un método de explicación que estima cuánto empuja cada característica de entrada una decisión hacia “VEGF” o “no VEGF”. Este análisis mostró que las huellas aprendidas por los modelos de lenguaje de proteínas aportaron la mayor parte del poder predictivo, mientras que las características tradicionales basadas en química y estructura añadieron detalle fino y estabilidad.
Qué significa esto para la medicina y la investigación
Para no especialistas, DeepStack-VEGF puede verse como un reconocedor de patrones altamente entrenado para una señal clave de curación en el organismo. En lugar de esperar experimentos laboriosos, los científicos ahora pueden introducir secuencias proteicas en el modelo para estimar rápidamente si se comportan como VEGF. Esta capacidad puede ayudar a reducir la lista de candidatos para nuevos tratamientos contra el cáncer o enfermedades oculares, guiar el diseño de fármacos antiangiogénicos y respaldar investigaciones proteicas más amplias. Aunque cualquier predicción prometedora aún necesita confirmación en laboratorio, herramientas como DeepStack-VEGF trasladan parte del trabajo de descubrimiento del banco al ordenador, potencialmente haciendo que el desarrollo de futuras terapias sea más rápido y barato.
Cita: Ali, F., Khalid, M., Algarni, A. et al. DeepStackVEGF a stacking ensemble deep learning framework for vascular endothelial growth factor prediction. Sci Rep 16, 13035 (2026). https://doi.org/10.1038/s41598-026-40134-0
Palabras clave: predicción de VEGF, angiogénesis, aprendizaje profundo en biología, modelos de lenguaje de proteínas, descubrimiento de fármacos