Clear Sky Science · de
DeepStackVEGF ein Stacking-Ensemble-Deep-Learning-Framework zur Vorhersage des vaskulären endothelialen Wachstumsfaktors
Warum die Vorhersage eines Heilungssignals wichtig ist
Unser Körper ist auf ein Protein angewiesen, das als vaskulärer endothelialer Wachstumsfaktor oder VEGF bezeichnet wird, um neue Blutgefäße zu bilden. Dieses Signal ist essenziell für die Wundheilung, die Knochenreparatur und die normale Entwicklung – gleichzeitig kapern Krebszellen es, um Tumore zu versorgen und sich im Körper auszubreiten. Das Messen und Charakterisieren von VEGF im Labor ist zeitaufwändig und teuer. Diese Studie stellt DeepStack-VEGF vor, ein leistungsfähiges Computermodell, das schnell vorhersagen kann, ob ein bestimmtes Protein sich wie VEGF verhält, und so die Wirkstoffforschung und Präzisionsmedizin beschleunigen könnte.
Vom Laborbank zur Laptop
Traditionell verwenden Forschende aufwendige Techniken wie Kristallographie, NMR und Gewebefärbung, um VEGF zu untersuchen. Diese Methoden zeigen Struktur und Lokalisation des Moleküls, erfordern jedoch spezialisiertes Gerät und Zeit. Gleichzeitig enthalten öffentliche Datenbanken inzwischen Millionen von Proteinsequenzen, deren Funktionen nur teilweise bekannt sind. Die Autor:innen erkannten eine Chance: Anstatt zunächst Kristalle zu züchten oder komplexe Experimente durchzuführen, könnten Computer Proteinsequenzen durchsuchen und solche markieren, die wahrscheinlich wie VEGF wirken. DeepStack-VEGF wurde als schnelles, skalierbares Werkzeug entwickelt, das genau dies tut – rohe Proteinbuchstaben in aussagekräftige Vorhersagen verwandelt.
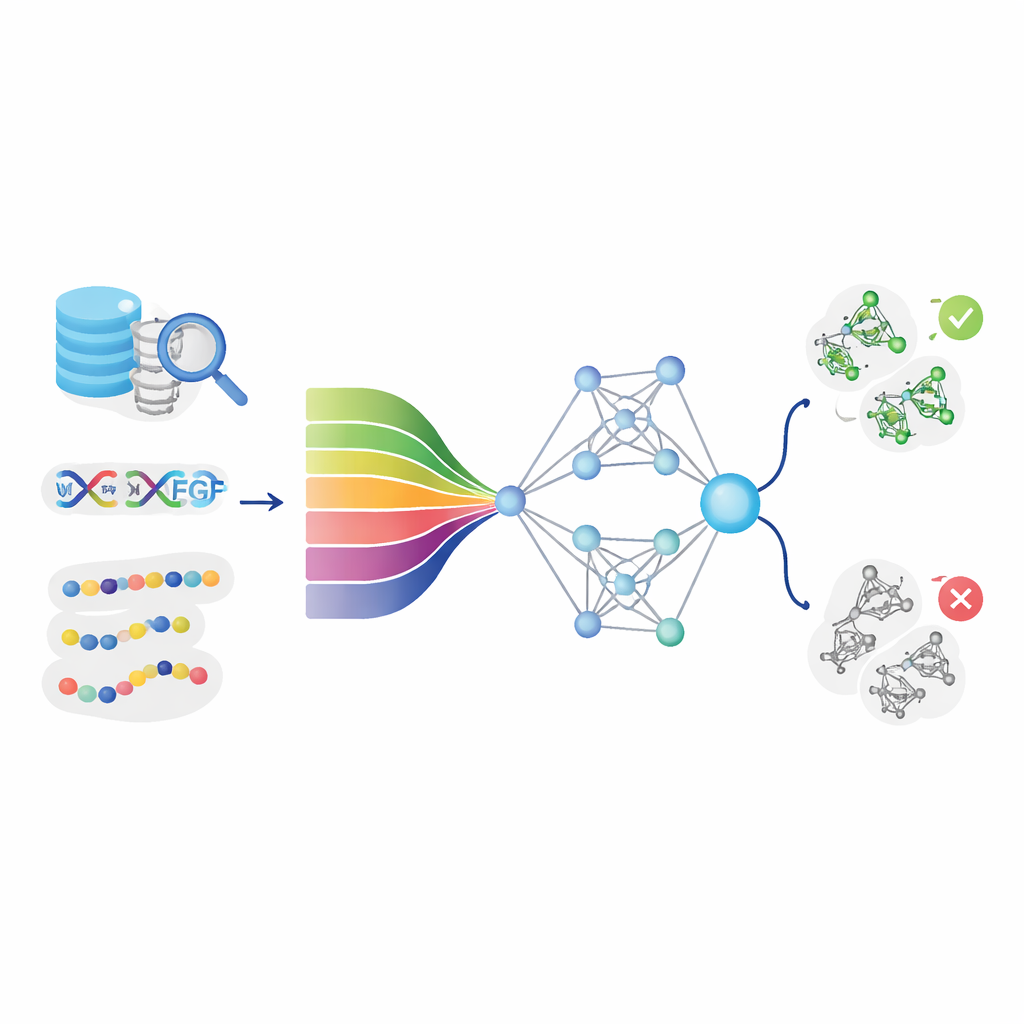
Computern das Lesen der Protein-„Sprache“ beibringen
Die Kernidee von DeepStack-VEGF ist, dass eine Proteinsequenz verborgene Muster enthält, die auf ihr Verhalten hinweisen. Das Team sammelte Tausende von VEGF- und Nicht-VEGF-Proteinen aus großen Datenbanken und bereinigte die Daten sorgfältig, um nahezu identische Einträge zu vermeiden. Anschließend beschrieben sie jedes Protein aus vielen Blickwinkeln. Einige Merkmale erfassten grundlegende chemische Eigenschaften, etwa wie hydrophob oder geladen bestimmte Positionen sind. Andere fassten zusammen, wie häufig bestimmte Paare oder Tripel von Bausteinen vorkommen oder wie sich die Kette voraussichtlich zu Helices und Faltblättern formt. Entscheidend nutzte das Modell außerdem moderne „Protein-Sprachmodelle“ – KI-Systeme, die ähnlich wie Sprachwerkzeuge für Text tiefe Muster aus Millionen natürlicher Proteinsequenzen lernen und jede Sequenz in einen reichen numerischen Fingerabdruck übersetzen.
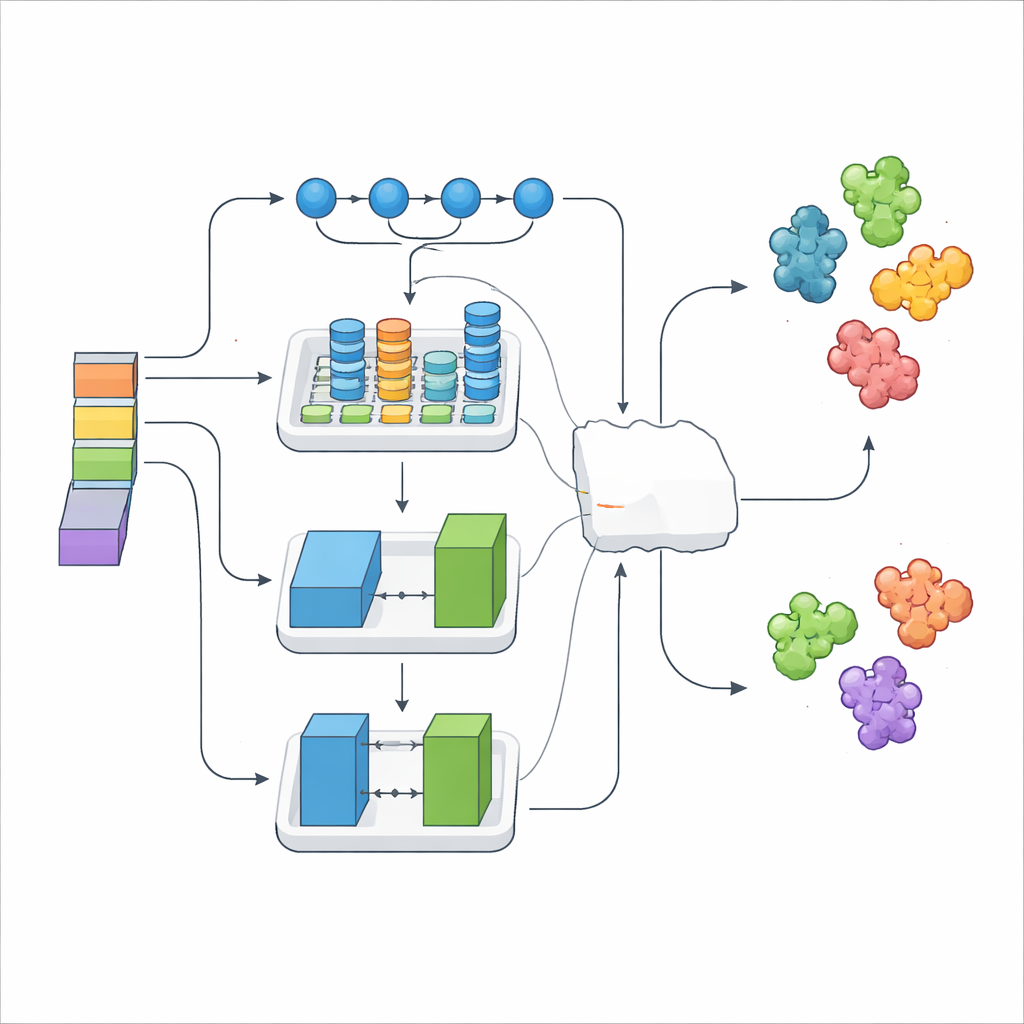
Viele Blickwinkel zu einer Entscheidung vereinen
Das bloße Stapeln von Tausenden numerischer Merkmale kann Rauschen einführen, daher verwendeten die Forschenden eine Selektionsmethode, die nur die informativsten Signale behält. Diese verfeinerten Merkmale wurden dann in drei verschiedene Deep-Learning-Module eingespeist, die jeweils eine besondere Stärke hatten. Ein Modell zeichnete sich dadurch aus, langreichweitige Muster entlang der Sequenz zu verfolgen, ein anderes erfasste lokale Strukturmotive und deren Beziehungen, und ein drittes nutzte ein spielähnliches Generator–Kritiker-Setup, um die Daten zu bereichern und zu regularisieren. Darüber lernte eine Meta-Schicht, wie sich deren Ausgaben am besten kombinieren lassen — das DeepStack-VEGF-Ensemble. Diese geschichtete Strategie spiegelt wider, wie ein Expertengremium mit unterschiedlicher Ausbildung vor einer gemeinsamen Entscheidung abwägen würde.
Genauigkeit prüfen und die Blackbox öffnen
Um ihr System zu testen, nutzten die Autor:innen rigorose Kreuzvalidierung und einen unabhängigen Testsatz. In mehreren Genauigkeitsmaßen übertraf DeepStack-VEGF jedes seiner Komponentenmodelle sowie zwei frühere State-of-the-Art-VEGF-Prädiktoren. Die finale Version klassifizierte VEGF-ähnliche Proteine in weit über neun von zehn Fällen korrekt und produzierte weniger Fehlalarme als konkurrierende Ansätze. Das Team wandte außerdem eine Erklärungsmethode an, die abschätzt, wie stark jedes Eingangsmerkmal eine Entscheidung Richtung „VEGF“ oder „kein VEGF“ treibt. Diese Analyse zeigte, dass die gelernten Protein-Sprach-Fingerabdrücke den Großteil der Vorhersagekraft lieferten, während traditionelle chemie- und strukturbasierte Merkmale feinkörnige Details und Stabilität beitrugen.
Was das für Medizin und Forschung bedeutet
Für Nicht-Spezialist:innen lässt sich DeepStack-VEGF als hochtrainierten Mustererkenner für ein zentrales Heilungssignal im Körper ansehen. Anstatt auf mühsame Experimente zu warten, können Wissenschaftler:innen jetzt Proteinsequenzen in das Modell einspeisen, um schnell abzuschätzen, ob sie sich wie VEGF verhalten. Diese Fähigkeit kann helfen, Kandidat:innen für neue Krebs- oder Augenerkrankungsbehandlungen einzuschränken, das Design anti-angiogener Wirkstoffe zu leiten und allgemeine Proteinforschung zu unterstützen. Während vielversprechende Vorhersagen weiterhin im Labor bestätigt werden müssen, verlagern Werkzeuge wie DeepStack-VEGF Teile der Entdeckungsarbeit vom Labor auf den Computer und könnten so die Entwicklung künftiger Therapien schneller und kostengünstiger machen.
Zitation: Ali, F., Khalid, M., Algarni, A. et al. DeepStackVEGF a stacking ensemble deep learning framework for vascular endothelial growth factor prediction. Sci Rep 16, 13035 (2026). https://doi.org/10.1038/s41598-026-40134-0
Schlüsselwörter: VEGF-Vorhersage, Angiogenese, Deep Learning in der Biologie, Protein-Sprachmodelle, Wirkstoffforschung