Clear Sky Science · sv
MFF som knoppas från mitokondrier reglerar melanosomstorlek och mognad
Varför cellernas färgskapande maskineri spelar roll
Vår hud, hår och ögon får sin färg från små pigmentfabriker inne i cellerna som kallas melanosomer. Att hålla dessa strukturer i rätt storlek och i fungerande skick är viktigt inte bara för utseendet, utan också för att skydda våra vävnader mot solljus. Denna studie avslöjar en överraskande aktör i hur melanosomer växer, delar sig och mognar: ett protein mest känt för att forma mitokondrierna, cellens kraftverk. Genom att visa att detta protein också skulpterar melanosomer kopplar forskarna energiproducerande organeller till pigmentproducerande, vilket ger nya ledtrådar till hur färg regleras i hälsa och sjukdom.
En ny uppgift för en mitokondriell hjälpare
Melanosomer är specialiserade fack som tillverkar och lagrar melanin, det mörka pigment som skyddar celler mot ultraviolett skada. När de utvecklas passerar melanosomerna flera stadier och fylls gradvis med pigment innan de överförs till närliggande hudceller. Under denna process omformas deras membran ständigt—de sträcks ut till tubuli, knoppas av små delar och ibland smälter samman. Den maskineri som driver denna omformning har bara varit delvis förstådd. Författarna koncentrerade sig på ett protein kallat mitochondrial fission factor (MFF), känt för att hjälpa mitokondrier att dela sig. Till sin förvåning fann de MFF inte bara på mitokondrier utan också på melanosomer, särskilt vid platser där dessa pigmentgranuler smalnar av och verkar redo att dela sig.
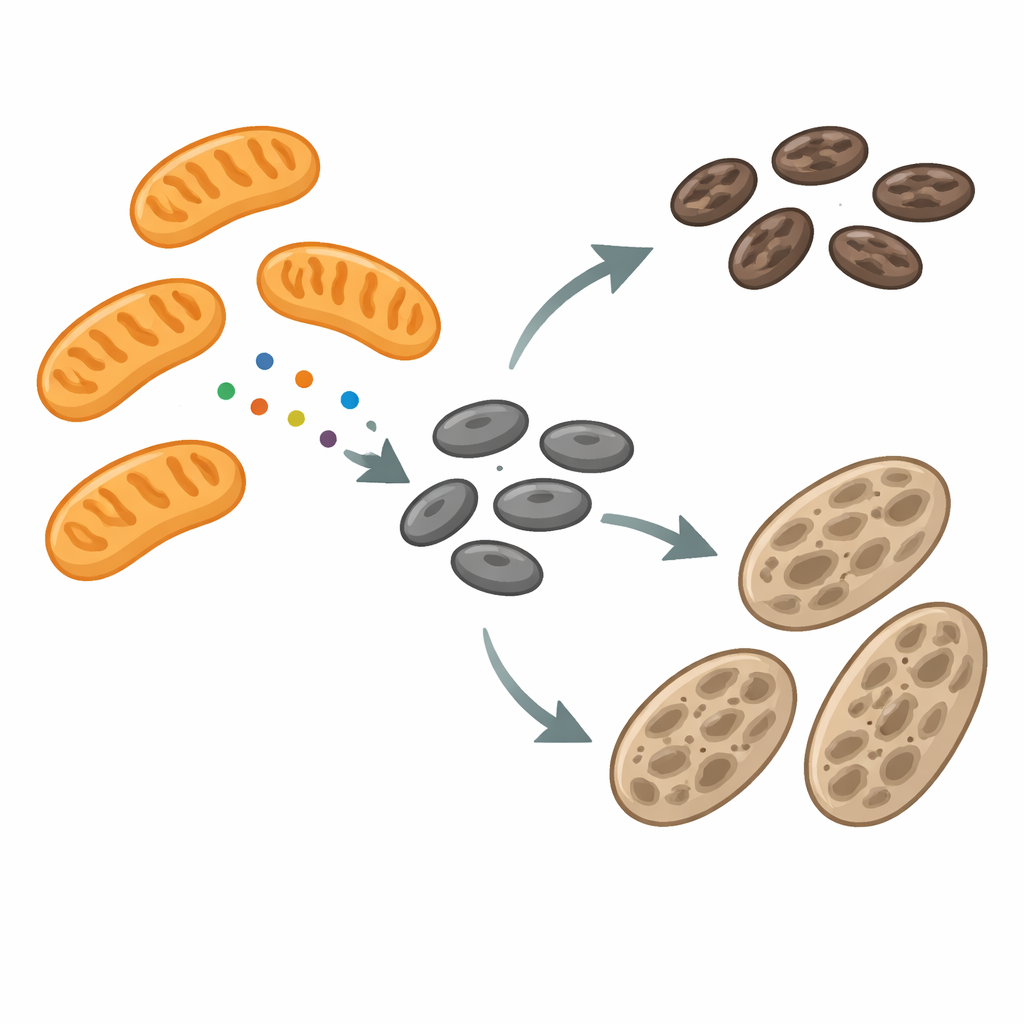
När pigmenteringen stannar av förändras kontakter och signaler
För att undersöka hur mitokondrier och melanosomer kommunicerar jämförde teamet normala pigmentproducerande musceller med albino-celler som inte kan bilda melanin på grund av en defekt i tyrosinasgenen. Albino-cellerna ackumulerade många omogna melanosomer och visade tätare fysiska kontakter mellan melanosomer och mitokondrier. RNA-sekvensering och proteinanalyser avslöjade att i dessa albino-celler var gener och proteiner kopplade till mitokondrier uppreglerade, inklusive MFF som sitter på det yttre mitokondriella membranet. Mitokondriernas form såg dock i stort sett normal ut, medan melanosomerna var både större och mer dynamiska och genomgick frekventa fissions- och fusionshändelser. Detta mönster antydde att MFF kan ha omdirigerats från mitokondrier mot melanosomer, där det kan påverka hur dessa pigmentorganelle delar sig och mognar.
MFF förflyttar sig till melanosomer och styr deras uppdelning
Med hjälp av högupplöst mikroskopi och immunogold-elektronmikroskopi spårade forskarna MFF direkt på ytan av melanosomer i alla stadier av deras livscykel. Tidsförlöpande avbildning fångade till och med MFF som lämnade mitokondrier som små punkter och rörde sig över på LAMP1- och LysoTracker-markerade melanosomer. På dessa platser smalnade melanosomernas membran ofta av och knoppade, vilket bildade tubuli och vesiklar. Kvantitativ analys visade att ungefär en fjärdedel av synliga melanosom-fissionsregioner var dekorerade med MFF, vilket tyder på att det markerar en viktig kategori av delningshändelser. När forskarna minskade MFF-nivåerna i pigmentceller blev tidiga melanosomer onormalt förstorade, ofta som hybridstrukturer med egenskaper från både omogna och mer avancerade stadier. Dessa svällda organeller delade melanin mer omfattande med tidiga markörer, och levande avbildning visade färre lyckade fissionshändelser, vilket understryker att MFF behövs för korrekt delning och mognad av melanosomer.
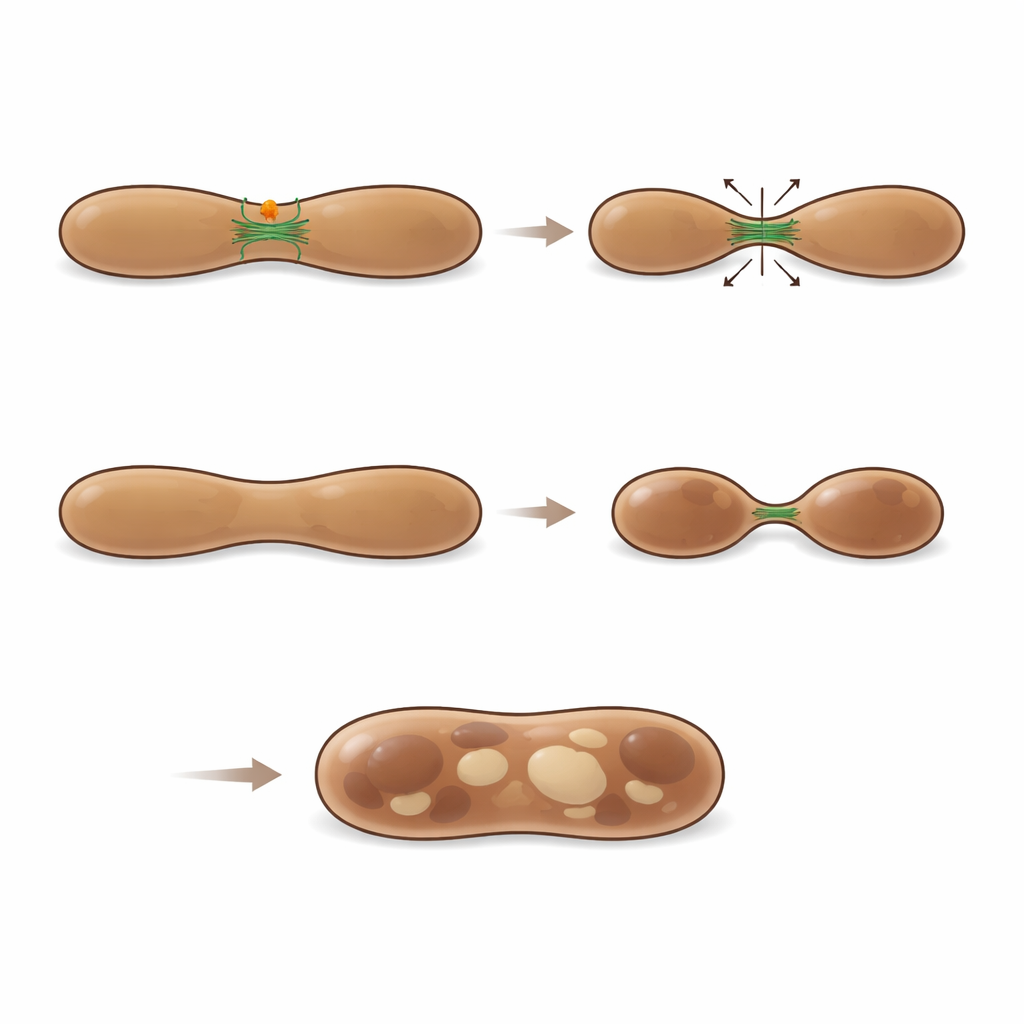
Balans mellan nedbrytning och uppbyggnad med aktinfilament
MFF:s vanliga partner vid mitokondriedelning är ett annat protein, DRP1. Men i melanosomer överlappade DRP1 och MFF sällan, och att tysta respektive protein gav väldigt olika konsekvenser. Förlust av DRP1 dämpade främst det genetiska programmet som driver pigmentproduktionen. I kontrast orsakade förlust av MFF förstorade tidiga melanosomer och utlöste en stark ökning i gener och proteiner kopplade till lysosomer—cellens återvinningscentraler—och till katabola enzymer såsom kathepsin B. Dessa enzymer koncentrerades inne i melanosomer, vilket gjorde dem mer sura och mer benägna att bryta ner sitt eget pigmentmaskineri. När kathepsin B också blev tystad svällde melanosomerna i MFF-bristceller ytterligare och samlades i stora antal, vilket visar att förstärkt intern nedbrytning normalt tjänar som en reservmekanism för att förhindra ansamling av dysfunktionella, förstorade pigmentgranuler.
Hur cellens skelett hjälper till att skära pigmentgranuler
För att förstå hur MFF fysiskt hjälper melanosomer att dela sig kartlade författarna vilka proteiner som binder till det. De fann många regulatorer av aktin-cytoskelettet, inklusive komponenter i WASH-komplexet och ARP2/3, maskineriet som initierar bildandet av aktinfilament. Avbildning visade aktinfilament som samlades vid melanosomens halsar där MFF-punkter satt, och bildade broar över de förträngda regionerna mellan två knoppande fack. När viktiga ARP2/3-subenheter tystades förstördes tidiga melanosomer på ungefär samma sätt som vid förlust av MFF, vilket indikerar att aktin-driven filamentbildning är nödvändig för korrekt delning. Hämning av ARP2/3-aktivitet utplånade också den melanosomförstorande effekten av MFF-förlust, vilket kopplar MFF-funktionen starkt till aktindynamik snarare än till DRP1. Tillsammans visar dessa fynd att MFF rekryterar eller stabiliserar en aktinbaserad fissionsmaskin vid melanosomer, vilket möjliggör att de kan avsöndra onödiga komponenter och mogna till fullgott pigmenterade, korrekt stora organeller.
Vad detta betyder för pigmentstörningar
Studien visar att MFF, länge sett som en specialist i mitokondriedelning, också verkar utanför mitokondrier för att reglera storlek, form och mognad hos melanosomer genom aktin-driven fission. När MFF saknas kan inte tidiga pigmentgranuler dela sig korrekt, de växer för stora och blir i allt högre grad liknande nedbrytande kompartiment, vilket får cellen att öka deras nedbrytning. Dessa insikter hjälper till att förklara hur jättestora melanosomer uppstår i vissa ärftliga former av albinism och relaterade tillstånd, och de framhäver MFF och dess aktinpartners som potentiella mål för att modulera pigmentering eller förstå hur pigmentceller fungerar fel i sjukdom.
Citering: Magalhães Rebelo, A.P., Maracani, A., Greco, S. et al. MFF budding from mitochondria regulates melanosome size and maturation. Nat Commun 17, 3932 (2026). https://doi.org/10.1038/s41467-026-70572-3
Nyckelord: melanosomer, mitokondrier, MFF-protein, pigmentering, aktin-cytoskelett