Clear Sky Science · nl
MFF dat uit mitochondriën uitsnijdt reguleert melanosoomgrootte en -rijping
Waarom de kleurproducerende machines van cellen ertoe doen
Onze huid, haar en ogen krijgen hun kleur door kleine pigmentfabriekjes in cellen, melanosomen genoemd. Het op de juiste grootte houden en goed laten functioneren van deze structuren is van wezenlijk belang, niet alleen voor uiterlijk, maar ook voor de bescherming van weefsels tegen zonlicht. Deze studie onthult een verrassende speler in hoe melanosomen groeien, zich delen en rijpen: een eiwit dat vooral bekend is vanwege het vormen van mitochondriën, de energiecentrales van de cel. Door aan te tonen dat dit eiwit ook melanosomen vormt, leggen de onderzoekers een verband tussen energieproducerende organellen en pigmentproducerende organellen en bieden ze nieuwe aanwijzingen voor hoe kleur in gezondheid en ziekte wordt gereguleerd.
Een nieuwe taak voor een mitochondriale helper
Melanosomen zijn gespecialiseerde compartimenten die melanine maken en opslaan, het donkere pigment dat cellen beschermt tegen ultraviolet licht. Tijdens hun ontwikkeling doorlopen melanosomen meerdere stadia en vullen ze zich geleidelijk met pigment voordat ze aan naburige huidcellen worden doorgegeven. Gedurende dit traject worden hun membranen voortdurend heringericht—uitrekken tot tubuli, afknijpen van kleine stukjes en soms samensmelten. De machinerie die deze herinrichting aandrijft was slechts deels bekend. De auteurs richtten zich op een eiwit genaamd mitochondrial fission factor (MFF), dat bekendstaat om het helpen van mitochondriale deling. Tot hun verbazing vonden ze MFF niet alleen op mitochondriën, maar ook op melanosomen, vooral op plekken waar deze pigmentgranules vernauwen en klaar lijken om te splitsen.
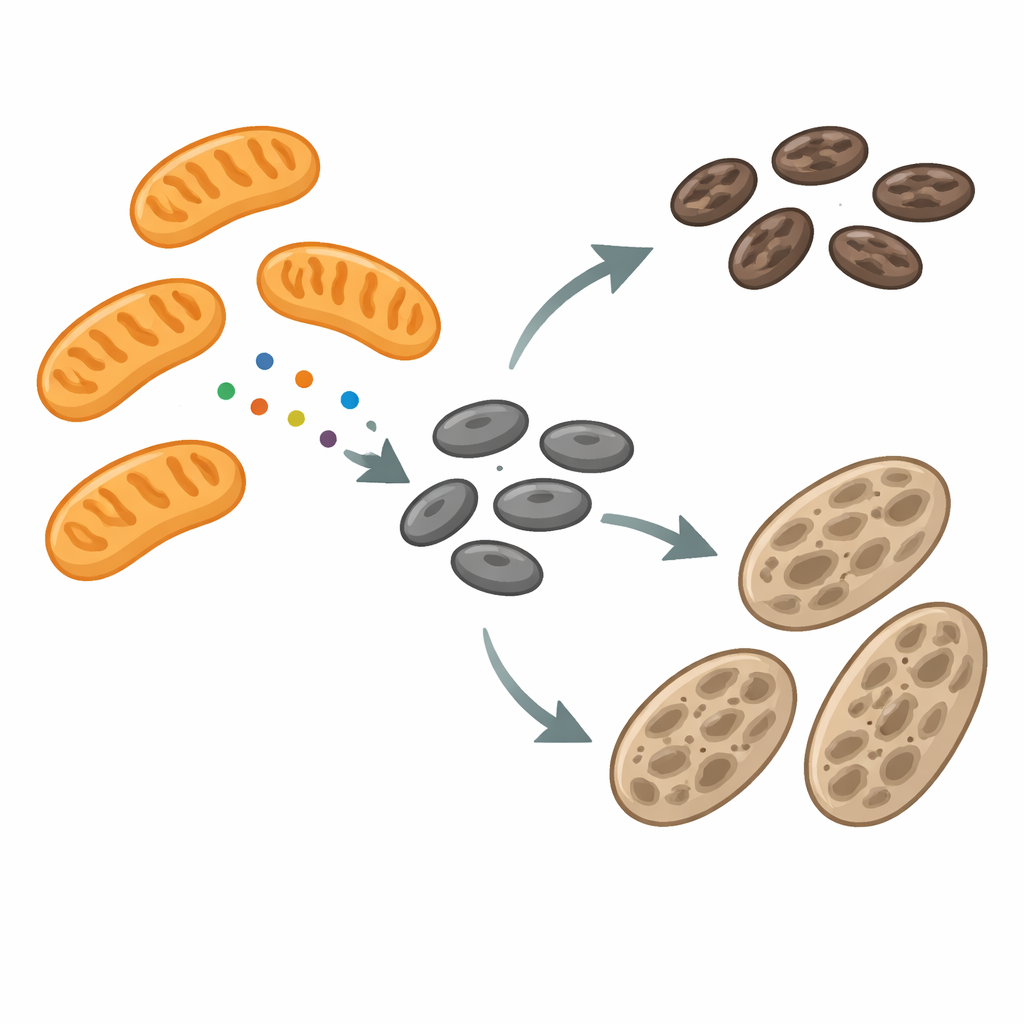
Wanneer pigment stokt, veranderen contacten en signalen
Om te onderzoeken hoe mitochondriën en melanosomen communiceren, vergeleek het team normale pigmentproducerende muizencellen met albino cellen die geen melanine kunnen maken door een defect in het tyrosinase-gen. De albino cellen stapelden veel onrijpe melanosomen op en vertoonden vaker fysieke contacten tussen melanosomen en mitochondriën. RNA-sequencing en proteïneanalyse toonden aan dat in deze albino cellen genen en eiwitten die met mitochondriën samenhangen verhoogd waren, waaronder MFF op het buitenmembraan van mitochondriën. Toch zag de mitochondriale vorm er grotendeels normaal uit, terwijl melanosomen zowel groter als dynamischer waren, met frequente fission- en fusiegebeurtenissen. Dit patroon suggereerde dat MFF mogelijk van mitochondriën weg wordt hergebruikt naar melanosomen, waar het kan beïnvloeden hoe deze pigmentorganellen splitsen en rijpen.
MFF reist naar melanosomen en reguleert hun splitsing
Met behulp van hoogresolutiemicroscopie en immunogoud-elektronenmicroscopie volgden de onderzoekers MFF direct op het oppervlak van melanosomen in alle stadia van hun levenscyclus. Time-lapse beelden legden zelfs vast dat MFF kleine puncta verliet op mitochondriën en naar LAMP1- en LysoTracker-gemarkeerde melanosomen bewoog. Op deze plekken vernauwden melanosoommembranen vaak en knepen ze af, waarbij tubuli en vesikels werden gevormd. Kwantitatieve analyse liet zien dat ongeveer een kwart van zichtbare melanosoomfissieregio’s door MFF was gemarkeerd, wat suggereert dat het een belangrijke klasse van splitsingsgebeurtenissen aanduidt. Wanneer de wetenschappers MFF-niveaus in pigmentcellen verlaagden, werden vroege melanosomen abnormaal vergroot en verschenen ze vaak als hybride structuren met kenmerken van zowel onrijpe als meer gevorderde stadia. Deze opgezwollen organellen deelden melanine uitgebreider met vroege markers, en live-imaging toonde minder succesvolle fission-gebeurtenissen, wat benadrukt dat MFF nodig is voor correcte deling en rijping van melanosomen.
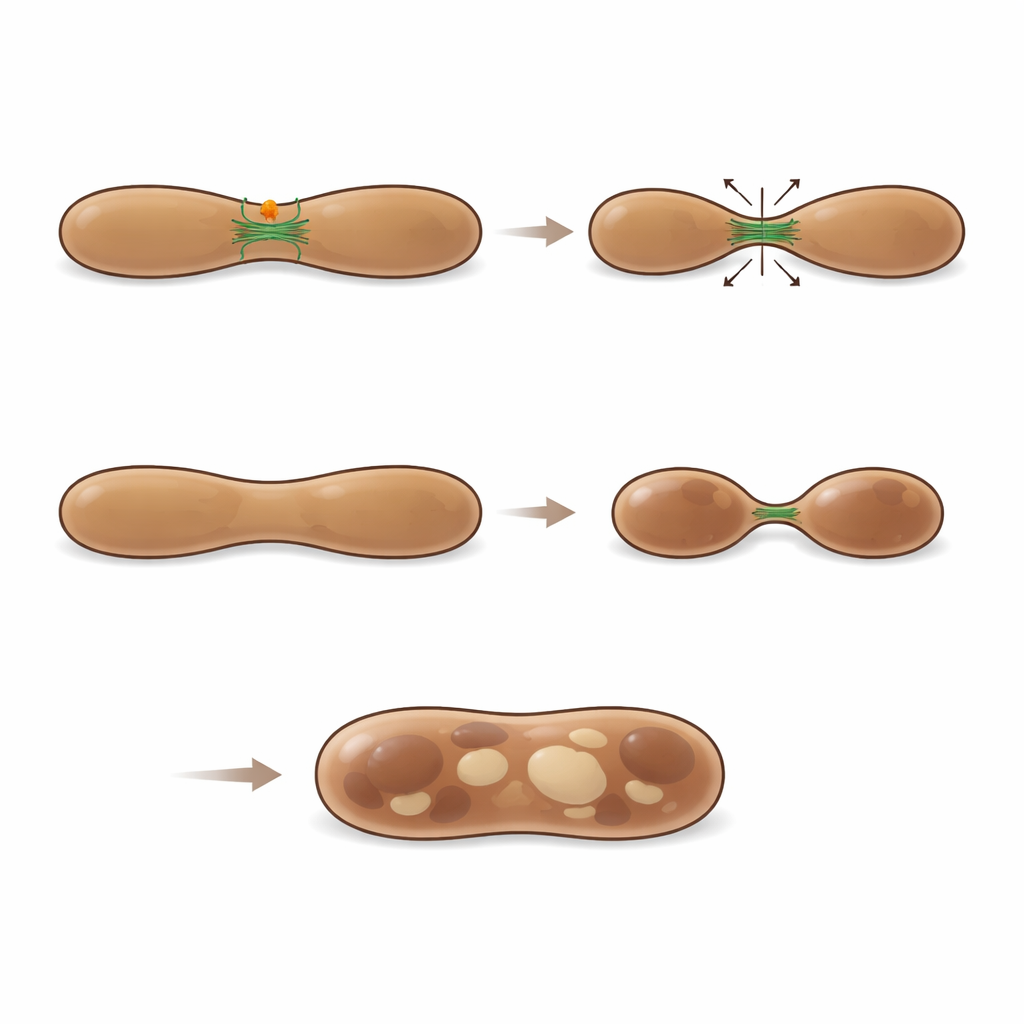
Balanceren van afbraak en opbouw met actinefilamenten
De gebruikelijke partner van MFF bij mitochondriale deling is een ander eiwit, DRP1. In melanosomen overlappen DRP1 en MFF echter zelden, en het stilleggen van elk van beide had zeer verschillende gevolgen. Verlies van DRP1 dempte hoofdzakelijk het genetische programma dat pigmentproductie aandrijft. Daarentegen vergrootte verlies van MFF vroege melanosomen en veroorzaakte een sterke toename van genen en eiwitten die met lysosomen—cellulaire recyclingscentra—en catabole enzymen zoals cathepsine B samenhangen. Deze enzymen concentreerden zich binnen melanosomen, waardoor ze zuurder werden en meer geneigd waren hun eigen pigmentmachinerie af te breken. Toen cathepsine B ook werd stilgelegd, zwollen melanosomen in MFF-deficiënte cellen verder op en stapelden ze zich in grote aantallen op, wat laat zien dat versterkte interne vertering normaal als noodoplossing dient om ophoping van disfunctionele, te grote pigmentgranules te voorkomen.
Hoe het skelet van de cel helpt pigmentgranules te snijden
Om te begrijpen hoe MFF fysiek helpt bij het splitsen van melanosomen, bepaalden de auteurs welke eiwitten eraan binden. Ze vonden talrijke regulatoren van het actinecytoskelet, waaronder componenten van het WASH-complex en de ARP2/3 actine-nucleerende machinerie. Beelden toonden actinefilamenten die zich concentreerden bij de nekken van melanosomen waar MFF-puncta zaten, en die vernauwde regio’s tussen twee uitgroeiende compartimenten overbrugden. Wanneer sleutelondereenheden van ARP2/3 werden stilgelegd, vergrootten vroege melanosomen op vrijwel dezelfde manier als bij verlies van MFF, wat aantoont dat actine-gestuurde filamentvorming essentieel is voor correcte splitsing. Remmen van ARP2/3-activiteit wist ook het melanosoomvergrotende effect van MFF-verlies uit, en koppelt zo MFF-functie sterk aan actinedynamiek in plaats van aan DRP1. Gezamenlijk onthullen deze bevindingen dat MFF een actinegebaseerde fissiemachine bij melanosomen rekruteert of stabiliseert, waardoor ze ongewenste componenten kunnen afstoten en kunnen doorgroeien naar volledig gepigmenteerde, correct gekalibreerde organellen.
Wat dit betekent voor pigmentstoornissen
De studie toont aan dat MFF, lang gezien als specialist in mitochondriale deling, ook buiten mitochondriën optreedt om de grootte, vorm en rijping van melanosomen te reguleren via actine-gestuurde fissies. Wanneer MFF ontbreekt, kunnen vroege pigmentgranules niet goed splitsen, groeien ze te groot en lijken ze steeds meer op degraderende compartimenten, waardoor de cel hun afbraak opvoert. Deze inzichten helpen verklaren hoe gigantische melanosomen ontstaan bij bepaalde erfelijke vormen van albinisme en aanverwante aandoeningen, en ze wijzen op MFF en zijn actinepartners als potentiële doelwitten om pigmentatie te moduleren of te begrijpen hoe pigmentcellen in ziekte falen.
Bronvermelding: Magalhães Rebelo, A.P., Maracani, A., Greco, S. et al. MFF budding from mitochondria regulates melanosome size and maturation. Nat Commun 17, 3932 (2026). https://doi.org/10.1038/s41467-026-70572-3
Trefwoorden: melanosomen, mitochondriën, MFF-eiwit, pigmentatie, actine cytoskelet