Clear Sky Science · es
MFF que brota desde las mitocondrias regula el tamaño y la maduración de los melanosomas
Por qué importa la maquinaria que produce color en las células
Nuestra piel, cabello y ojos deben su color a pequeñas fábricas de pigmento dentro de las células llamadas melanosomas. Mantener estas estructuras en el tamaño adecuado y en buen estado no es solo importante para la apariencia, sino también para proteger los tejidos de la luz solar. Este estudio descubre un actor sorprendente en cómo los melanosomas crecen, se dividen y maduran: una proteína conocida principalmente por moldear las mitocondrias, las centrales energéticas de la célula. Al mostrar que esta proteína también esculpe los melanosomas, los investigadores conectan orgánulos productores de energía con orgánulos productores de pigmento, ofreciendo nuevas pistas sobre cómo se controla el color en la salud y la enfermedad.
Un nuevo papel para un ayudante mitocondrial
Los melanosomas son compartimentos especializados que sintetizan y almacenan melanina, el pigmento oscuro que protege a las células del daño ultravioleta. A medida que se desarrollan, los melanosomas pasan por varias fases, llenándose gradualmente de pigmento antes de transferirse a células vecinas de la piel. Durante este proceso, sus membranas se remodelan constantemente: se alargan en túbulos, se desprenden pequeños fragmentos y, a veces, se fusionan. La maquinaria que impulsa esta remodelación solo se entendía parcialmente. Los autores se centraron en una proteína llamada factor de fisión mitocondrial (MFF), conocida por ayudar a dividir las mitocondrias. Para su sorpresa, encontraron MFF no solo en las mitocondrias, sino también en los melanosomas, especialmente en sitios donde estos gránulos de pigmento se estrechan y parecen listos para dividirse.
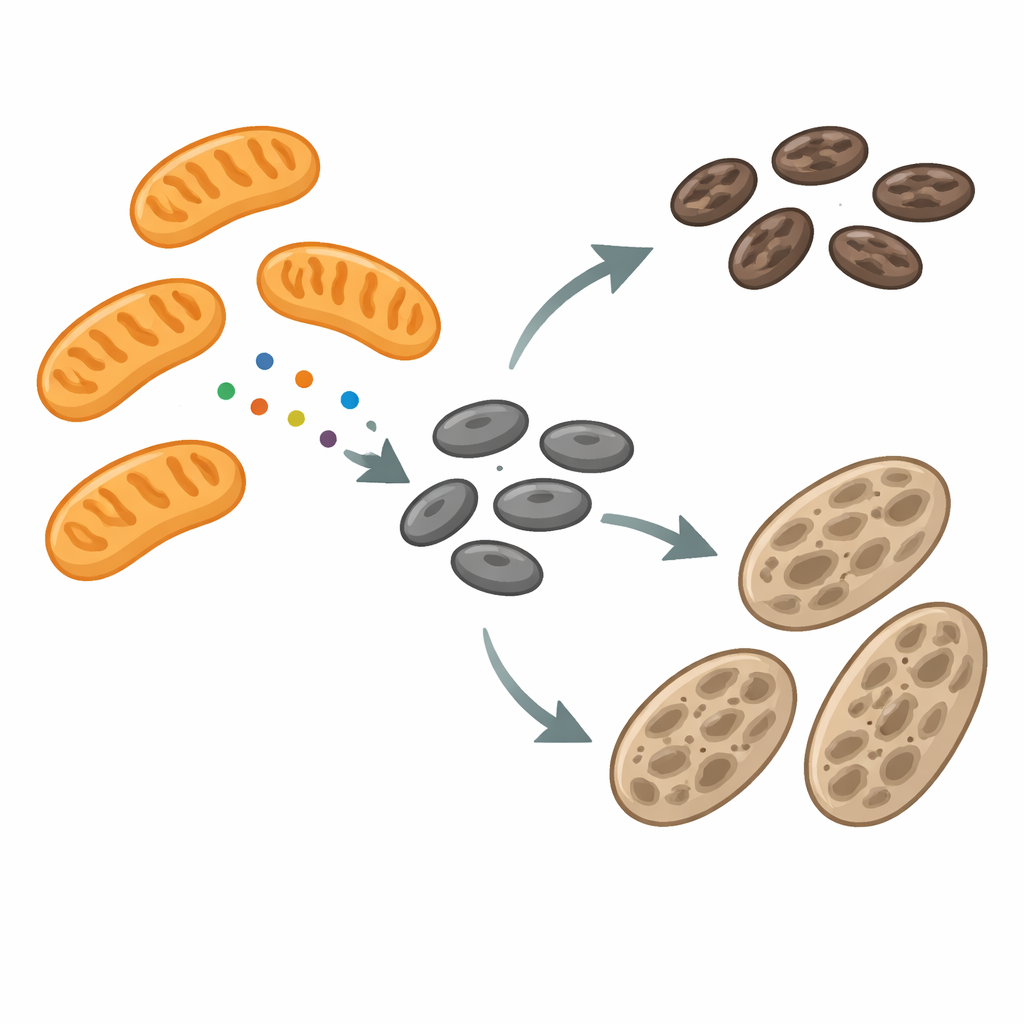
Cuando el pigmento se atasca, cambian los contactos y las señales
Para investigar cómo se comunican mitocondrias y melanosomas, el equipo comparó células de ratón productoras de pigmento normales con células albinas que no pueden sintetizar melanina debido a un gen de tirosinasa defectuoso. Las células albinas acumularon muchos melanosomas inmaduros y mostraron contactos físicos más frecuentes entre melanosomas y mitocondrias. La secuenciación de ARN y el análisis proteico revelaron que, en estas células albinas, se activaron genes y proteínas vinculados a las mitocondrias, incluyendo MFF localizado en la membrana mitocondrial externa. Sin embargo, la morfología mitocondrial parecía en gran medida normal, mientras que los melanosomas eran tanto más grandes como más dinámicos, sufriendo frecuentes procesos de fisión y fusión. Este patrón sugirió que MFF podría ser redirigido desde las mitocondrias hacia los melanosomas, donde podría influir en cómo estos orgánulos de pigmento se dividen y maduran.
MFF viaja a los melanosomas y controla su escisión
Usando microscopía de alta resolución e inmunomicroscopía con oro, los investigadores localizaron MFF directamente en la superficie de los melanosomas en todas las etapas de su ciclo vital. Imágenes tiempo real incluso captaron a MFF abandonando las mitocondrias en forma de pequeños puntos y moviéndose hacia melanosomas marcados con LAMP1 y LysoTracker. En estos sitios, las membranas de los melanosomas con frecuencia se estrechaban y se pellizcaban, formando túbulos y vesículas. El análisis cuantitativo mostró que aproximadamente una cuarta parte de las regiones visibles de fisión de melanosomas estaban decoradas por MFF, lo que sugiere que marca una clase importante de eventos de escisión. Cuando los científicos redujeron los niveles de MFF en células pigmentarias, los melanosomas tempranos se agrandaron de forma anómala, apareciendo a menudo como estructuras híbridas con rasgos tanto de etapas inmaduras como de más avanzadas. Estos orgánulos hinchados compartían melanina más extensamente con marcadores tempranos, y las imágenes en vivo mostraron menos eventos de fisión exitosos, lo que subraya que MFF es necesario para la división y maduración adecuadas de los melanosomas.
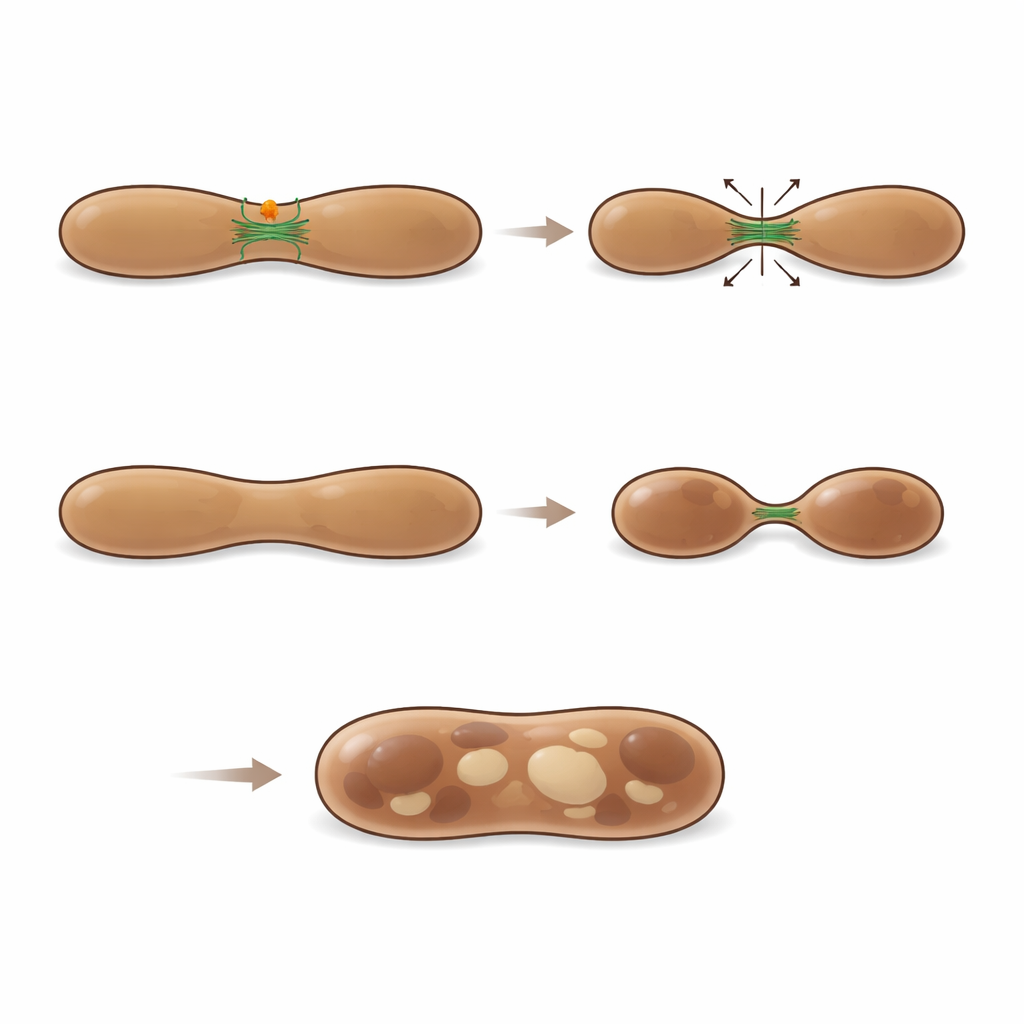
Equilibrar la degradación y la construcción con filamentos de actina
El compañero habitual de MFF en la división mitocondrial es otra proteína, DRP1. Sin embargo, en los melanosomas, DRP1 y MFF rara vez se solaparon, y silenciar cada una produjo consecuencias muy diferentes. La pérdida de DRP1 atenuó principalmente el programa genético que impulsa la producción de pigmento. En contraste, la pérdida de MFF agrandó los melanosomas tempranos y desencadenó un fuerte aumento en genes y proteínas vinculados a los lisosomas—centros de reciclaje celular—y a enzimas catabólicas como la catepsina B. Estas enzimas se concentraron dentro de los melanosomas, haciéndolos más ácidos y más propensos a degradar su propia maquinaria de pigmento. Cuando la catepsina B también se silenció, los melanosomas en células deficientes en MFF se hincharon aún más y se acumularon en gran número, mostrando que la digestión interna aumentada actúa normalmente como una copia de seguridad para evitar la acumulación de gránulos de pigmento disfuncionales y sobredimensionados.
Cómo el esqueleto celular ayuda a cortar los gránulos de pigmento
Para entender cómo MFF ayuda físicamente a dividir los melanosomas, los autores trazaron qué proteínas se unen a él. Encontraron numerosos reguladores del citoesqueleto de actina, incluyendo componentes del complejo WASH y la maquinaria nucleante ARP2/3. La imagen mostró filamentos de actina concentrándose en los cuellos de los melanosomas donde se ubicaban los puntos de MFF, conectando regiones constriñidas entre dos compartimentos que brotaban. Cuando se silenciaron subunidades clave de ARP2/3, los melanosomas tempranos se agrandaron de forma muy similar a lo observado con la pérdida de MFF, lo que indica que la formación de filamentos impulsada por actina es esencial para una escisión adecuada. Inhibir la actividad de ARP2/3 también eliminó el efecto de agrandamiento de melanosomas causado por la pérdida de MFF, vinculando estrechamente la función de MFF a la dinámica de la actina más que a DRP1. En conjunto, estos hallazgos revelan que MFF recluta o estabiliza una máquina de fisión basada en actina en los melanosomas, permitiéndoles desprender componentes innecesarios y avanzar hacia orgánulos plenamente pigmentados y de tamaño adecuado.
Qué significa esto para los trastornos del pigmento
El estudio muestra que MFF, considerada durante mucho tiempo una especialista en la división mitocondrial, también actúa fuera de las mitocondrias para regular el tamaño, la forma y la maduración de los melanosomas a través de la fisión impulsada por actina. Cuando falta MFF, los gránulos de pigmento tempranos no pueden dividirse correctamente, crecen demasiado y se asemejan cada vez más a compartimentos degradativos, lo que lleva a la célula a aumentar su degradación. Estas ideas ayudan a explicar cómo surgen melanosomas gigantes en ciertas formas hereditarias de albinismo y condiciones relacionadas, y señalan a MFF y sus socios de actina como posibles dianas para modular la pigmentación o entender cómo las células pigmentarias funcionan mal en la enfermedad.
Cita: Magalhães Rebelo, A.P., Maracani, A., Greco, S. et al. MFF budding from mitochondria regulates melanosome size and maturation. Nat Commun 17, 3932 (2026). https://doi.org/10.1038/s41467-026-70572-3
Palabras clave: melanosomas, mitocondrias, proteína MFF, pigmentación, citoesqueleto de actina