Clear Sky Science · pt
O brotamento de MFF a partir de mitocôndrias regula o tamanho e a maturação de melanossomos
Por que a maquinaria que produz cor nas células importa
Nossa pele, cabelo e olhos devem sua cor a pequenas fábricas de pigmento dentro das células chamadas melanossomos. Manter essas estruturas com o tamanho adequado e em bom funcionamento é essencial não apenas para a aparência, mas também para proteger nossos tecidos contra a luz solar. Este estudo revela um ator surpreendente em como os melanossomos crescem, se dividem e amadurecem: uma proteína mais conhecida por moldar mitocôndrias, as usinas de energia da célula. Ao mostrar que essa proteína também escultura melanossomos, os pesquisadores conectam organelas produtoras de energia às produtoras de pigmento, oferecendo pistas novas sobre como a cor é controlada na saúde e na doença.
Um novo papel para um auxiliar mitocondrial
Melanossomos são compartimentos especializados que sintetizam e armazenam melanina, o pigmento escuro que protege as células dos danos ultravioleta. À medida que se desenvolvem, os melanossomos passam por vários estágios, enchendo-se progressivamente de pigmento antes de serem transferidos para células vizinhas da pele. Durante essa jornada, suas membranas remodelam-se constantemente—esticando-se em túbulos, destacando pequenos fragmentos e, às vezes, fundindo-se. A maquinaria que dirige essa remodelação foi apenas parcialmente compreendida. Os autores focaram em uma proteína chamada fator de fissão mitocondrial (MFF), conhecida por ajudar a dividir mitocôndrias. Para surpresa deles, encontraram MFF não apenas nas mitocôndrias, mas também nos melanossomos, especialmente em locais onde esses grânulos de pigmento se estreitam e parecem prontos para se dividir.
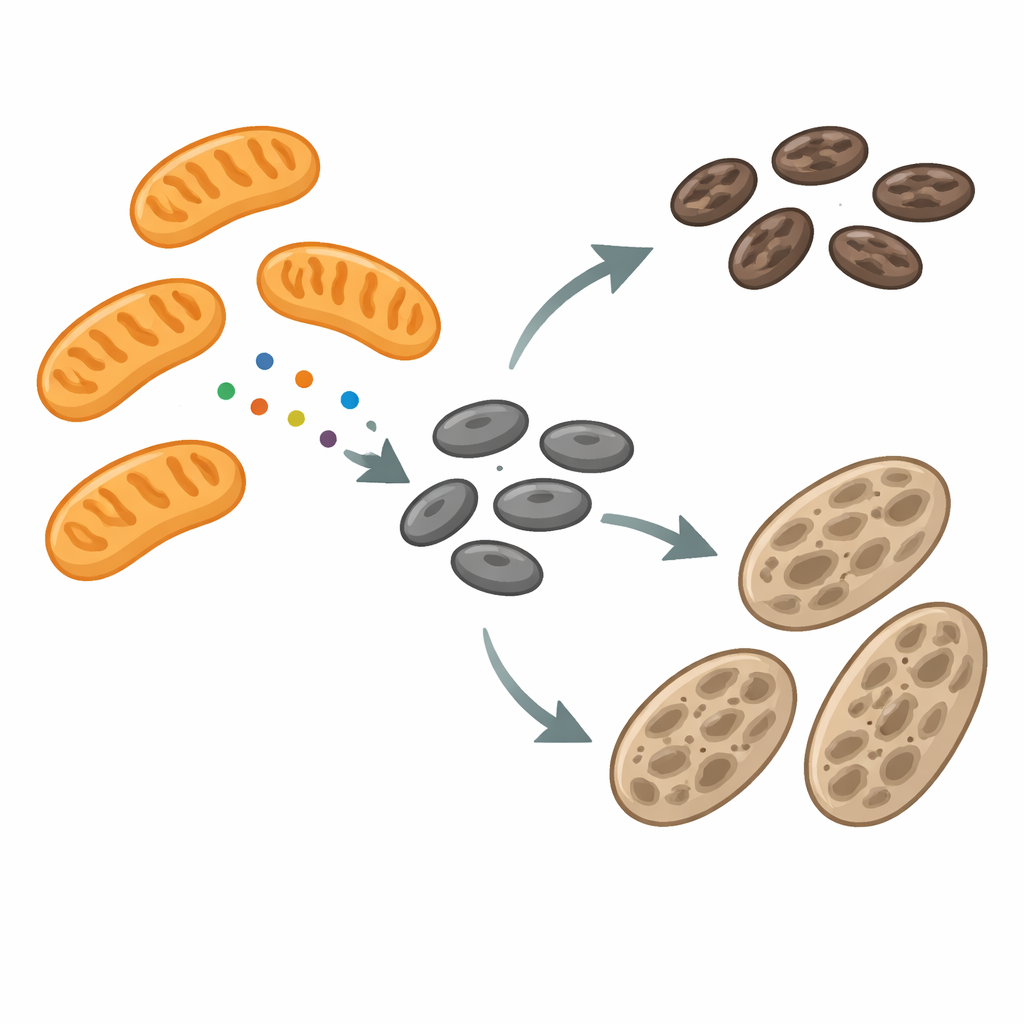
Quando o pigmento atrasa, contatos e sinais mudam
Para investigar como mitocôndrias e melanossomos se comunicam, a equipe comparou células produtoras de pigmento normais de camundongo com células albinas que não conseguem produzir melanina por causa de um gene da tirosinase defeituoso. As células albinas acumularam muitos melanossomos imaturos e mostraram contatos físicos mais frequentes entre melanossomos e mitocôndrias. Sequenciamento de RNA e análise proteica revelaram que, nessas células albinas, genes e proteínas ligados às mitocôndrias estavam aumentados, inclusive MFF localizado na membrana externa mitocondrial. Ainda assim, a forma mitocondrial parecia em grande parte normal, enquanto os melanossomos eram maiores e mais dinâmicos, sofrendo fusões e físsões frequentes. Esse padrão sugeriu que MFF poderia estar sendo redirecionado das mitocôndrias para os melanossomos, onde poderia influenciar como essas organelas de pigmento se dividem e amadurecem.
MFF viaja para os melanossomos e controla sua divisão
Usando microscopia de alta resolução e microscopia eletrônica com imunogold, os pesquisadores rastrearam MFF diretamente na superfície dos melanossomos em todos os estágios de seu ciclo de vida. Imagens em lapso de tempo capturaram até MFF saindo das mitocôndrias como pequenos pontinhos e se movendo para melanossomos marcados por LAMP1 e LysoTracker. Nesses locais, as membranas dos melanossomos frequentemente se estreitavam e se destacavam, formando túbulos e vesículas. Análises quantitativas mostraram que cerca de um quarto das regiões visíveis de fissão de melanossomos eram decoradas por MFF, sugerindo que ele marca uma classe importante de eventos de separação. Quando os cientistas reduziram os níveis de MFF em células pigmentares, os melanossomos precoces tornaram-se anormalmente aumentados, frequentemente aparecendo como estruturas híbridas que exibiam características tanto de estágios imaturos quanto de estágios mais avançados. Essas organelas inchadas compartilhavam melanina de forma mais extensiva com marcadores precoces, e imagens ao vivo mostraram menos eventos de fissão bem-sucedidos, ressaltando que MFF é necessário para a divisão e maturação adequadas dos melanossomos.
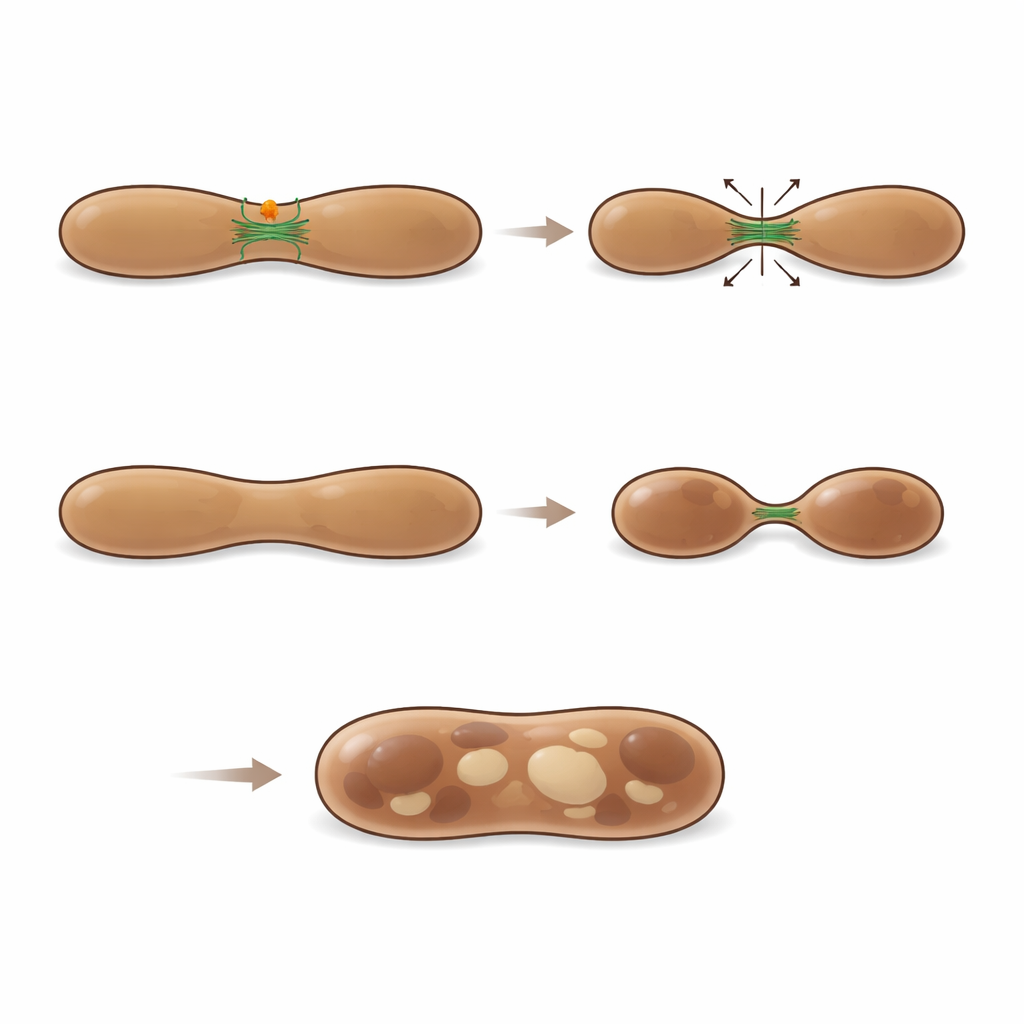
Equilibrando degradação e construção com filamentos de actina
O parceiro usual de MFF na divisão mitocondrial é outra proteína, DRP1. Contudo, nos melanossomos, DRP1 e MFF raramente se sobrepunham, e a silenciação de cada um causou consequências muito diferentes. A perda de DRP1 suprimiu principalmente o programa genético que impulsiona a produção de pigmento. Em contraste, a perda de MFF aumentou o tamanho dos melanossomos precoces e desencadeou um forte aumento em genes e proteínas ligados aos lisossomos—centros de reciclagem celular—e a enzimas catabólicas como a catepsina B. Essas enzimas se concentraram dentro dos melanossomos, tornando-os mais ácidos e mais propensos a degradar sua própria maquinaria de pigmento. Quando a catepsina B também foi silenciada, os melanossomos em células deficientes em MFF inchavam ainda mais e se acumulavam em grande número, demonstrando que a digestão interna aumentada normalmente funciona como um mecanismo de backup para evitar o acúmulo de grânulos de pigmento disfuncionais e sobredimensionados.
Como o esqueleto da célula ajuda a fatiar grânulos de pigmento
Para entender como MFF fisicamente auxilia a divisão dos melanossomos, os autores mapearam quais proteínas se ligam a ele. Encontraram numerosos reguladores do citoesqueleto de actina, incluindo componentes do complexo WASH e da maquinaria nucleadora de actina ARP2/3. A imageologia mostrou filamentos de actina se aglomerando nos pedúnculos dos melanossomos onde pontinhos de MFF estavam presentes, fazendo a ponte em regiões constritas entre dois compartimentos em formação. Quando subunidades chave do ARP2/3 foram silenciadas, melanossomos precoces aumentaram de tamanho de modo muito semelhante ao observado com a perda de MFF, indicando que a formação de filamentos conduzida por actina é essencial para a fissão adequada. Inibir a atividade do ARP2/3 também anulou o efeito de aumento de melanossomos causado pela perda de MFF, vinculando fortemente a função de MFF à dinâmica da actina em vez de ao DRP1. Em conjunto, esses achados revelam que MFF recruta ou estabiliza uma máquina de fissão baseada em actina nos melanossomos, permitindo que eles descartem componentes desnecessários e progridam em direção a organelas totalmente pigmentadas e de tamanho adequado.
O que isso significa para distúrbios de pigmentação
O estudo mostra que MFF, largamente vista como especialista na divisão mitocondrial, também atua fora das mitocôndrias para regular o tamanho, a forma e a maturação dos melanossomos por meio de fissão dirigida por actina. Quando MFF está ausente, os grânulos de pigmento precoces não conseguem se dividir corretamente, crescem demais e tendem a se assemelhar a compartimentos degradativos, levando a célula a aumentar sua quebra. Esses insights ajudam a explicar como melanossomos gigantes surgem em certas formas hereditárias de albinismo e condições relacionadas, e destacam MFF e seus parceiros de actina como alvos potenciais para modular a pigmentação ou entender como as células produtoras de pigmento funcionam de forma anômala em doenças.
Citação: Magalhães Rebelo, A.P., Maracani, A., Greco, S. et al. MFF budding from mitochondria regulates melanosome size and maturation. Nat Commun 17, 3932 (2026). https://doi.org/10.1038/s41467-026-70572-3
Palavras-chave: melanossomos, mitocôndrias, proteína MFF, pigmentação, citoesqueleto de actina