Clear Sky Science · ar
عُنقود MFF المتبرعم من الميتوكوندريا ينظم حجم الميلازين ونضجها
لماذا تهم آلات صنع اللون داخل الخلايا
تدين بشرتنا وشعرنا وعيوننا بلونها لمصانع صبغية صغيرة داخل الخلايا تُدعى الميلازين. الحفاظ على هذه التركيبات بالحجم المناسب وبحالة تشغيل جيدة أمر أساسي ليس فقط للمظهر، بل أيضاً لحماية أنسجتنا من ضوء الشمس. تكشف هذه الدراسة عن لاعب مفاجئ في كيفية نمو الميلازين وتقسيمها ونضجها: بروتين معروف أساساً بتشكيل الميتوكوندريا، محطات طاقة الخلية. من خلال إظهار أن هذا البروتين ينحت أيضاً الميلازين، يربط الباحثون العضيات المنتجة للطاقة بتلك المصنعة للصبغة، مقدِّمين دلائل جديدة على كيفية التحكم في اللون في الصحة والمرض.
وظيفة جديدة لمساعد ميتوكوندري
الميلازين هي مقصورات متخصصة تُصنع وتخزن الميلاين، الصبغة الداكنة التي تحمي الخلايا من أضرار الأشعة فوق البنفسجية. أثناء تطورها، تمر الميلازين بعدة مراحل، وتمتلئ تدريجياً بالصبغة قبل أن تُنقل إلى الخلايا المجاورة في الجلد. خلال هذه الرحلة، تُعاد تشكيل أغشيتها باستمرار—تمتد إلى أنابيب، تنقبض لتقطع أجزاء صغيرة، وأحياناً تندمج معًا. كانت الآلات التي تقود هذا إعادة التشكيل مفهومة جزئياً فقط. ركز المؤلفون على بروتين يسمى عامل الانقسام الميتوكوندري (MFF)، المعروف بمساعدته في انقسام الميتوكوندريا. ولدهشتهم، وجدوا MFF ليس فقط على الميتوكوندريا، بل أيضاً على الميلازين، خصوصاً في مواقع تضيق فيها هذه الحبيبات الصبغية وتبدو مستعدة للانقسام.
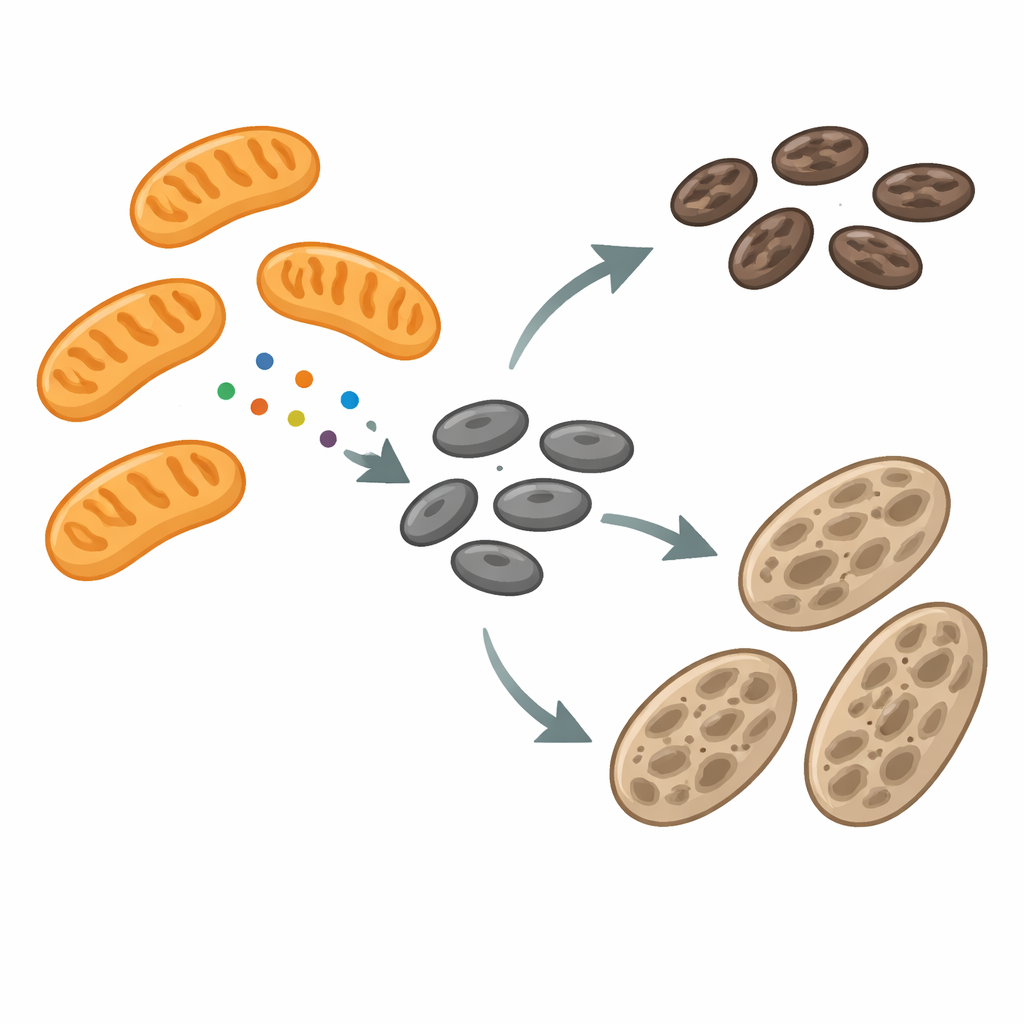
عندما يتعثر الصبغ، تتغير الاتصالات والإشارات
لفحص كيفية تواصل الميتوكوندريا والميلازين، قارن الفريق خلايا فأر طبيعية منتجة للصبغة مع خلايا ألبية لا تستطيع صنع الميلاين بسبب طفرة في جين التيروسيناز. تراكمت في الخلايا الألبية العديد من الميلازين غير الناضجة وأظهرت اتصالات مادية أكثر تكراراً بين الميلازين والميتوكوندريا. كشف تسلسل الرنا والبروتينات أن الجينات والبروتينات المرتبطة بالميتوكوندريا كانت مرتفعة في هذه الخلايا الألبية، بما في ذلك MFF الموجود على الغشاء الخارجي للميتوكوندريا. ومع ذلك بدا شكل الميتوكوندريا طبيعياً إلى حد كبير، بينما كانت الميلازين أكبر وأكثر ديناميكية، تخضع لانقسامات واندماجات متكررة. ألمح هذا النمط إلى احتمال إعادة توظيف MFF بعيداً عن الميتوكوندريا باتجاه الميلازين، حيث قد يؤثر على كيفية انقسام هذه العضيات الصبغية ونضوجها.
MFF ينتقل إلى الميلازين ويتحكم في انقسامها
باستخدام مجاهر عالية الدقة ومجهر إلكتروني مناعي مع ذهب منقّط، تتبع الباحثون MFF مباشرة على سطح الميلازين في جميع مراحل دورة حياتها. حتى أن تصوير الزمن-المتسلسل التقط MFF وهو يغادر الميتوكوندريا كحبيبات صغيرة ويتحرك إلى الميلازين المعلّمة بـ LAMP1 وLysoTracker. في هذه المواقع غالباً ما تضيق أغشية الميلازين وتنقبض، مكونة أنابيب وحويصلات. أظهر التحليل الكمي أن حوالي ربع مناطق انقسام الميلازين المرئية كانت مزينة بـ MFF، مما يشير إلى أنه يحدد فئة كبيرة من أحداث الانقسام. عندما قلل العلماء مستويات MFF في خلايا الصباغ، أصبحت الميلازين المبكرة متضخمة بشكل غير طبيعي، وغالباً ما ظهرت كتركيبات هجينة تمتلك خصائص لكل من المراحل غير الناضجة والمتقدمة. شاركت هذه العضيات المنتفخة الميلاين على نحو أوسع مع العلامات المبكرة، وأظهر التصوير الحي عددًا أقل من أحداث الانقسام الناجحة، مما يبرز أن MFF ضروري للانقسام والنضج السليم للميلازين.
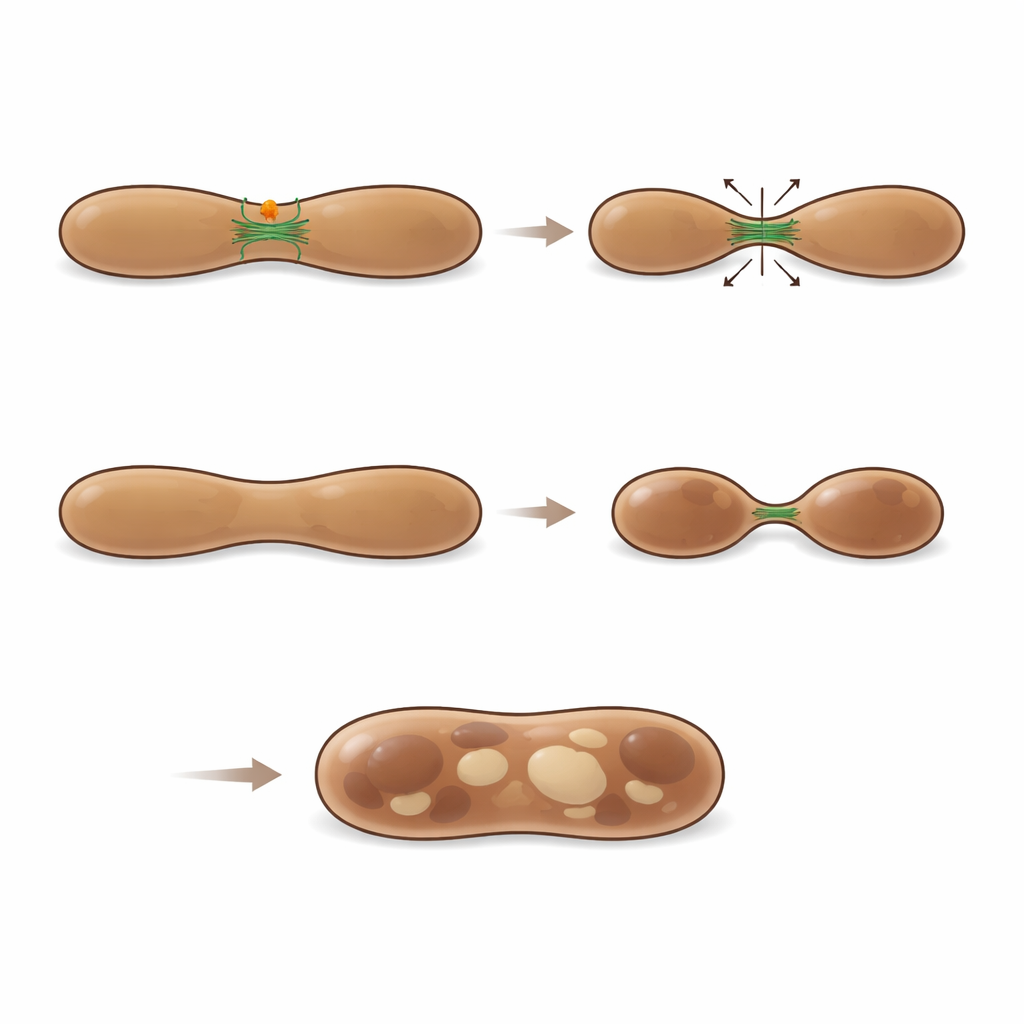
موازنة التحلل والبناء بخيوط الأكتين
الشريك المعتاد لـ MFF في انقسام الميتوكوندريا هو بروتين آخر، DRP1. لكن في الميلازين، نادراً ما تداخل DRP1 وMFF، وكمون كل واحد منهما أدى إلى نتائج مختلفة جداً. أدى فقدان DRP1 أساساً إلى كبح البرنامج الجيني الذي يقود إنتاج الصبغة. بالمقابل، وسع فقدان MFF الميلازين المبكرة وحفز زيادة قوية في الجينات والبروتينات المرتبطة بالجسيمات الحالّة—مراكز إعادة التدوير الخلوية—وبالإنزيمات الهضمية مثل الكاتيبتسين B. تراكمت هذه الإنزيمات داخل الميلازين، مما جعلها أكثر حموضة وأكثر ميلاً لتحليل آلية الصبغة الخاصة بها. عندما تم إسكات الكاتيبتسين B أيضاً، انتفخت الميلازين في الخلايا الناقصة عن MFF بشكل أكبر وتراكمت بأعداد كبيرة، مبينة أن الهضم الداخلي المعزز يعمل عادة كآلية احتياطية لمنع تراكم حبيبات صبغية معطلة ومفرطة الحجم.
كيف تساعد هياكل الخلية في تقطيع الحبيبات الصبغية
لفهم كيف يساعد MFF فعلياً في انقسام الميلازين، رسم المؤلفون خريطة البروتينات التي ترتبط به. وجدوا العديد من منظمات هيكل الأكتين، بما في ذلك مكونات مركب WASH وآلية نوواة الأكتين ARP2/3. أظهر التصوير تجمع خيوط الأكتين عند أعناق الميلازين حيث جلست بقع MFF، جسرًا للمناطق المقيدة بين مقصورتين متبرعمتين. عندما سُكّت وحدات فرعية رئيسية من ARP2/3، اتسعت الميلازين المبكرة بطريقة مشابهة للغاية لما يحدث عند فقدان MFF، مما يشير إلى أن تكوين الخيوط المدفوع بالأكتين ضروري للانقسام السليم. كما أزال تثبيط نشاط ARP2/3 أيضاً تأثير تضخيم الميلازين الناتج عن فقدان MFF، رابطاً وظيفة MFF ارتباطاً وثيقاً بديناميكيات الأكتين بدلاً من DRP1. تكشف هذه النتائج مجتمعة أن MFF يستقطب أو يثبت آلة انقسام قائمة على الأكتين عند الميلازين، مما يمكّنها من التخلص من مكونات غير مرغوب فيها والتقدم نحو عضيات مكتملة الصباغ وبالحجم المناسب.
ما الذي يعنيه هذا لاضطرابات الصباغ
تُظهر الدراسة أن MFF، الذي كان يُنظر إليه طويلاً كمتخصص في انقسام الميتوكوندريا، يعمل أيضاً خارج الميتوكوندريا لتنظيم حجم وشكل ونضج الميلازين عبر انقسام مدفوع بالأكتين. عندما يغيب MFF، لا تستطيع حبيبات الصباغ المبكرة الانقسام بشكل صحيح، فتتكبر وتتشابه بشكل متزايد مع مقصورات هاضمة، مما يدفع الخلية إلى رفع وتيرة تحللها. تساعد هذه الرؤى على تفسير كيف تنشأ ميلازين عملاقة في أشكال وراثية معينة من المهق والحالات المرتبطة بها، وتبرز MFF وشركاءه المرتبطين بالأكتين كأهداف محتملة لتعديل التصبغ أو لفهم كيف تفشل خلايا الصباغ في المرض.
الاستشهاد: Magalhães Rebelo, A.P., Maracani, A., Greco, S. et al. MFF budding from mitochondria regulates melanosome size and maturation. Nat Commun 17, 3932 (2026). https://doi.org/10.1038/s41467-026-70572-3
الكلمات المفتاحية: الميلازين, الميتوكوندريا, بروتين MFF, تصبغ, هيكل الأكتين الخلوي