Clear Sky Science · de
MFF, das von Mitochondrien abschnürt, reguliert Melanosomgröße und -reifung
Warum die farbproduzierende Maschinerie der Zellen wichtig ist
Unsere Haut, Haare und Augen verdanken ihre Farbe winzigen Pigmentfabriken in den Zellen, den Melanosomen. Diese Strukturen in der richtigen Größe und in funktionstüchtigem Zustand zu halten, ist nicht nur für das Erscheinungsbild wichtig, sondern schützt Gewebe auch vor Sonnenlicht. Diese Studie deckt einen überraschenden Akteur auf, der beeinflusst, wie Melanosomen wachsen, sich teilen und reifen: ein Protein, das vor allem dafür bekannt ist, Mitochondrien — die Kraftwerke der Zelle — zu formen. Indem die Forschenden zeigen, dass dieses Protein auch Melanosomen gestaltet, verknüpfen sie energieproduzierende Organellen mit pigmentbildenden und liefern neue Hinweise darauf, wie Farbe in Gesundheit und Krankheit gesteuert wird.
Eine neue Aufgabe für einen mitochondrialen Helfer
Melanosomen sind spezialisierte Kompartimente, die Melanin herstellen und speichern, das dunkle Pigment, das Zellen vor UV-Schäden schützt. Während ihrer Entwicklung durchlaufen Melanosomen mehrere Stadien und füllen sich nach und nach mit Pigment, bevor sie an benachbarte Hautzellen weitergegeben werden. Dabei remodelieren ihre Membranen ständig — sie dehnen sich zu Tubuli aus, schnüren kleine Teile ab und verschmelzen gelegentlich. Die Maschinerie, die dieses Remodeling antreibt, war bisher nur teilweise verstanden. Die Autorinnen und Autoren konzentrierten sich auf ein Protein namens mitochondrialer Spaltungsfaktor (MFF), das dafür bekannt ist, Mitochondrien bei der Teilung zu unterstützen. Zu ihrer Überraschung fanden sie MFF nicht nur auf Mitochondrien, sondern auch auf Melanosomen, insbesondere an Stellen, an denen diese Pigmentgranula sich verengen und offenbar kurz vor dem Abschnüren stehen.
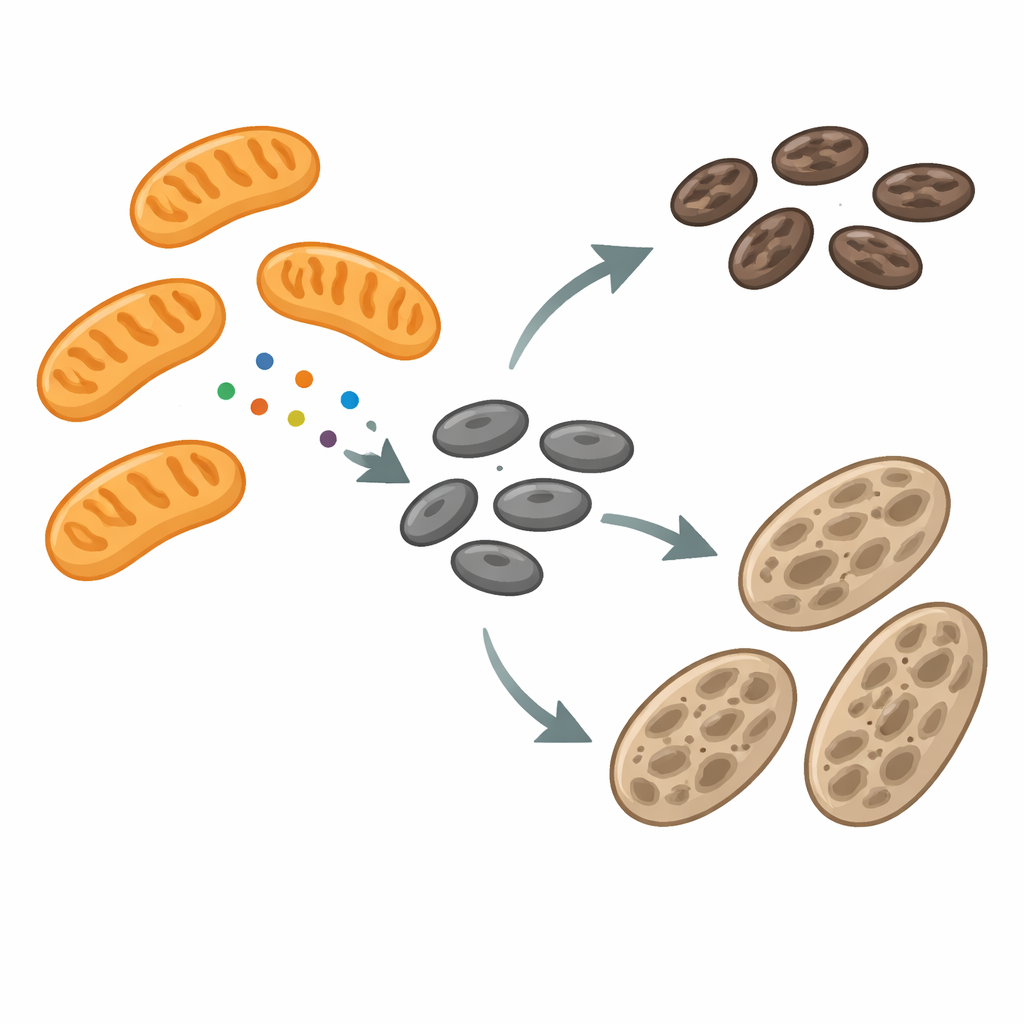
Wenn Pigment stagniert, verändern sich Kontakte und Signale
Um zu untersuchen, wie Mitochondrien und Melanosomen kommunizieren, verglich das Team normale pigmentproduzierende Mäusezellen mit albinospezifischen Zellen, die aufgrund eines defekten Tyrosinase-Gens kein Melanin herstellen können. Die Albinozellen häuften viele unreife Melanosomen an und zeigten häufigere physische Kontakte zwischen Melanosomen und Mitochondrien. RNA-Sequenzierung und Proteinanalysen ergaben, dass in diesen Albinozellen Gene und Proteine, die mit Mitochondrien verknüpft sind, hochreguliert waren, darunter MFF auf der äußeren mitochondrialen Membran. Die Gestalt der Mitochondrien wirkte jedoch weitgehend normal, während die Melanosomen sowohl größer als auch dynamischer waren und häufige Fissions- und Fusionsereignisse zeigten. Dieses Muster deutete darauf hin, dass MFF möglicherweise von den Mitochondrien zu den Melanosomen umgelagert wird, wo es beeinflussen könnte, wie diese Pigmentorganellen sich teilen und reifen.
MFF wandert zu Melanosomen und steuert deren Abspaltung
Mithilfe hochauflösender Mikroskopie und immunogold-elektronenmikroskopischer Aufnahmen verfolgten die Forschenden MFF direkt an der Oberfläche von Melanosomen in allen Stadien ihres Lebenszyklus. Zeitrafferaufnahmen dokumentierten sogar, wie MFF als kleine Punktstrukturen von Mitochondrien absprang und auf mit LAMP1 und LysoTracker markierte Melanosomen überging. An diesen Stellen verengten sich Melanosomenmembranen häufig und schnürten sich ab, wobei Tubuli und Vesikel entstanden. Quantitative Analysen zeigten, dass etwa ein Viertel der sichtbaren Melanosomen-Fissionsregionen von MFF markiert war, was darauf hindeutet, dass es eine bedeutende Klasse von Spaltungsereignissen kennzeichnet. Reduzierten die Wissenschaftlerinnen und Wissenschaftler MFF-Level in pigmentbildenden Zellen, wurden frühe Melanosomen ungewöhnlich vergrößert und traten oft als hybride Strukturen auf, die Merkmale sowohl unreifer als auch weiter entwickelter Stadien kombinierten. Diese angeschwollenen Organellen teilten Melanin stärker mit frühen Markern, und Live-Imaging zeigte weniger erfolgreiche Fissionsereignisse, was unterstreicht, dass MFF für die richtige Teilung und Reifung von Melanosomen notwendig ist.
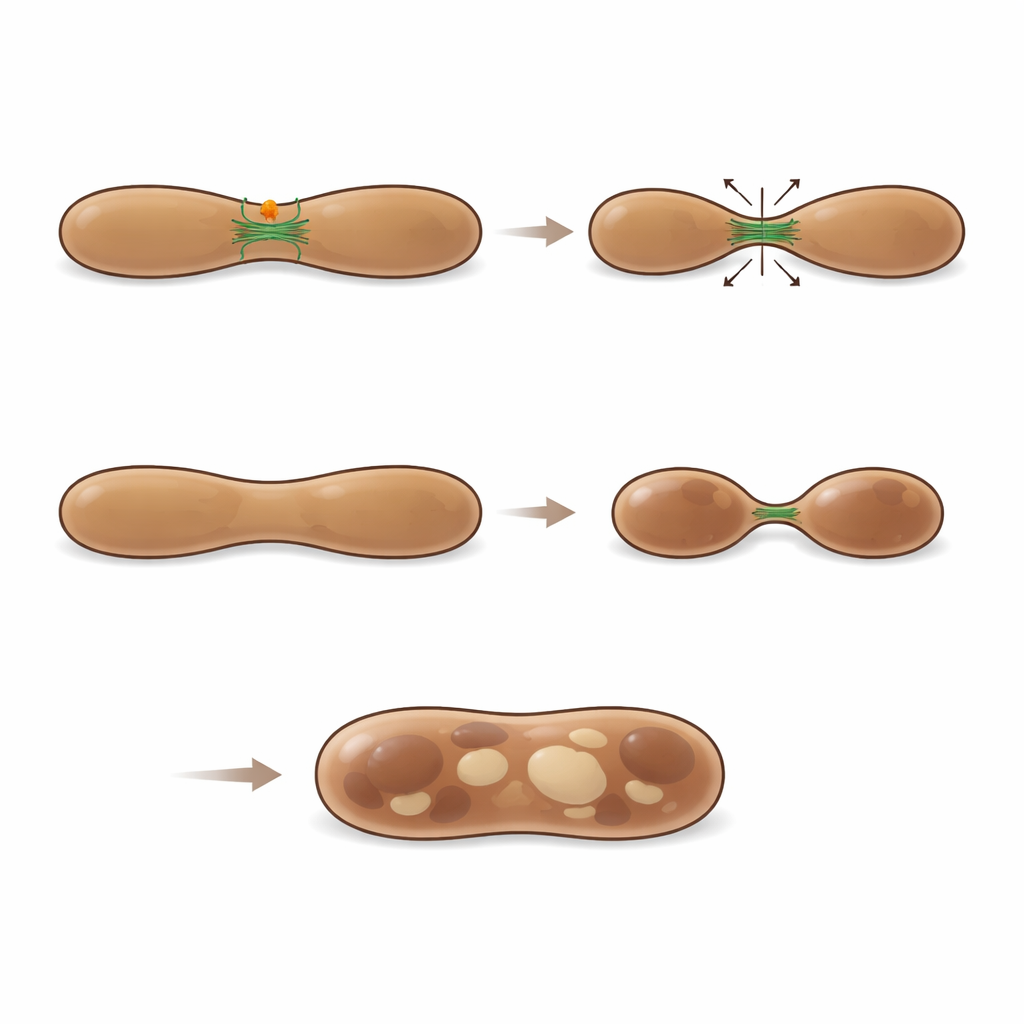
Gleichgewicht zwischen Abbau und Aufbau durch Aktinfilamente
Der übliche Partner von MFF bei mitochondrialer Spaltung ist ein anderes Protein, DRP1. In Melanosomen jedoch überschnitten sich DRP1 und MFF nur selten, und das Abschalten der jeweils einen oder anderen Komponente hatte sehr unterschiedliche Folgen. Der Verlust von DRP1 dämpfte vor allem das genetische Programm, das die Pigmentproduktion antreibt. Im Gegensatz dazu vergrößerte der Verlust von MFF frühe Melanosomen und rief eine starke Zunahme von Genen und Proteinen hervor, die mit Lysosomen — den zellulären Recyclingzentren — und katabolischen Enzymen wie Cathepsin B verbunden sind. Diese Enzyme konzentrierten sich innerhalb der Melanosomen, machten sie saurer und erhöhten deren Neigung, die eigene Pigmentmaschinerie zu zersetzen. Wurde Cathepsin B ebenfalls stillgelegt, schwollen die Melanosomen in MFF-defizienten Zellen weiter an und akkumulierten in großer Zahl, was zeigt, dass verstärkter interner Abbau normalerweise als Backup dient, um die Ansammlung dysfunktionaler, übergroßer Pigmentgranula zu verhindern.
Wie das zelluläre Skelett beim Zerteilen von Pigmentgranula hilft
Um zu verstehen, wie MFF physikalisch die Teilung von Melanosomen unterstützt, kartierten die Autorinnen und Autoren die an MFF bindenden Proteine. Sie fanden zahlreiche Regulatoren des Aktin-Zytoskeletts, darunter Komponenten des WASH-Komplexes und die Aktin-nukleierende ARP2/3-Maschinerie. Bildgebende Verfahren zeigten Aktinfilamente, die an den Hälsen von Melanosomen konzentriert waren, wo MFF-Punktstrukturen saßen und verengte Bereiche zwischen zwei abschnürenden Kompartimenten überbrückten. Wurden zentrale ARP2/3-Untereinheiten stillgelegt, vergrößerten sich frühe Melanosomen in sehr ähnlicher Weise wie bei MFF-Verlust, was darauf hinweist, dass aktingetriebene Filamentbildung für die korrekte Abspaltung unerlässlich ist. Die Hemmung der ARP2/3-Aktivität beseitigte außerdem den Melanosomvergrößerungseffekt von MFF-Mangel und verband so die Funktion von MFF eng mit Aktindynamik statt mit DRP1. Zusammengenommen zeigen diese Befunde, dass MFF eine aktinbasierte Spaltungsmaschinerie an Melanosomen rekrutiert oder stabilisiert und es diesen ermöglicht, unnötige Komponenten abzuschnüren und zur vollständigen Pigmentierung und richtigen Größe voranzuschreiten.
Was das für Pigmentstörungen bedeutet
Die Studie zeigt, dass MFF, lange als Spezialist für mitochondriale Teilung betrachtet, auch außerhalb von Mitochondrien wirkt, um Größe, Form und Reifung von Melanosomen über aktingetriebene Spaltung zu regulieren. Fehlt MFF, können frühe Pigmentgranula sich nicht richtig teilen, wachsen zu groß und ähneln zunehmend degradativen Kompartimenten, woraufhin die Zelle ihren Abbau hochfährt. Diese Einsichten helfen zu erklären, wie riesige Melanosomen bei bestimmten erblichen Formen von Albinismus und verwandten Erkrankungen entstehen, und heben MFF sowie seine Aktin-Partner als potenzielle Ziele hervor, um Pigmentierung zu modulieren oder zu verstehen, wie Pigmentzellen bei Krankheiten fehlfunktionieren.
Zitation: Magalhães Rebelo, A.P., Maracani, A., Greco, S. et al. MFF budding from mitochondria regulates melanosome size and maturation. Nat Commun 17, 3932 (2026). https://doi.org/10.1038/s41467-026-70572-3
Schlüsselwörter: Melanosomen, Mitochondrien, MFF-Protein, Pigmentierung, Aktin-Zytoskelett