Clear Sky Science · it
MFF che si origina dai mitocondri regola la dimensione e la maturazione dei melanosomi
Perché conta la macchina che produce il colore nelle cellule
La nostra pelle, i capelli e gli occhi devono il loro colore a minuscoli laboratori di pigmento all’interno delle cellule chiamati melanosomi. Mantenere queste strutture della giusta dimensione e in buono stato è essenziale non solo per l’aspetto, ma anche per proteggere i tessuti dalla luce solare. Questo studio scopre un attore sorprendente nel modo in cui i melanosomi crescono, si dividono e maturano: una proteina nota soprattutto per modellare i mitocondri, le centrali energetiche della cellula. Dimostrando che questa proteina plasma anche i melanosomi, i ricercatori collegano gli organelli produttori di energia con quelli che producono pigmento, offrendo nuovi indizi su come il colore sia controllato in salute e in malattia.
Un nuovo ruolo per un aiutante mitocondriale
I melanosomi sono compartimenti specializzati che sintetizzano e immagazzinano la melanina, il pigmento scuro che protegge le cellule dai danni ultravioletti. Durante il loro sviluppo, i melanosomi attraversano più stadi, riempiendosi gradualmente di pigmento prima di essere trasferiti alle cellule cutanee vicine. Nel corso di questo percorso, le loro membrane si rimodellano costantemente—si allungano in tubuli, si staccano piccole porzioni e talvolta si fondono. La macchina che guida questo rimodellamento è stata compresa solo in parte. Gli autori si sono concentrati su una proteina chiamata mitochondrial fission factor (MFF), nota per favorire la divisione mitocondriale. Con loro sorpresa, hanno trovato MFF non solo sui mitocondri, ma anche sui melanosomi, specialmente nei siti in cui questi granuli di pigmento si restringono e sembrano pronti a dividersi.
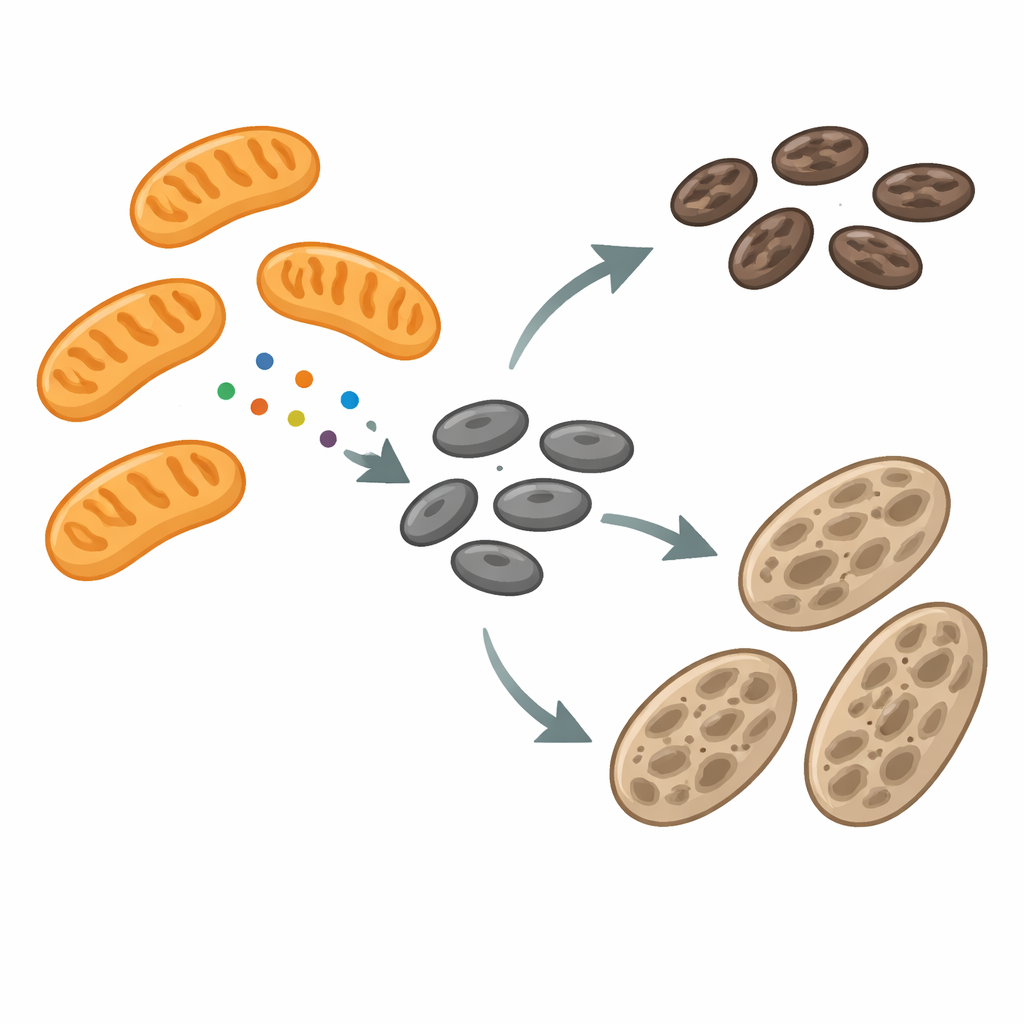
Quando il pigmento si blocca, cambiano i contatti e i segnali
Per indagare come mitocondri e melanosomi comunicano, il team ha confrontato cellule murine normali produttrici di pigmento con cellule albino che non possono sintetizzare melanina a causa di un gene della tirosinasi difettoso. Le cellule albino accumulavano molti melanosomi immaturi e mostravano contatti fisici più frequenti tra melanosomi e mitocondri. L’RNA-sequencing e l’analisi proteica hanno rivelato che, in queste cellule albino, geni e proteine legati ai mitocondri erano aumentati, compresa MFF localizzata sulla membrana mitocondriale esterna. Eppure la forma dei mitocondri appariva in gran parte normale, mentre i melanosomi risultavano sia più grandi sia più dinamici, sottoponendosi a frequenti eventi di fissione e fusione. Questo schema suggeriva che MFF potesse essere riprogrammata, spostandosi dai mitocondri verso i melanosomi, dove potrebbe influenzare come questi organelli di pigmento si dividono e maturano.
MFF arriva sui melanosomi e controlla la loro scissione
Usando microscopia ad alta risoluzione e immuno-microscopia elettronica con oro, i ricercatori hanno tracciato MFF direttamente sulla superficie dei melanosomi in tutte le fasi del loro ciclo vitale. Immagini time-lapse hanno persino catturato MFF che lasciava i mitocondri come piccoli puncta e si spostava su melanosomi marcati da LAMP1 e LysoTracker. In questi siti, le membrane dei melanosomi spesso si restringevano e si pizzicavano, formando tubuli e vescicole. L’analisi quantitativa ha mostrato che circa un quarto delle regioni visibili di fissione dei melanosomi era decorato da MFF, suggerendo che essa marca una classe importante di eventi di scissione. Quando gli scienziati ridussero i livelli di MFF nelle cellule produttrici di pigmento, i melanosomi precoci divennero anormalmente ingrossati, spesso apparendo come strutture ibride che presentavano caratteristiche sia degli stadi immaturi sia di quelli più avanzati. Questi organelli gonfi condividevano la melanina in modo più ampio con marker precoci, e l’imaging in vivo mostrò meno eventi di fissione riusciti, sottolineando che MFF è necessaria per la corretta divisione e maturazione dei melanosomi.
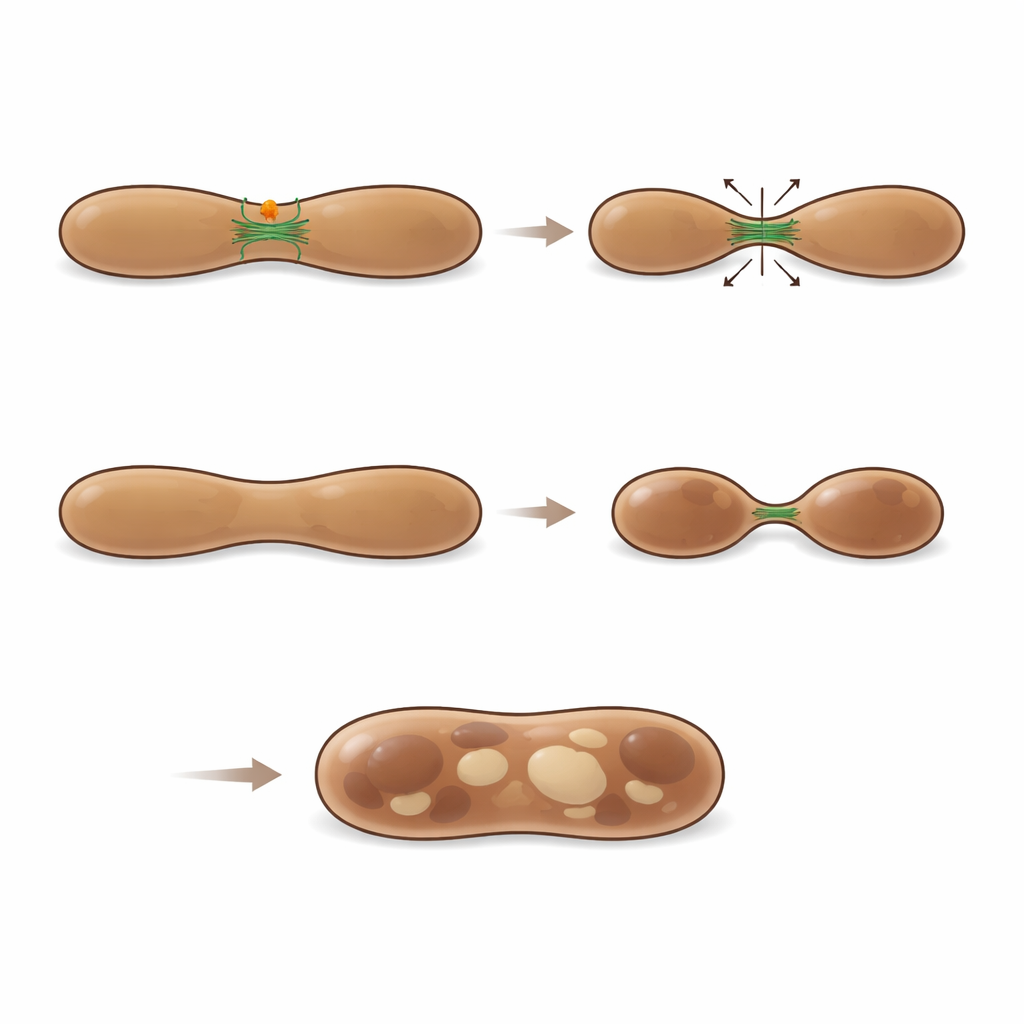
Bilanciare degradazione e costruzione con i filamenti di actina
Il partner abituale di MFF nella divisione mitocondriale è un’altra proteina, DRP1. Tuttavia, nei melanosomi, DRP1 e MFF si sovrapponevano raramente, e il silenziamento di ciascuna comportava conseguenze molto diverse. La perdita di DRP1 principalmente attenuava il programma genetico che guida la produzione di pigmento. Al contrario, la perdita di MFF ingrandiva i melanosomi precoci e scatenava un forte aumento di geni e proteine legati ai lisosomi—i centri di riciclo cellulare—e ad enzimi catabolici come la catepsina B. Questi enzimi si concentravano all’interno dei melanosomi, rendendoli più acidi e più inclini a degradare la propria macchina pigmentaria. Quando anche la catepsina B veniva silenziata, i melanosomi nelle cellule carenti di MFF si gonfiavano ulteriormente e si accumulavano in gran numero, mostrando che l’aumentata digestione interna serve normalmente come un meccanismo di riserva per evitare l’accumulo di granuli di pigmento disfunzionali e sovradimensionati.
Come lo scheletro cellulare aiuta a sezionare i granuli di pigmento
Per capire come MFF aiuti fisicamente la divisione dei melanosomi, gli autori hanno mappato le proteine che vi si legano. Hanno trovato numerosi regolatori del citoscheletro di actina, inclusi componenti del complesso WASH e della macchina nucleante ARP2/3. L’imaging ha mostrato filamenti di actina che si raggruppavano ai colli dei melanosomi dove si trovavano i puncta di MFF, collegando regioni ristrette tra due compartimenti in via di gemmazione. Quando subunità chiave di ARP2/3 furono silenziate, i melanosomi precoci si ingrandirono in modo molto simile a quanto osservato con la perdita di MFF, indicando che la formazione di filamenti guidata dall’actina è essenziale per una corretta scissione. L’inibizione dell’attività di ARP2/3 cancellò anche l’effetto di ingrossamento dei melanosomi dovuto alla perdita di MFF, collegando strettamente la funzione di MFF alla dinamica dell’actina piuttosto che a DRP1. Nel complesso, questi risultati rivelano che MFF recluta o stabilizza una macchina di fissione basata sull’actina sui melanosomi, permettendo loro di eliminare componenti non necessari e progredire verso organelli completamente pigmentati e della dimensione appropriata.
Cosa significa per i disturbi della pigmentazione
Lo studio mostra che MFF, a lungo considerata specialista della divisione mitocondriale, agisce anche al di fuori dei mitocondri per regolare dimensione, forma e maturazione dei melanosomi tramite la fissione guidata dall’actina. Quando MFF manca, i granuli di pigmento precoci non riescono a dividersi correttamente, crescono troppo e somigliano sempre più a compartimenti degradativi, spingendo la cellula ad aumentare la loro demolizione. Questi risultati aiutano a spiegare come sorgano melanosomi giganti in certe forme ereditarie di albinismo e in condizioni correlate, e mettono in luce MFF e i suoi partner dell’actina come possibili bersagli per modulare la pigmentazione o per comprendere come le cellule pigmentarie malfunzionino nelle malattie.
Citazione: Magalhães Rebelo, A.P., Maracani, A., Greco, S. et al. MFF budding from mitochondria regulates melanosome size and maturation. Nat Commun 17, 3932 (2026). https://doi.org/10.1038/s41467-026-70572-3
Parole chiave: melanosomi, mitocondri, proteina MFF, pigmentazione, cito scheletro a base di actina