Clear Sky Science · fr
MFF bourgeonnant depuis les mitochondries régule la taille et la maturation des mélanosomes
Pourquoi la machinerie de production de couleur des cellules compte
Notre peau, nos cheveux et nos yeux doivent leur couleur à d’infimes usines à pigments à l’intérieur des cellules appelées mélanosomes. Maintenir ces structures à la bonne taille et en bon état de fonctionnement est essentiel non seulement pour l’apparence, mais aussi pour protéger nos tissus du soleil. Cette étude met en lumière un acteur surprenant dans la façon dont les mélanosomes grandissent, se divisent et mûrissent : une protéine surtout connue pour façonner les mitochondries, les centrales énergétiques de la cellule. En montrant que cette protéine sculpte aussi les mélanosomes, les chercheurs relient les organites producteurs d’énergie aux organites fabriquant le pigment, offrant de nouveaux indices sur le contrôle de la couleur en santé et en maladie.
Un nouveau rôle pour un auxiliaire mitochondrial
Les mélanosomes sont des compartiments spécialisés qui synthétisent et stockent la mélanine, le pigment foncé qui protège les cellules des dommages ultraviolets. Au cours de leur développement, les mélanosomes traversent plusieurs étapes, se remplissant progressivement de pigment avant d’être transférés aux cellules cutanées voisines. Pendant ce parcours, leurs membranes se remodèlent en permanence : elles s’étirent en tubules, bourgeonnent pour former de petites vésicules et fusionnent parfois. La machinerie qui pilote ce remaniement n’était que partiellement comprise. Les auteurs se sont concentrés sur une protéine appelée facteur de fission mitochondrial (MFF), connue pour aider les mitochondries à se diviser. À leur grande surprise, ils ont trouvé MFF non seulement sur les mitochondries, mais aussi sur les mélanosomes, en particulier aux sites où ces granules de pigment se rétrécissent et semblent prêts à se scinder.
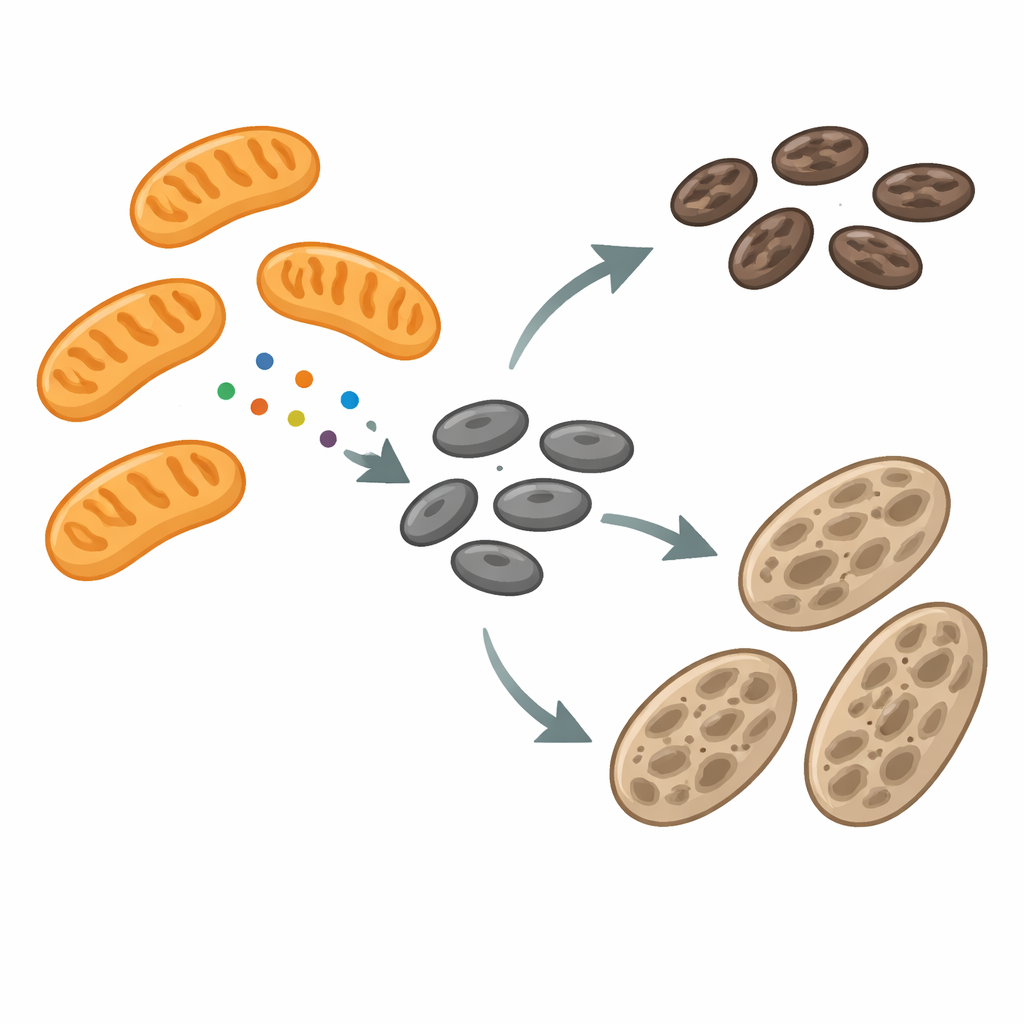
Quand le pigment stagne, les contacts et signaux changent
Pour étudier la communication entre mitochondries et mélanosomes, l’équipe a comparé des cellules de souris productrices de pigment normales à des cellules albinos incapables de fabriquer de la mélanine en raison d’un gène de la tyrosinase défectueux. Les cellules albinos accumulaient de nombreux mélanosomes immatures et présentaient des contacts physiques plus fréquents entre mélanosomes et mitochondries. Le séquençage de l’ARN et l’analyse protéique ont révélé que, dans ces cellules albinos, des gènes et protéines liés aux mitochondries étaient activés, y compris MFF situé sur la membrane externe mitochondriale. Pourtant, la forme des mitochondries semblait globalement normale, tandis que les mélanosomes étaient à la fois plus gros et plus dynamiques, subissant des fissions et des fusions fréquentes. Ce schéma laissait penser que MFF pourrait être réaffecté des mitochondries vers les mélanosomes, où il pourrait influencer la manière dont ces organites pigmentaires se scindent et mûrissent.
MFF se déplace vers les mélanosomes et contrôle leur division
À l’aide de microscopies à haute résolution et d’immunomarquage par microscopie électronique à l’or, les chercheurs ont tracé MFF directement à la surface des mélanosomes à tous les stades de leur cycle de vie. Des images en time-lapse ont même capturé MFF quittant les mitochondries sous forme de petites ponctuations et migrant vers des mélanosomes marqués par LAMP1 et LysoTracker. À ces sites, les membranes des mélanosomes se rétrécissaient souvent et bourgeonnaient, formant des tubules et des vésicules. L’analyse quantitative a montré qu’environ un quart des régions visibles de fission des mélanosomes étaient décorées par MFF, suggérant qu’il marque une classe importante d’événements de division. Lorsque les scientifiques ont réduit les niveaux de MFF dans des cellules pigmentaires, les mélanosomes précoces sont devenus anormalement volumineux, apparaissant souvent comme des structures hybrides présentant des caractéristiques à la fois immatures et plus avancées. Ces organites gonflés partageaient la mélanine de façon plus étendue avec des marqueurs précoces, et l’imagerie en direct a montré moins d’événements de fission réussis, soulignant que MFF est nécessaire pour une division et une maturation correctes des mélanosomes.
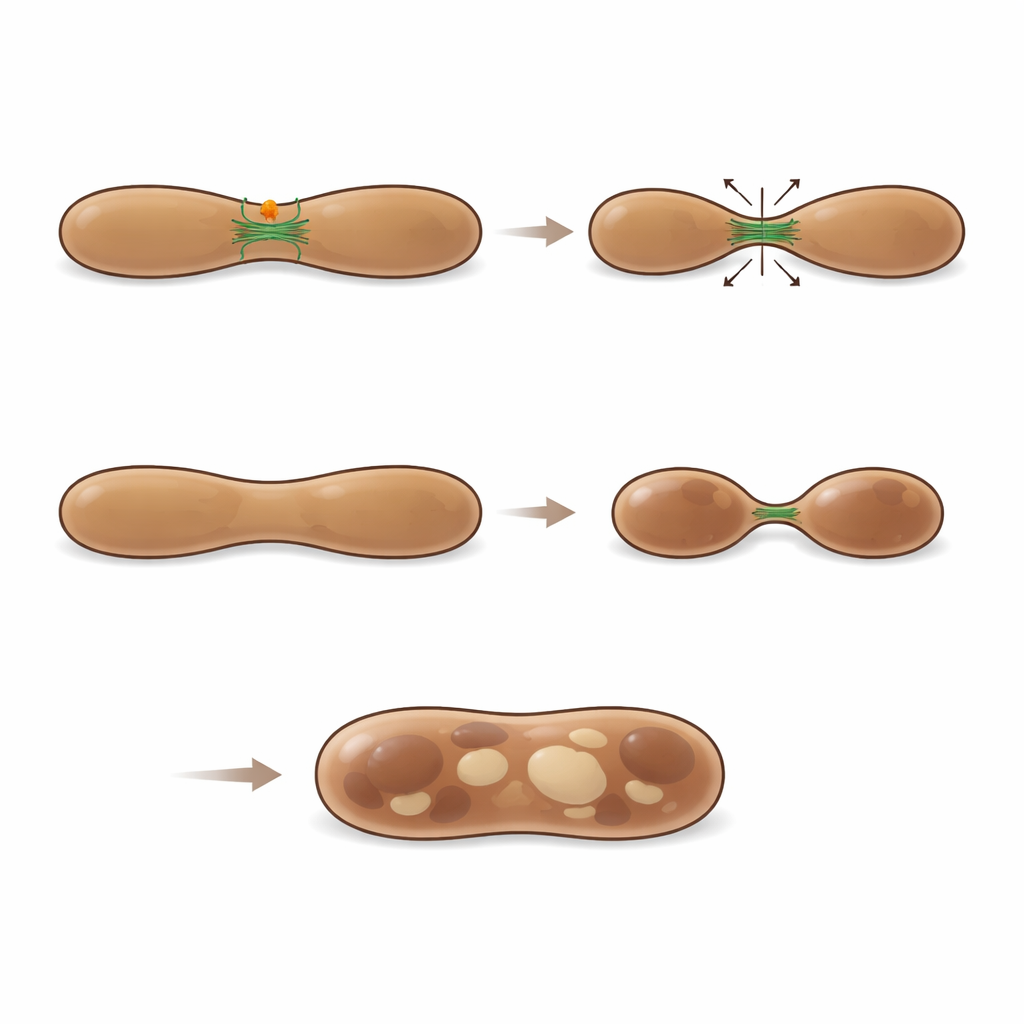
Équilibrer dégradation et construction avec les filaments d’actine
Le partenaire habituel de MFF dans la division mitochondriale est une autre protéine, DRP1. Cependant, dans les mélanosomes, DRP1 et MFF se chevauchent rarement, et l’inhibition de l’une ou l’autre a des conséquences très différentes. La perte de DRP1 atténuait principalement le programme génétique qui stimule la production de pigment. En revanche, l’absence de MFF agrandissait les mélanosomes précoces et déclenchait une forte augmentation des gènes et protéines liés aux lysosomes — centres de recyclage cellulaires — et aux enzymes cataboliques telles que la cathepsine B. Ces enzymes se concentraient à l’intérieur des mélanosomes, les rendant plus acides et plus enclin à dégrader leur propre machinerie pigmentaire. Lorsque la cathepsine B était également inhibée, les mélanosomes dans les cellules déficientes en MFF gonflaient encore davantage et s’accumulaient en grand nombre, montrant que la digestion interne renforcée sert normalement de mécanisme de secours pour éviter l’accumulation de granules pigmentaires dysfonctionnels et surdimensionnés.
Comment le squelette cellulaire aide à sectionner les granules de pigment
Pour comprendre comment MFF aide physiquement à la division des mélanosomes, les auteurs ont cartographié les protéines qui se lient à lui. Ils ont trouvé de nombreux régulateurs du cytosquelette d’actine, y compris des composants du complexe WASH et du dispositif nucléateur d’actine ARP2/3. L’imagerie montrait des filaments d’actine s’amassant aux « cols » des mélanosomes où siégeaient les ponctas de MFF, faisant office de pont entre des régions constrictes séparant deux compartiments en bourgeonnement. Lorsque des sous-unités clés d’ARP2/3 étaient inhibées, les mélanosomes précoces s’élargissaient de la même manière que lors de la perte de MFF, indiquant que la formation de filaments entraînée par l’actine est essentielle à une bonne division. L’inhibition de l’activité d’ARP2/3 effaçait également l’effet d’agrandissement des mélanosomes lié à la perte de MFF, reliant fortement la fonction de MFF à la dynamique de l’actine plutôt qu’à DRP1. Ensemble, ces résultats montrent que MFF recrute ou stabilise une machine de fission basée sur l’actine aux mélanosomes, leur permettant d’éliminer des composants inutiles et de progresser vers des organites pleinement pigmentés et de taille adéquate.
Ce que cela signifie pour les troubles de la pigmentation
L’étude montre que MFF, longtemps considéré comme un spécialiste de la division mitochondriale, agit aussi en dehors des mitochondries pour réguler la taille, la forme et la maturation des mélanosomes via une fission entraînée par l’actine. En l’absence de MFF, les granules pigmentaires précoces ne peuvent pas se diviser correctement, deviennent trop volumineux et ressemblent de plus en plus à des compartiments dégradatifs, poussant la cellule à augmenter leur dégradation. Ces observations aident à expliquer comment de gigantesques mélanosomes apparaissent dans certaines formes héréditaires d’albinisme et de maladies apparentées, et elles mettent en évidence MFF et ses partenaires d’actine comme cibles potentielles pour moduler la pigmentation ou comprendre comment les cellules pigmentaires dysfonctionnent en pathologie.
Citation: Magalhães Rebelo, A.P., Maracani, A., Greco, S. et al. MFF budding from mitochondria regulates melanosome size and maturation. Nat Commun 17, 3932 (2026). https://doi.org/10.1038/s41467-026-70572-3
Mots-clés: mélanosomes, mitochondries, protéine MFF, pigmentation, cytosquelette d’actine