Clear Sky Science · pl
MFF odszczepiający się od mitochondriów reguluje rozmiar i dojrzewanie melanosomów
Dlaczego maszyna tworząca kolor w komórkach ma znaczenie
Kolor naszej skóry, włosów i oczu zawdzięczamy drobnym fabrykom pigmentu w komórkach zwanym melanosomami. Utrzymanie tych struktur w odpowiednim rozmiarze i sprawności jest nie tylko ważne dla wyglądu, lecz także dla ochrony tkanek przed światłem słonecznym. W tym badaniu odkryto zaskakujący element wpływający na wzrost, podział i dojrzewanie melanosomów: białko znane przede wszystkim z kształtowania mitochondriów, elektrowni komórkowych. Pokazując, że to białko także formuje melanosomy, autorzy łączą organelle produkujące energię z tymi wytwarzającymi pigment, dając nowe wskazówki, jak kontrolowana jest barwa w zdrowiu i chorobie.
Nowa rola pomocnika mitochondrialnego
Melanosomy to wyspecjalizowane przegrody, które wytwarzają i magazynują melaninę — ciemny pigment chroniący komórki przed promieniowaniem ultrafioletowym. W toku rozwoju melanosomy przechodzą przez kilka stadiów, stopniowo napełniając się pigmentem, zanim zostaną przekazane sąsiednim komórkom skóry. W trakcie tej drogi ich błony ciągle się przebudowują — wydłużają się w tubule, odcinają małe fragmenty i czasem łączą ze sobą. Mechanizmy napędzające to przebudowywanie były do tej pory tylko częściowo poznane. Autorzy skupili się na białku zwanym czynnikiem szczepu mitochondrialnego (MFF), znanym z udziału w podziale mitochondriów. Ku ich zaskoczeniu MFF znaleziono nie tylko na mitochondriach, ale także na melanosomach, zwłaszcza w miejscach, gdzie te ziarna pigmentu się przewężają i wyglądają, jakby miały się podzielić.
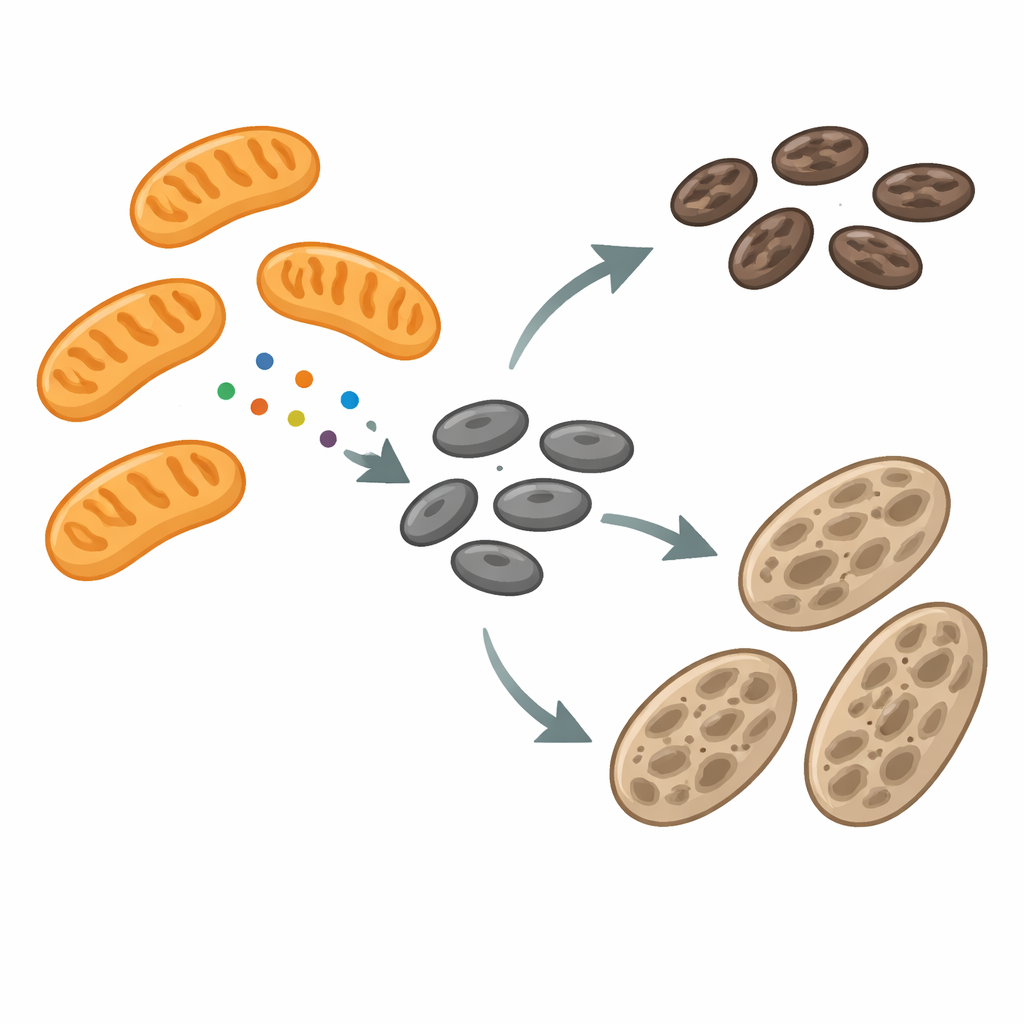
Gdy pigment stoi w miejscu, zmieniają się kontakty i sygnały
Aby zbadać komunikację między mitochondriami a melanosomami, zespół porównał normalne mysie komórki produkujące pigment z albinosowymi komórkami, które nie mogą wytwarzać melaniny z powodu wadliwego genu tyrozynazy. Komórki albinosowe gromadziły wiele niedojrzałych melanosomów i wykazywały częstsze fizyczne kontakty między melanosomami a mitochondriami. Sekwencjonowanie RNA i analiza białek ujawniły, że w tych komórkach podwyższona była aktywność genów i poziomów białek związanych z mitochondriami, w tym MFF zlokalizowanego w zewnętrznej błonie mitochondrialnej. Kształt mitochondriów wydawał się w dużej mierze normalny, podczas gdy melanosomy były jednocześnie większe i bardziej dynamiczne, często podlegały fuzji i podziałom. Ten wzorzec sugerował, że MFF może być przekierowywany z mitochondriów na melanosomy, gdzie mógłby wpływać na to, jak te organelle pigmentowe się dzielą i dojrzewają.
MFF przemieszcza się na melanosomy i kontroluje ich dzielenie
Wykorzystując mikroskopię o wysokiej rozdzielczości i immunogoldową mikroskopię elektronową, badacze wykryli MFF bezpośrednio na powierzchni melanosomów na wszystkich etapach ich cyklu życiowego. Obrazowanie w czasie rzeczywistym uchwyciło nawet MFF odchodzący z mitochondriów jako małe punkty, przemieszczające się na melanosomy oznaczone LAMP1 i LysoTrackerem. W tych miejscach błony melanosomów często się przewężały i zaciskały, tworząc tubule i pęcherzyki. Analiza ilościowa pokazała, że około jednej czwartej widocznych regionów podziału melanosomów było ozdobionych MFF, co sugeruje, że oznacza on istotną klasę zdarzeń rozdzielania. Gdy naukowcy zmniejszyli poziom MFF w komórkach pigmentowych, wczesne melanosomy stały się patologicznie powiększone, często przypominając struktury hybrydowe z cechami zarówno niedojrzałych, jak i bardziej zaawansowanych stadiów. Te rozdęte organelle wymieniały melaninę szerzej z wczesnymi markerami, a obrazowanie na żywo wykazało mniej udanych zdarzeń podziału, podkreślając, że MFF jest potrzebny do właściwego dzielenia i dojrzewania melanosomów.
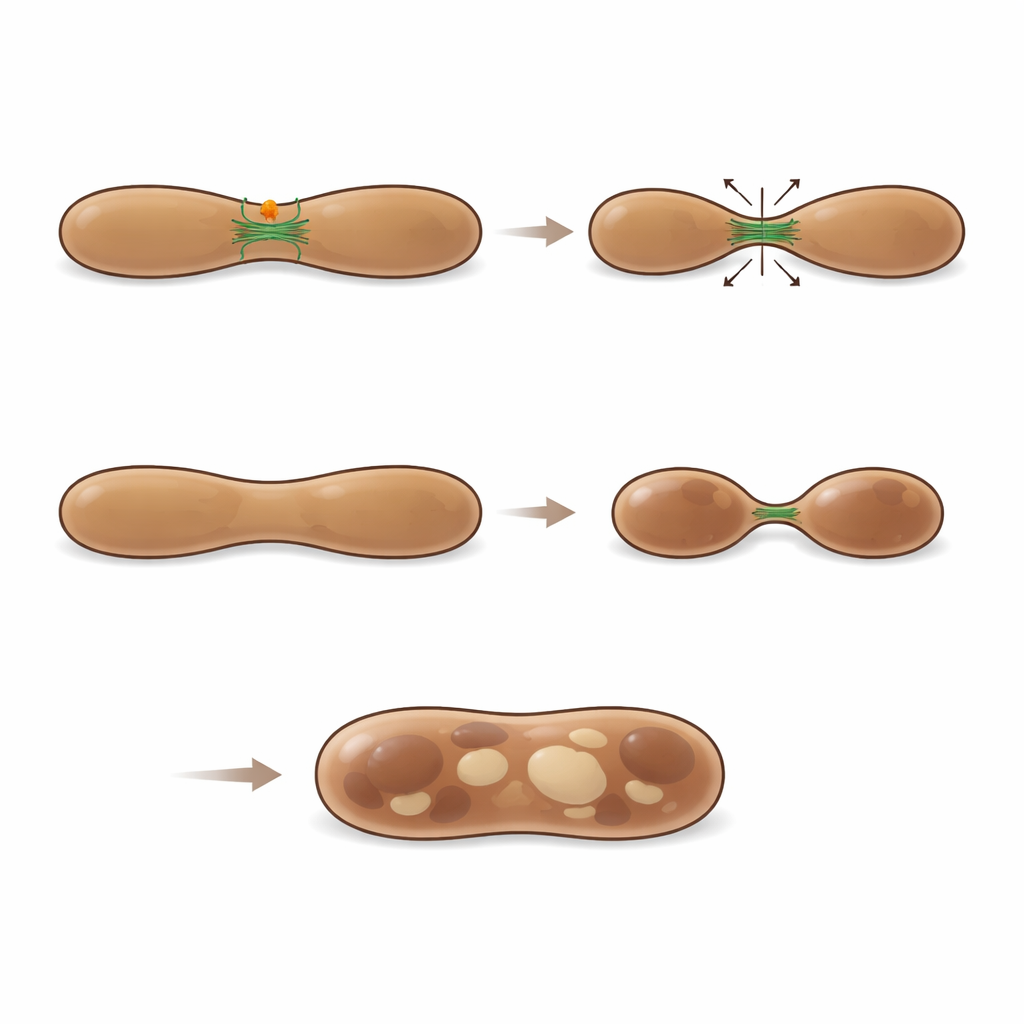
Równoważenie rozkładu i budowy za pomocą filamentów aktynowych
Zwykłym partnerem MFF w podziale mitochondriów jest inne białko, DRP1. Jednak w melanosomach DRP1 i MFF rzadko się pokrywały, a wyciszenie każdego z nich dało zupełnie różne skutki. Utrata DRP1 głównie osłabiła program genetyczny napędzający produkcję pigmentu. Natomiast utrata MFF powiększała wczesne melanosomy i wywoływała silny wzrost genów i białek powiązanych z lizosomami — komórkowymi centrami recyklingu — oraz z enzymami katabolicznymi, takimi jak katepsyna B. Enzymy te koncentrowały się wewnątrz melanosomów, czyniąc je bardziej kwaśnymi i bardziej skłonnymi do rozkładu własnej aparatury pigmentacyjnej. Gdy katepsyna B była również wyciszana, melanosomy w komórkach pozbawionych MFF pęcznieją jeszcze bardziej i gromadzą się w dużej liczbie, co pokazuje, że zwiększone wewnętrzne trawienie normalnie działa jako mechanizm zapobiegający nagromadzeniu się dysfunkcyjnych, nadmiernie dużych ziaren pigmentu.
Jak szkielet komórki pomaga rozcinać ziarna pigmentu
Aby zrozumieć, jak MFF fizycznie pomaga melanosomom się dzielić, autorzy zmapowali białka, które się z nim wiążą. Znaleźli liczne regulatory cytoszkieletu aktynowego, w tym komponenty kompleksu WASH oraz maszynerię nukleującą aktynę ARP2/3. Obrazowanie pokazało filamenty aktynowe skupiające się przy szyjkach melanosomów tam, gdzie widoczne były punkty MFF, łącząc przewężone regiony między dwoma rozwijającymi się przegrodami. Gdy wyciszono kluczowe podjednostki ARP2/3, wczesne melanosomy powiększały się w podobny sposób jak przy utracie MFF, co wskazuje, że formowanie filamentów napędzane przez aktynę jest niezbędne do prawidłowego rozdzielania. Hamowanie aktywności ARP2/3 także znosiło efekt powiększania melanosomów wywołany brakiem MFF, wiążąc funkcję MFF ściśle z dynamiką aktyny, a nie z DRP1. Razem te ustalenia ujawniają, że MFF rekrutuje lub stabilizuje opartą na aktynie maszynerię szczepową przy melanosomach, umożliwiając im odrzucanie niepotrzebnych komponentów i przejście do w pełni zabarwionych, prawidłowo wymiarowych organelli.
Co to oznacza dla zaburzeń pigmentacji
Badanie pokazuje, że MFF, długo uważany za specjalistę w podziale mitochondriów, działa także poza mitochondriami, regulując rozmiar, kształt i dojrzewanie melanosomów poprzez szczepienie napędzane aktyną. Gdy brakuje MFF, wczesne ziarna pigmentu nie potrafią się prawidłowo dzielić, rosną zbyt duże i coraz bardziej przypominają przegrody degradacyjne, co skłania komórkę do zwiększenia ich rozkładu. Te spostrzeżenia pomagają wyjaśnić, jak powstają olbrzymie melanosomy w niektórych dziedzicznych formach albinizmu i pokrewnych schorzeniach, oraz wskazują MFF i jego partnerów aktynowych jako potencjalne cele do modulowania pigmentacji lub zrozumienia, jak komórki pigmentowe zawodzą w chorobie.
Cytowanie: Magalhães Rebelo, A.P., Maracani, A., Greco, S. et al. MFF budding from mitochondria regulates melanosome size and maturation. Nat Commun 17, 3932 (2026). https://doi.org/10.1038/s41467-026-70572-3
Słowa kluczowe: melanosomy, mitochondria, białko MFF, pigmentacja, cytoszkielet aktynowy