Clear Sky Science · sv
En bakteries YopJ‑familj acetyltransferas dämpar värdens immunsvar genom Nε‑acetylation av JAK1
Hur bakterier tystar kroppens alarmsystem
När skadliga mikrober invaderar signalerar våra celler normalt genom att släppa ut kemiska budbärare som aktiverar kraftfulla antivirala och antibakteriella försvar. Denna studie avslöjar hur den pneumoniska bakterien Legionella pneumophila använder ett litet proteinvapen, kallat Lem17, för att dämpa det larmet vid källan. Genom att manipulera en central cellulär strömbrytare, JAK‑STAT‑vägen, kan bakterien smyga förbi immunförsvaret och föröka sig inne i våra celler.
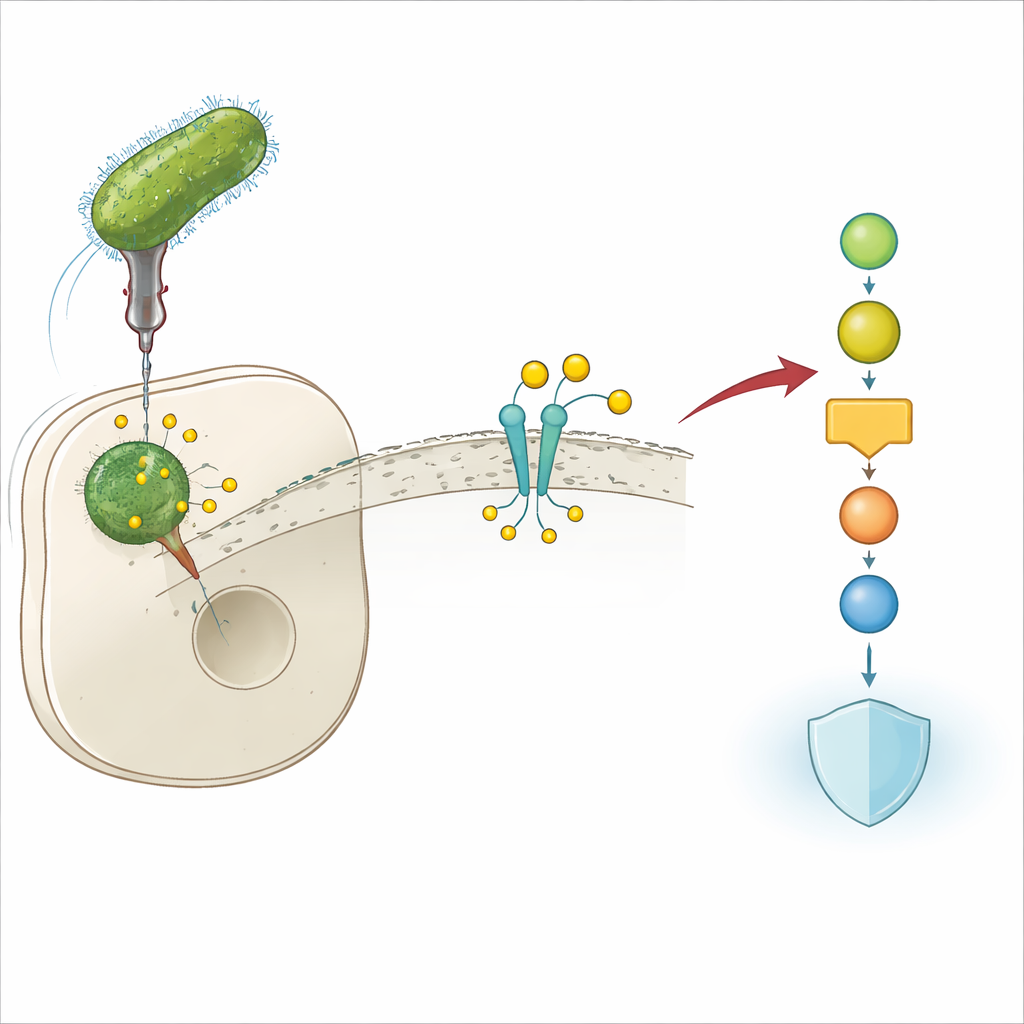
En bakterietrick för att undkomma försvar
Legionella pneumophila lever inne i mänskliga immunceller och kan orsaka en svår form av lunginflammation, känd som legionärssjuka. För att överleva i denna fientliga miljö injicerar bakterien många ”effektor”proteiner i värdcellen. Dessa effektorer omkopplar viktiga cellulära kretsar som annars skulle stoppa infektionen. Författarna fann att en av dessa effektorer, Lem17, är avgörande för Legionellas förmåga att växa i celler: när Lem17‑genen tas bort replikerar bakterierna dåligt i mus‑ och humana cellmodeller. Det tyder omedelbart på att Lem17 spelar en central roll i att avväpna värdens försvar.
Organismens signalomkopplare angrips
Våra celler förlitar sig på JAK‑STAT‑vägen för att översätta nödsignaler, såsom interferoner och interleukiner, till ett brett antiviralt och antibakteriellt svar. Dessa signalmolekyler binder till receptorer på cellytan, vilka sedan rekryterar ett enzym kallat JAK1. JAK1 aktiverar downstream STAT‑proteiner som rör sig in i kärnan och slår på hundratals skyddande gener. Forskarna visade att Lem17 specifikt riktar in sig på JAK1. Det binder direkt till JAK1 vid en region som normalt känner igen cytokinreceptorer, och konkurrerar i praktiken med dessa receptorer och blockerar JAK1 från att rekryteras korrekt när signalsubstanser anländer.
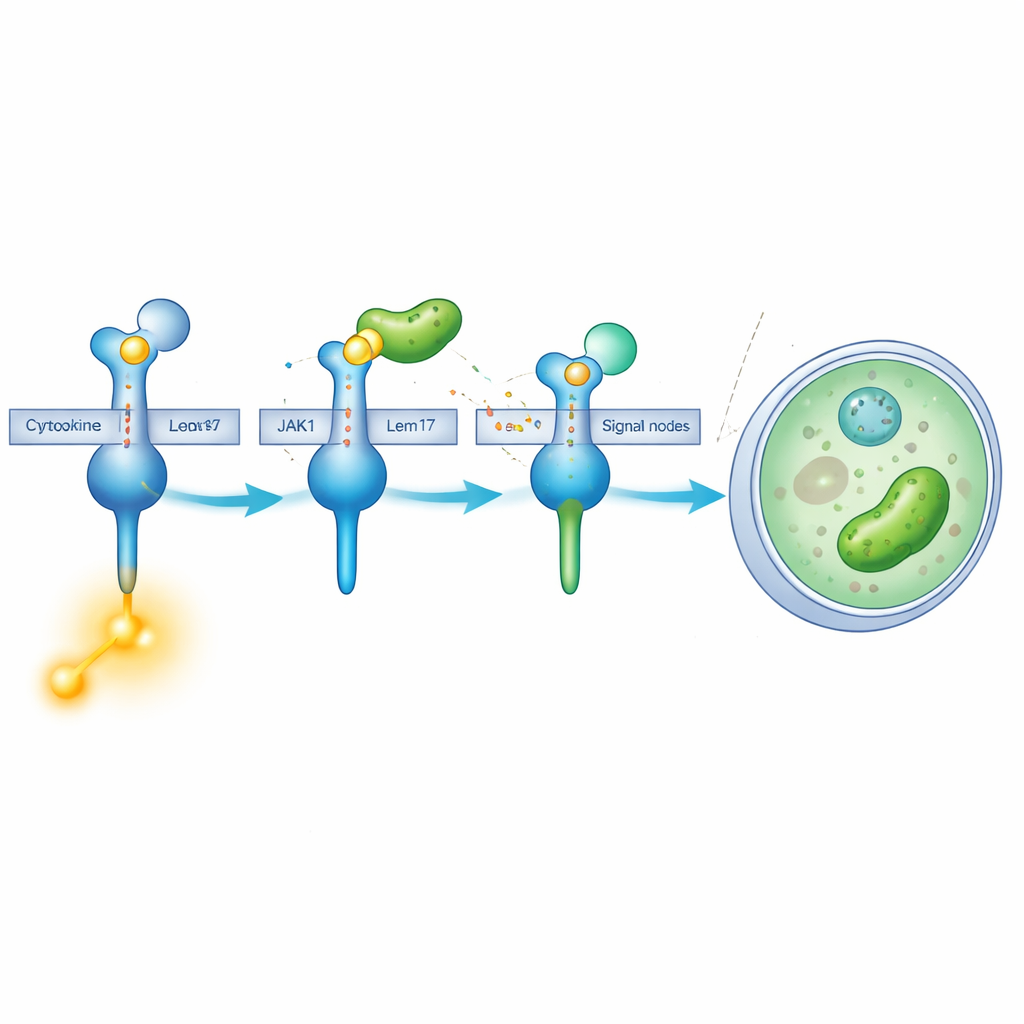
Kemisk ”maskering” av ett nyckelenzym
Lem17 gör mer än att bara stå i vägen. Det tillhör en familj av enzymer som fäster små acetylgrupper på andra proteiner. Med cellbaserade experiment och masspektrometri fann teamet att Lem17 pryder flera lysin‑platser på JAK1 med dessa acetylmarkörer. Många av de modifierade platserna klustras i två viktiga regioner: en som hjälper JAK1 att docka på receptorer och en annan som utför dess kinasfunktion — det kemiska steget som omvandlar signaler till handling. När JAK1 är acetylerat av Lem17 minskar dess förmåga att använda energimolekyler och fosforylera substrat kraftigt, vilket innebär att signaleringskaskaden effektivt stängs ner.
Värdens molekyl aktiverar det bakteriella vapnet
Studien förklarar också hur Lem17 själv aktiveras först inne i värdceller. Strukturarbete visade att Lem17 binder tätt till inositolhexafosfat (IP6), en liten molekyl som är rikligt förekommande i eukaryota celler men inte i bakterier. IP6 passar in i en positivt laddad ficka i Lem17 och låses på plats under en flexibel ”lock”‑domän. Utan IP6 kan Lem17 inte binda sitt acetyldonatormolekyl och förblir inaktivt. Detta krav säkerställer att Lem17:s acetyltransferasaktivitet slås på först efter att Legionella har tagit sig in i en värdcell, vilket förhindrar för tidig aktivering inne i bakterien.
Immun tystnad och bakterietillväxt
Genom att mäta genaktivitet och proteinmodifikationer i humana celler behandlade med interferon visade författarna att Lem17 kraftigt dämpar JAK‑STAT‑signaleringen: fosforylering av STAT1 och STAT2 minskar, och många interferon‑stimulerade gener slås inte på. Celler där JAK1 är borttaget eller tystat blir mer tillåtande för Legionella‑replikation, vilket återspeglar effekten av Lem17. Tillsammans stöder dessa resultat en tydlig modell: Legionella använder Lem17 för att binda och kemiskt maskera JAK1, blockera överföringen av cytokinsinaler och låta bakterien frodas inne i en skyddad cellnisch.
Varför detta är viktigt för infektioner och terapi
Detta arbete kartlägger ett precist sätt som en bakteriepatogen inaktiverar en av immunförsvarets centrala alarmomkopplare. Genom att visa att Lem17 både konkurrerar med receptorer om tillgång till JAK1 och kemiskt inaktiverar JAK1:s funktion, framhäver studien JAK‑STAT‑vägen som en viktig stridslinje vid bakteriella infektioner, inte bara vid virussjukdomar. Att förstå denna mekanism kan vägleda framtida strategier för att stärka värdförsvaret, exempelvis genom att designa läkemedel som blockerar Lem17:s interaktion med JAK1 eller förhindrar dess acetyltransferasaktivitet, och därigenom återställa cellens förmåga att initiera ett robust immunsvar.
Citering: Chen, TT., Zheng, SR., Yang, B. et al. A bacterial YopJ-family acetyltransferase suppresses host immune response by Nε-acetylation of JAK1. Nat Commun 17, 2910 (2026). https://doi.org/10.1038/s41467-026-69623-6
Nyckelord: Legionella pneumophila, JAK‑STAT‑signalering, bakteriella effektorer, proteacetylering, medfödd immunitet