Clear Sky Science · nl
Een bacteriële YopJ-familie acetyltransferase onderdrukt de immuunrespons van de gastheer door Nε-acetylatie van JAK1
Hoe bacteriën het alarmsysteem van het lichaam dempen
Wanneer schadelijke microben het lichaam binnendringen, geven onze cellen normaal gesproken alarm door chemische boodschappers vrij te geven die krachtige antivirale en antibacteriële verdedigingsmechanismen inschakelen. Deze studie onthult hoe de longontstekingveroorzakende bacterie Legionella pneumophila een klein eiwitwerktuigje, Lem17 genoemd, inzet om dat alarm bij de bron te dempen. Door te knoeien met een centraal cellulair schakelpunt, de JAK‑STAT-route, kan de bacterie langs de immuunafweer glippen en zich binnen onze cellen vermenigvuldigen.
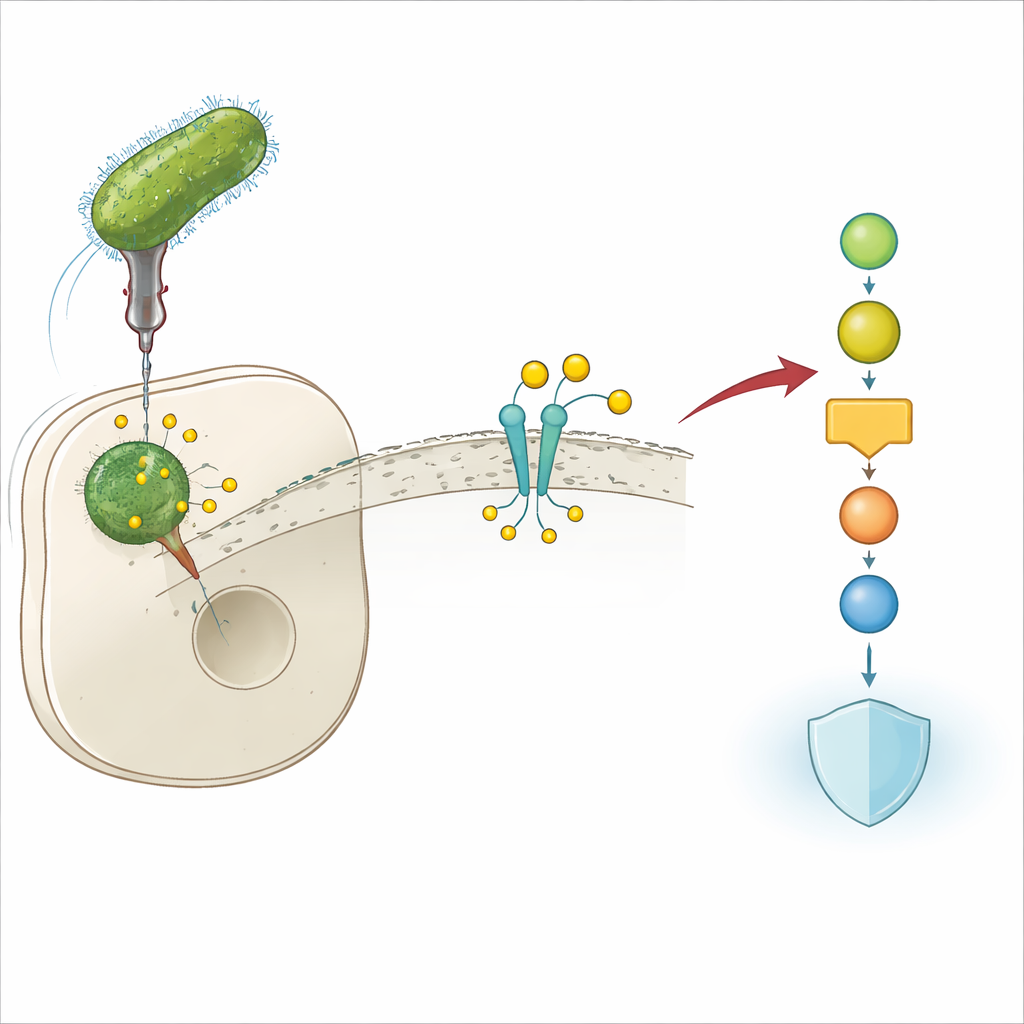
Een bacterietrick om afweer te ontwijken
Legionella pneumophila leeft in menselijke immuuncellen en kan een ernstige vorm van longontsteking veroorzaken, bekend als de ziekte van Legionairs. Om in deze vijandige omgeving te overleven spuit de bacterie veel "effector"-eiwitten in de gastheercel. Deze effectoren herschakelen belangrijke cellulaire circuits die de infectie anders zouden blokkeren. De auteurs ontdekten dat één van deze effectoren, Lem17, cruciaal is voor het vermogen van Legionella om binnen cellen te groeien: wanneer het gen voor Lem17 wordt verwijderd, repliceren de bacteriën slecht in muis- en menselijke cellijnen. Dit suggereert onmiddellijk dat Lem17 een centrale rol speelt bij het uitschakelen van de afweer van de gastheer.
Het signaal‑schakelpunt van het lichaam onder aanval
Onze cellen vertrouwen op de JAK‑STAT-route om noodsignalen, zoals interferonen en interleukines, om te zetten in een brede antivirale en antibacteriële respons. Deze signaalmoleculen binden aan receptoren op het celoppervlak, die vervolgens een enzym genaamd JAK1 rekruteren. JAK1 activeert downstream STAT-eiwitten die naar de kern bewegen en honderden beschermende genen inschakelen. De onderzoekers toonden aan dat Lem17 specifiek JAK1 als doelwit heeft. Het bindt rechtstreeks aan JAK1 op een regio die normaal cytokinereceptoren herkent, waardoor het feitelijk concurreert met die receptoren en verhindert dat JAK1 juist wordt aangetrokken wanneer waarschuwingssignalen binnenkomen.
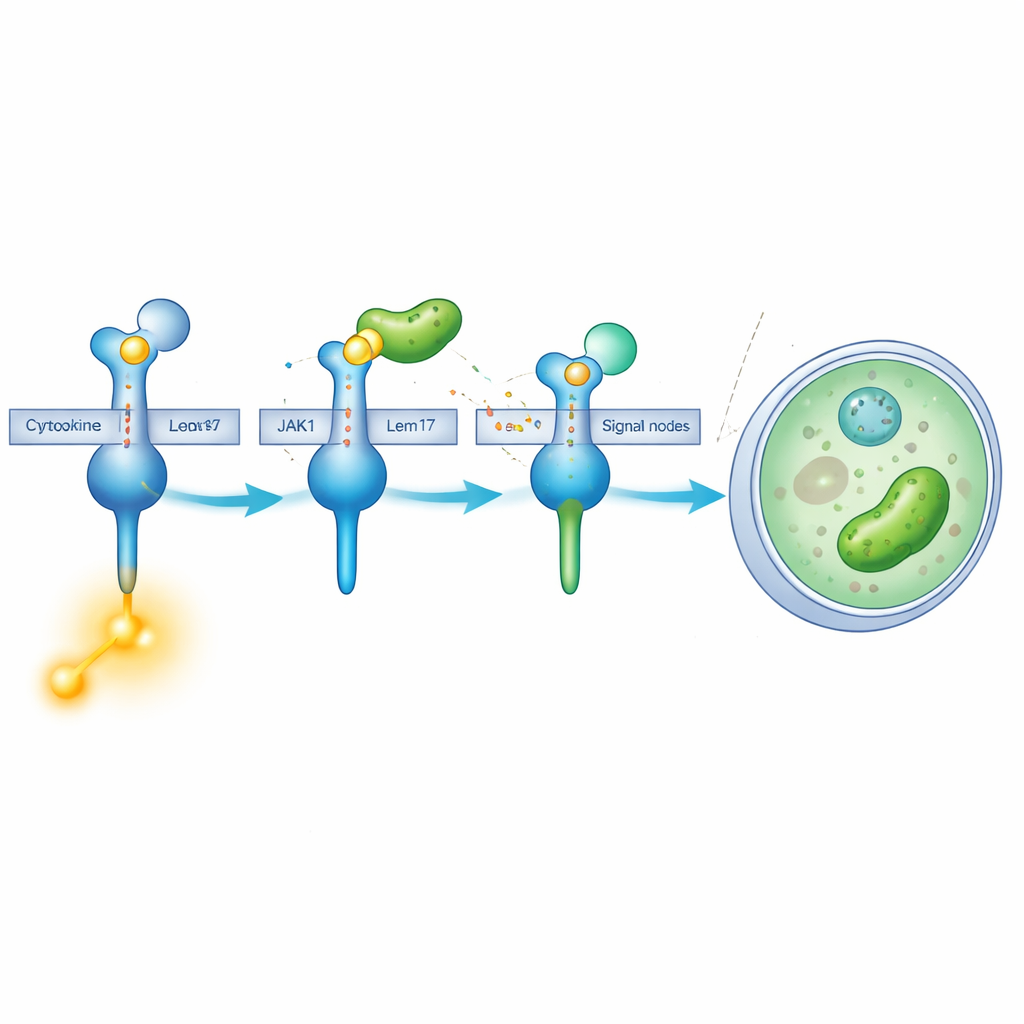
Chemische "maskering" van een sleuteleiwit
Lem17 doet meer dan alleen in de weg zitten. Het behoort tot een familie van enzymen die kleine acetylgroepen aan andere eiwitten koppelen. Met cellulaire experimenten en massaspectrometrie vond het team dat Lem17 meerdere lysineplaatsen op JAK1 voorziet van deze acetylmarkeringen. Veel van de gewijzigde locaties clusteren in twee belangrijke gebieden: één die helpt JAK1 aan receptoren te laten hechten en een ander dat zijn kinaserol vervult—de chemische stap die signalen omzet in actie. Wanneer JAK1 door Lem17 wordt geacetyleerd, neemt zijn vermogen om energierijke moleculen te gebruiken en substraten te fosforyleren sterk af, wat betekent dat de signaalcascade effectief wordt stilgelegd.
Een gastheer-molecuul zet het bacteriële wapen aan
De studie verklaart ook hoe Lem17 zelf alleen in gastheercellen wordt geactiveerd. Structureel werk liet zien dat Lem17 sterk bindt aan inositolhexafosfaat (IP6), een klein molecuul dat van nature overvloedig aanwezig is in eukaryote cellen maar niet in bacteriën. IP6 past in een positief geladen pocket in Lem17 en wordt vastgezet onder een flexibele "klep"-domein. Zonder IP6 kan Lem17 zijn acetyldonormolecuul niet binden en blijft het inactief. Deze vereiste zorgt ervoor dat de acetyltransferase-activiteit van Lem17 pas wordt ingeschakeld nadat Legionella een gastheercel is binnengegaan, waardoor voortijdige activatie binnen de bacterie wordt voorkomen.
Immuunsuppressie en bacteriële groei
Door genactiviteit en eiwitmodificaties te meten in humane cellen die met interferon werden behandeld, lieten de auteurs zien dat Lem17 de JAK‑STAT-signalisatie sterk dempt: fosforylering van STAT1 en STAT2 neemt af en veel interferon-gestimuleerde genen worden niet geactiveerd. Cellen waarin JAK1 is verwijderd of stilgelegd, worden meer permissief voor Legionella-replicatie, wat het effect van Lem17 nabootst. Samen ondersteunen deze resultaten een duidelijk model: Legionella gebruikt Lem17 om JAK1 te binden en chemisch te maskeren, waardoor de overdracht van cytokinesignalen wordt geblokkeerd en de bacterie kan gedijen in een beschermde cellulaire nis.
Waarom dit belangrijk is voor infectie en therapie
Dit werk onthult een nauwkeurige manier waarop een bacterieel pathogeen een van de centrale alarmschakelaars van het immuunsysteem uitschakelt. Door te laten zien dat Lem17 zowel concurreert met receptoren om toegang tot JAK1 als JAK1 chemisch inactief maakt, benadrukt de studie de JAK‑STAT-route als een belangrijk strijdtoneel bij bacteriële infecties, niet alleen bij virale ziektes. Inzicht in dit mechanisme kan toekomstige strategieën sturen om de afweer van de gastheer te versterken, bijvoorbeeld door medicijnen te ontwikkelen die de interactie tussen Lem17 en JAK1 blokkeren of de acetyltransferase-activiteit ervan verhinderen, en daarmee het vermogen van de cel herstellen om een robuuste immuunreactie op te bouwen.
Bronvermelding: Chen, TT., Zheng, SR., Yang, B. et al. A bacterial YopJ-family acetyltransferase suppresses host immune response by Nε-acetylation of JAK1. Nat Commun 17, 2910 (2026). https://doi.org/10.1038/s41467-026-69623-6
Trefwoorden: Legionella pneumophila, JAK-STAT-signaleringsroute, bacteriële effectoren, eiwitacetylatie, aangeboren immuniteit