Clear Sky Science · es
Una acetiltransferasa bacteriana de la familia YopJ suprime la respuesta inmune del hospedador por Nε-acetilación de JAK1
Cómo las bacterias silencian el sistema de alarma del organismo
Cuando microbios dañinos invaden, nuestras células normalmente lanzan la alarma liberando mensajeros químicos que activan poderosas defensas antivirales y antibacterianas. Este estudio revela cómo la bacteria causante de neumonía Legionella pneumophila despliega una pequeña herramienta proteica, llamada Lem17, para amortiguar esa alarma en su origen. Al manipular un interruptor celular central, la vía JAK‑STAT, la bacteria puede eludir las defensas inmunitarias y multiplicarse dentro de nuestras células.
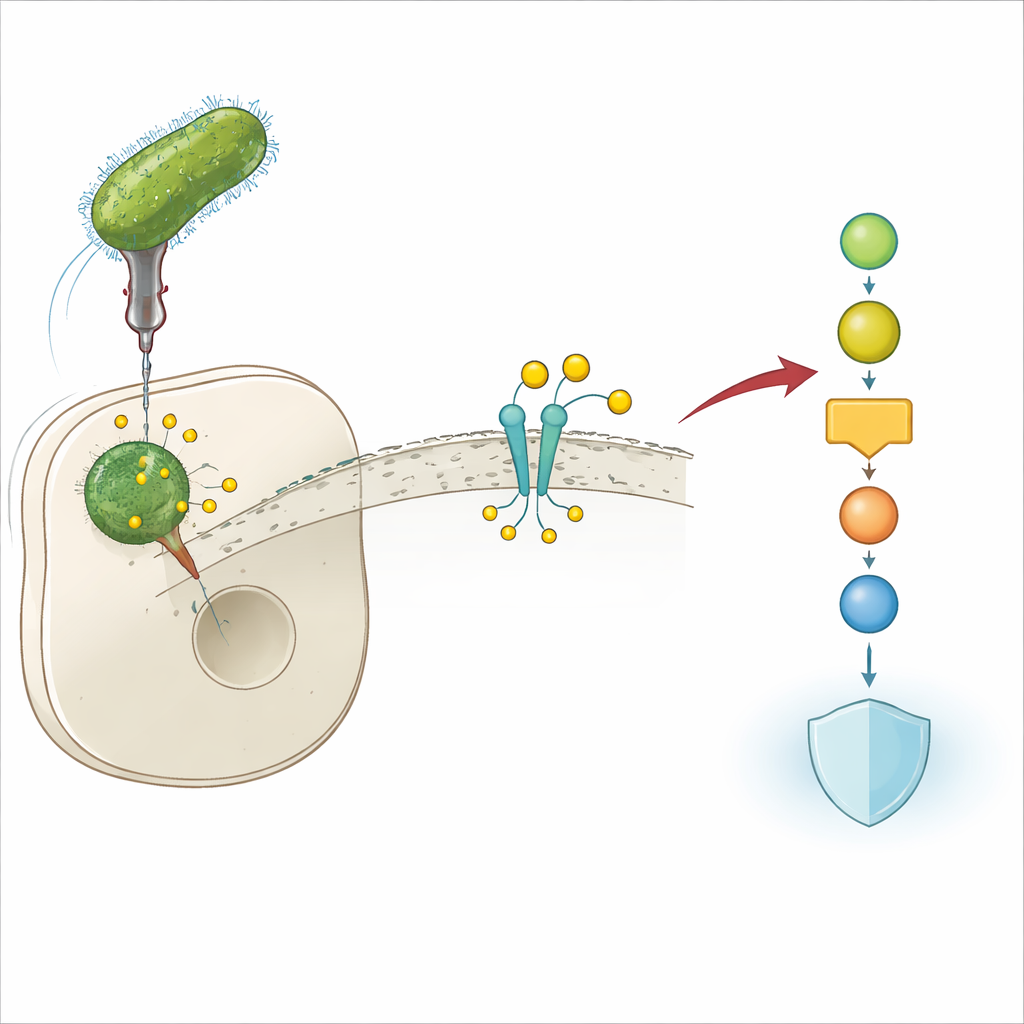
Un truco bacteriano para evadir las defensas
Legionella pneumophila vive dentro de células inmunitarias humanas y puede causar una forma grave de neumonía conocida como enfermedad del legionario. Para sobrevivir en este ambiente hostil, la bacteria inyecta numerosas proteínas “efectoras” en la célula hospedadora. Estos efectores reconectan circuitos celulares clave que de otro modo bloquearían la infección. Los autores descubrieron que uno de estos efectores, Lem17, es crucial para la capacidad de Legionella de crecer dentro de las células: cuando se elimina el gen de Lem17, las bacterias se replican mal en modelos celulares de ratón y humano. Esto sugiere de inmediato que Lem17 desempeña un papel central en desactivar las defensas del hospedador.
El interruptor de señalización del organismo bajo ataque
Nuestras células dependen de la vía JAK‑STAT para traducir señales de peligro, como interferones e interleucinas, en una amplia respuesta antiviral y antibacteriana. Estas moléculas señalizadoras se unen a receptores en la superficie celular, que a su vez reclutan una enzima llamada JAK1. JAK1 activa proteínas STAT aguas abajo que se trasladan al núcleo y encienden cientos de genes protectores. Los investigadores mostraron que Lem17 se dirige específicamente a JAK1. Se une directamente a JAK1 en una región que normalmente reconoce a los receptores de citocinas, compitiendo efectivamente con esos receptores y bloqueando el reclutamiento adecuado de JAK1 cuando llegan las señales de peligro.
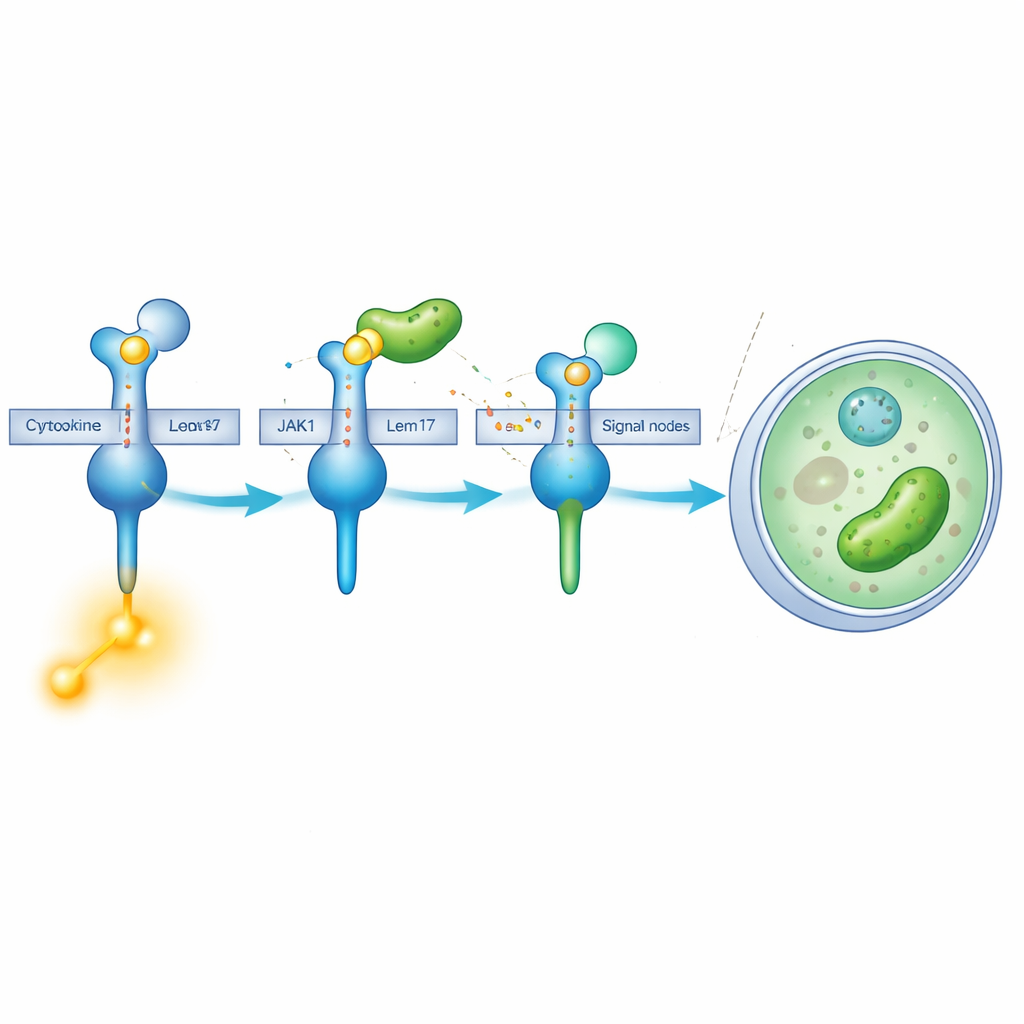
“Enmascaramiento” químico de una enzima clave
Lem17 hace más que simplemente interponerse. Pertenece a una familia de enzimas que añaden pequeños grupos acetilo a otras proteínas. Mediante experimentos en células y espectrometría de masas, el equipo encontró que Lem17 marca varios residuos de lisina en JAK1 con estas señales de acetilación. Muchos de los sitios modificados se concentran en dos regiones importantes: una que ayuda a JAK1 a acoplarse a los receptores y otra que realiza su función de quinasa—el paso químico que convierte las señales en acción. Cuando JAK1 es acetilado por Lem17, su capacidad para utilizar moléculas de energía y fosforilar sustratos disminuye drásticamente, lo que significa que la cascada de señalización queda efectivamente desactivada.
Una molécula del hospedador activa el arma bacteriana
El estudio también explica cómo Lem17 se activa solo dentro de las células del hospedador. Trabajos estructurales mostraron que Lem17 se une fuertemente al inositol hexafosfato (IP6), una pequeña molécula naturalmente abundante en células eucariotas pero no en bacterias. El IP6 encaja en un bolsillo cargado positivamente en Lem17 y se bloquea bajo un dominio “tapa” flexible. Sin IP6, Lem17 no puede unir su donador de acetilo y permanece inactiva. Este requisito asegura que la actividad acetiltransferasa de Lem17 se encienda solo después de que Legionella haya entrado en una célula hospedadora, evitando una activación prematura dentro de la propia bacteria.
Silenciamiento inmune y crecimiento bacteriano
Midiendo la actividad génica y las modificaciones proteicas en células humanas tratadas con interferón, los autores mostraron que Lem17 atenúa con fuerza la señalización JAK‑STAT: la fosforilación de STAT1 y STAT2 se reduce y muchos genes estimulados por interferón no se activan. Las células en las que JAK1 se elimina o silencia se vuelven más permisivas a la replicación de Legionella, imitando el efecto de Lem17. En conjunto, estos resultados apoyan un modelo claro: Legionella utiliza Lem17 para unirse y enmascarar químicamente JAK1, bloqueando el relevo de las señales de citocinas y permitiendo que la bacteria prospere dentro de un nicho celular protegido.
Por qué esto importa para la infección y la terapia
Este trabajo descubre una forma precisa en la que un patógeno bacteriano desactiva uno de los interruptores de alarma centrales del sistema inmunitario. Al mostrar que Lem17 tanto compite con los receptores por el acceso a JAK1 como inactiva químicamente la función de JAK1, el estudio destaca la vía JAK‑STAT como un campo de batalla clave en las infecciones bacterianas, no solo en las enfermedades virales. Comprender este mecanismo podría guiar estrategias futuras para reforzar las defensas del hospedador, por ejemplo diseñando fármacos que bloqueen la interacción de Lem17 con JAK1 o impidan su actividad acetiltransferasa, restaurando así la capacidad de la célula para montar una respuesta inmune robusta.
Cita: Chen, TT., Zheng, SR., Yang, B. et al. A bacterial YopJ-family acetyltransferase suppresses host immune response by Nε-acetylation of JAK1. Nat Commun 17, 2910 (2026). https://doi.org/10.1038/s41467-026-69623-6
Palabras clave: Legionella pneumophila, señalización JAK-STAT, efectores bacterianos, acetilación de proteínas, inmunidad innata