Clear Sky Science · it
Una acetiltransferasi batterica della famiglia YopJ sopprime la risposta immunitaria dell’ospite mediante Nε-acetilazione di JAK1
Come i batteri zittiscono il sistema di allarme del corpo
Quando microrganismi dannosi invadono, le nostre cellule normalmente danno l’allarme rilasciando messaggeri chimici che attivano potenti difese antivirali e antibatteriche. Questo studio rivela come il batterio causa-polmonite Legionella pneumophila impieghi un piccolo strumento proteico, chiamato Lem17, per attenuare quell’allarme alla fonte. Manomettendo un interruttore cellulare centrale, la via JAK‑STAT, il batterio riesce a eludere le difese immunitarie e a moltiplicarsi all’interno delle nostre cellule.
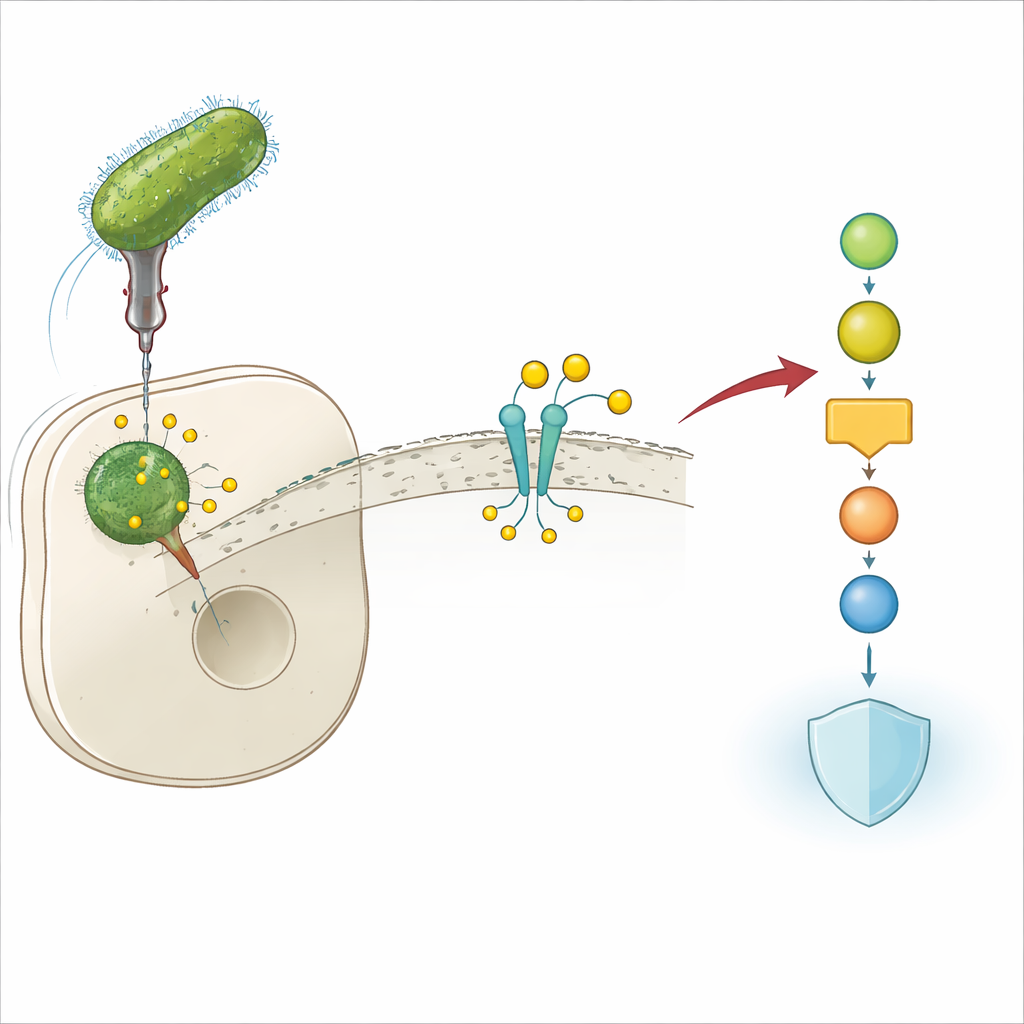
Un trucco batterico per sfuggire alle difese
Legionella pneumophila vive all’interno delle cellule immunitarie umane e può provocare una forma grave di polmonite nota come malattia dei legionari. Per sopravvivere in questo ambiente ostile, il batterio inietta nella cellula ospite numerose proteine “effettore”. Questi effettori riorientano circuiti cellulari chiave che altrimenti bloccherebbero l’infezione. Gli autori hanno scoperto che uno di questi effettori, Lem17, è cruciale per la capacità di Legionella di crescere all’interno delle cellule: quando il gene che codifica Lem17 viene eliminato, i batteri si replicano male nei modelli cellulari murini e umani. Ciò suggerisce immediatamente che Lem17 svolge un ruolo centrale nello disarmare le difese dell’ospite.
L’interruttore di segnalazione del corpo sotto attacco
Le nostre cellule si affidano alla via JAK‑STAT per tradurre segnali di allarme, come interferoni e interleuchine, in una risposta antivirale e antibatterica ampia. Queste molecole di segnalazione si legano a recettori sulla superficie cellulare, che quindi reclutano un enzima chiamato JAK1. JAK1 attiva le proteine STAT a valle, che si spostano nel nucleo e accendono centinaia di geni protettivi. I ricercatori hanno mostrato che Lem17 prende di mira specificamente JAK1. Si lega direttamente a JAK1 in una regione che normalmente riconosce i recettori delle citochine, competendo di fatto con quei recettori e impedendo il corretto reclutamento di JAK1 quando arrivano i segnali di pericolo.
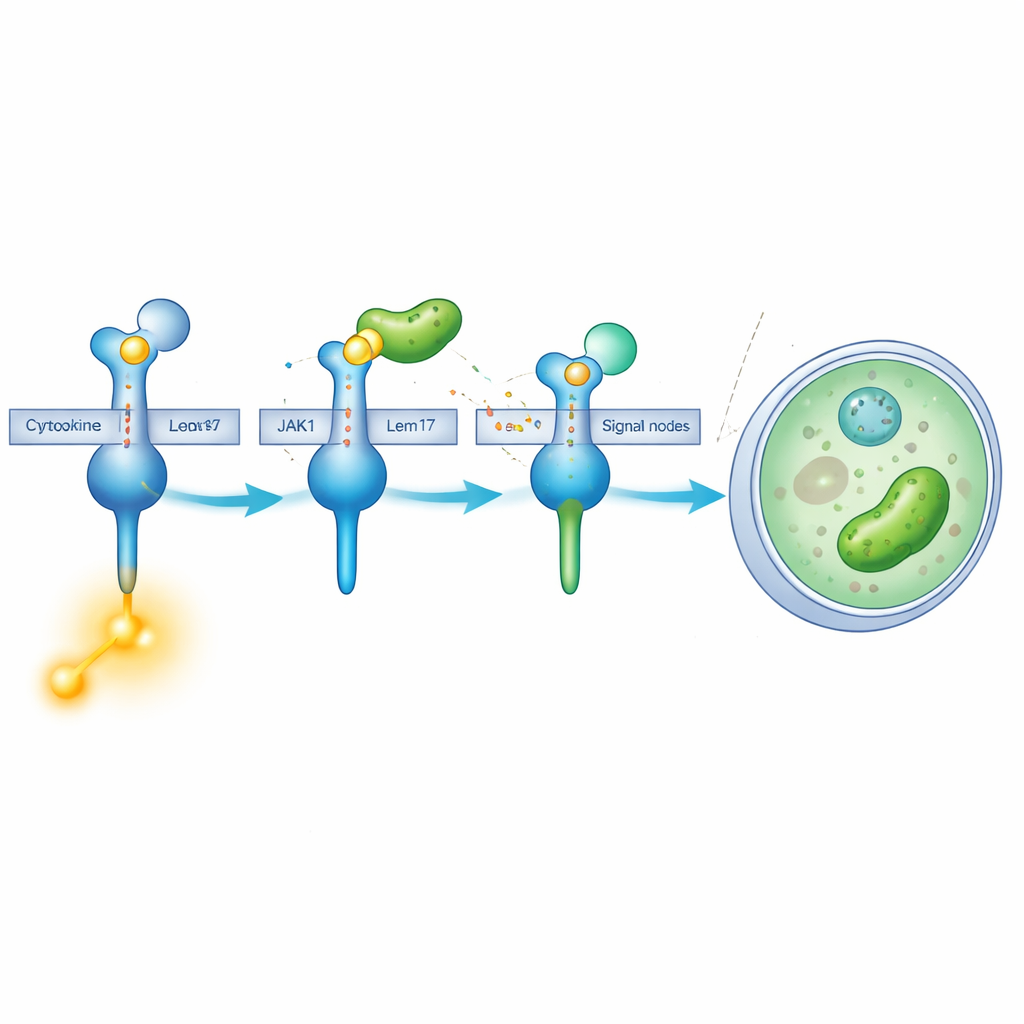
“Mascheramento” chimico di un enzima chiave
Lem17 non si limita a intralciare. Appartiene a una famiglia di enzimi che attaccano piccoli gruppi acetile su altre proteine. Attraverso esperimenti su cellule e spettrometria di massa, il gruppo ha scoperto che Lem17 aggiunge marcature acetile su diversi siti lisinici di JAK1. Molti dei siti modificati si concentrano in due regioni importanti: una che aiuta JAK1 ad agganciarsi ai recettori e un’altra che esegue la funzione chinasi—il passaggio chimico che trasforma i segnali in azione. Quando JAK1 è acetilato da Lem17, la sua capacità di utilizzare molecole energetiche e fosforilare substrati diminuisce drasticamente, il che significa che la cascata di segnalazione viene di fatto interrotta.
Una molecola dell’ospite attiva l’arma batterica
Lo studio spiega anche come Lem17 sia attivato solo all’interno delle cellule ospiti. Lavori strutturali hanno rivelato che Lem17 si lega strettamente all’inositolo esafosfato (IP6), una piccola molecola naturalmente abbondante nelle cellule eucariotiche ma non nei batteri. L’IP6 si inserisce in una tasca carica positivamente di Lem17 e si blocca sotto un dominio “coperchio” flessibile. Senza IP6, Lem17 non può legare il suo donatore di acetile e rimane inattivo. Questa necessità garantisce che l’attività acetiltransferasica di Lem17 si accenda solo dopo che Legionella è entrata in una cellula ospite, evitando un’attivazione prematura all’interno del batterio.
Silenziare l’immunità e crescita batterica
Misurando l’attività genica e le modificazioni proteiche in cellule umane trattate con interferone, gli autori hanno mostrato che Lem17 attenua fortemente la segnalazione JAK‑STAT: la fosforilazione di STAT1 e STAT2 è ridotta e molti geni stimolati dall’interferone non si attivano. Le cellule in cui JAK1 è rimosso o silenziato diventano più permissive alla replicazione di Legionella, imitandone l’effetto di Lem17. Nel loro insieme, questi risultati supportano un modello chiaro: Legionella usa Lem17 per legare e mascherare chimicamente JAK1, bloccando la trasmissione dei segnali delle citochine e permettendo al batterio di prosperare all’interno di una nicchia cellulare protetta.
Perché ciò è importante per infezione e terapia
Questo lavoro scopre un modo preciso in cui un patogeno batterico disabilita uno degli interruttori d’allarme centrali del sistema immunitario. Dimostrando che Lem17 sia in grado di competere con i recettori per l’accesso a JAK1 e di inattivare chimicamente la sua funzione, lo studio evidenzia la via JAK‑STAT come un campo di battaglia chiave nelle infezioni batteriche, non solo nelle malattie virali. Comprendere questo meccanismo potrebbe orientare strategie future per potenziare le difese dell’ospite, ad esempio progettando farmaci che blocchino l’interazione tra Lem17 e JAK1 o impediscano l’attività acetiltransferasica di Lem17, ripristinando così la capacità della cellula di montare una risposta immunitaria robusta.
Citazione: Chen, TT., Zheng, SR., Yang, B. et al. A bacterial YopJ-family acetyltransferase suppresses host immune response by Nε-acetylation of JAK1. Nat Commun 17, 2910 (2026). https://doi.org/10.1038/s41467-026-69623-6
Parole chiave: Legionella pneumophila, segnalazione JAK-STAT, effettori batterici, acetilazione delle proteine, immunità innata