Clear Sky Science · de
Ein bakterielles YopJ-Familien-Acetyltransferase unterdrückt die Wirtsimmunantwort durch Nε-Acetylierung von JAK1
Wie Bakterien das Alarmsystem des Körpers dämpfen
Wenn schädliche Mikroben eindringen, schlagen unsere Zellen normalerweise Alarm, indem sie chemische Botenstoffe freisetzen, die starke antivirale und antibakterielle Abwehrmechanismen aktivieren. Diese Studie zeigt, wie das die Lungenentzündung verursachende Bakterium Legionella pneumophila ein kleines Proteinwerkzeug namens Lem17 einsetzt, um diesen Alarm an der Quelle zu dämpfen. Indem es an einem zentralen zellulären Schalter, dem JAK‑STAT-Weg, manipuliert, kann das Bakterium an der Immunabwehr vorbeischlüpfen und sich in unseren Zellen vermehren.
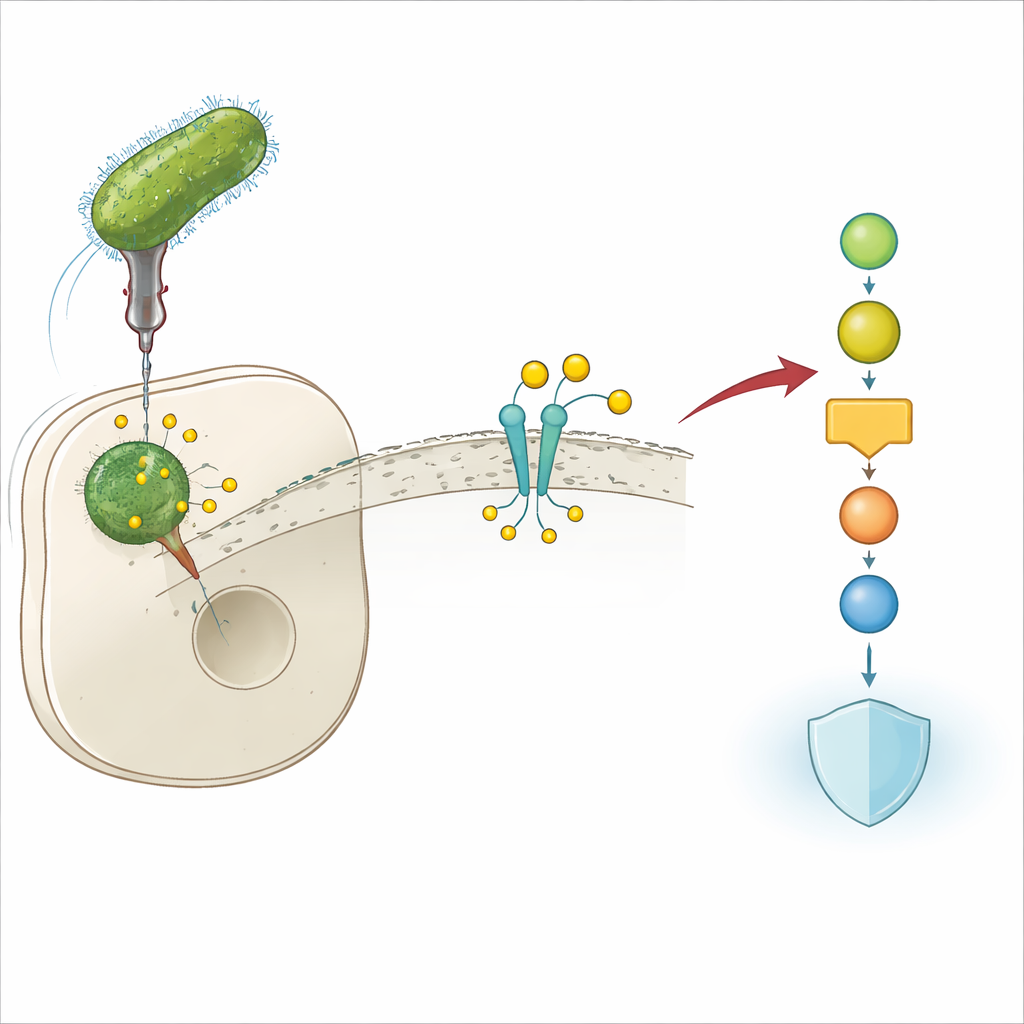
Ein bakteriischer Trick zur Umgehung der Abwehr
Legionella pneumophila lebt in menschlichen Immunzellen und kann eine schwere Form der Pneumonie hervorrufen, die als Legionärskrankheit bekannt ist. Um in dieser feindlichen Umgebung zu überleben, injiziert das Bakterium zahlreiche „Effektor“-Proteine in seine Wirtszelle. Diese Effektoren verkabeln wichtige zelluläre Schaltkreise um, die sonst eine Infektion verhindern würden. Die Autoren fanden heraus, dass einer dieser Effektoren, Lem17, entscheidend für die Fähigkeit von Legionella ist, in Zellen zu wachsen: Wird das Gen für Lem17 gelöscht, vermehren sich die Bakterien in Maus‑ und Humanzellmodellen schlecht. Das deutet unmittelbar darauf hin, dass Lem17 eine zentrale Rolle bei der Entwaffnung der Wirtsabwehr spielt.
Der Angriff auf den zellulären Signalschalter
Unsere Zellen sind auf den JAK‑STAT-Weg angewiesen, um Alarmsignale wie Interferone und Interleukine in eine umfassende antivirale und antibakterielle Antwort umzusetzen. Diese Signalmoleküle binden an Rezeptoren an der Zelloberfläche, welche dann ein Enzym namens JAK1 rekrutieren. JAK1 aktiviert downstream liegende STAT‑Proteine, die in den Zellkern wandern und Hunderte schützender Gene einschalten. Die Forscher zeigten, dass Lem17 gezielt JAK1 anvisiert. Es bindet direkt an JAK1 in einer Region, die normalerweise Zytokinrezeptoren erkennt, konkurriert effektiv mit diesen Rezeptoren und verhindert so, dass JAK1 bei Eintreffen von Gefahrensignalen korrekt rekrutiert wird.
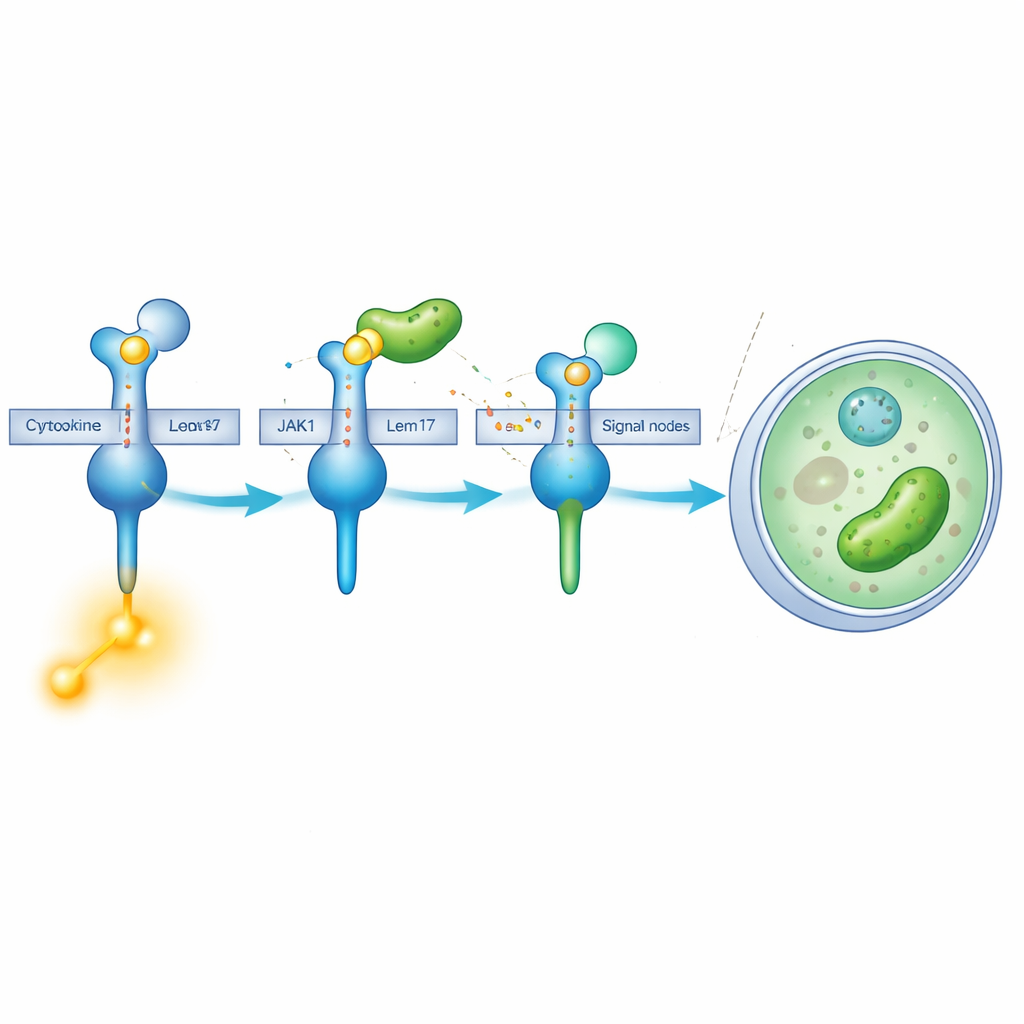
Chemisches „Maskieren“ eines Schlüsselenzyms
Lem17 macht mehr, als nur im Weg zu stehen. Es gehört zu einer Enzymfamilie, die kleinen Acetylgruppen an andere Proteine anhängt. Mithilfe von zellbasierten Experimenten und Massenspektrometrie fanden die Forschenden heraus, dass Lem17 mehrere Lysinstellen an JAK1 mit diesen Acetylmarken versieht. Viele der modifizierten Stellen gruppieren sich in zwei wichtigen Bereichen: einem, das JAK1 beim Andocken an Rezeptoren hilft, und einem anderen, das seine Kinasefunktion ausführt — der chemische Schritt, der Signale in Aktion umsetzt. Wenn JAK1 von Lem17 acetylriert wird, sinkt seine Fähigkeit, Energieträger zu nutzen und Substrate zu phosphorylieren, deutlich, was effektiv das Signalkaskaden-System abschaltet.
Ein Wirtsmolekül schaltet die bakterielle Waffe ein
Die Studie erklärt auch, wie Lem17 selbst nur innerhalb von Wirtszellen aktiviert wird. Strukturbiologische Arbeiten zeigten, dass Lem17 fest an Inositolhexaphosphat (IP6) bindet, ein kleines Molekül, das in eukaryotischen Zellen reichlich vorkommt, aber nicht in Bakterien. IP6 sitzt in einer positiv geladenen Tasche in Lem17 und klemmt sich unter eine flexible „Deckel“-Domäne. Ohne IP6 kann Lem17 seinen Acetylspender nicht binden und bleibt inaktiv. Diese Voraussetzung stellt sicher, dass die Acetyltransferase-Aktivität von Lem17 erst eingeschaltet wird, nachdem Legionella in eine Wirtszelle eingedrungen ist, und verhindert eine vorzeitige Aktivierung innerhalb des Bakteriums.
Immunsuppression und bakterielles Wachstum
Durch Messung von Genaktivität und Proteinmodifikationen in menschlichen Zellen, die mit Interferon behandelt wurden, zeigten die Autoren, dass Lem17 die JAK‑STAT-Signalisierung stark dämpft: Die Phosphorylierung von STAT1 und STAT2 ist reduziert, und viele interferon‑abhängige Gene werden nicht eingeschaltet. Zellen, in denen JAK1 entfernt oder stummgeschaltet ist, werden empfänglicher für die Vermehrung von Legionella, was den Effekt von Lem17 nachahmt. Zusammengenommen stützen diese Ergebnisse ein klares Modell: Legionella nutzt Lem17, um JAK1 zu binden und chemisch zu maskieren, die Weiterleitung von Zytokinsignalen zu blockieren und dem Bakterium das Gedeihen in einer geschützten zellulären Nische zu ermöglichen.
Warum das für Infektionen und Therapie wichtig ist
Diese Arbeit offenbart einen präzisen Mechanismus, mit dem ein bakterieller Erreger einen der zentralen Alarmschalter des Immunsystems außer Gefecht setzt. Indem gezeigt wird, dass Lem17 sowohl mit Rezeptoren um den Zugang zu JAK1 konkurriert als auch JAK1 chemisch inaktiviert, hebt die Studie den JAK‑STAT-Weg als ein zentrales Schlachtfeld bei bakteriellen Infektionen hervor — nicht nur bei Viruskrankheiten. Das Verständnis dieses Mechanismus könnte künftige Strategien leiten, die Wirtsabwehr zu stärken, zum Beispiel durch die Entwicklung von Wirkstoffen, die die Wechselwirkung zwischen Lem17 und JAK1 blockieren oder seine Acetyltransferase‑Aktivität verhindern und so die Fähigkeit der Zelle wiederherstellen, eine robuste Immunantwort zu entfalten.
Zitation: Chen, TT., Zheng, SR., Yang, B. et al. A bacterial YopJ-family acetyltransferase suppresses host immune response by Nε-acetylation of JAK1. Nat Commun 17, 2910 (2026). https://doi.org/10.1038/s41467-026-69623-6
Schlüsselwörter: Legionella pneumophila, JAK-STAT-Signalübertragung, bakterielle Effektorproteine, Proteinacetylierung, angeborene Immunität