Clear Sky Science · pt
Uma acetiltransferase bacteriana da família YopJ suprime a resposta imune do hospedeiro por Nε-acetilação de JAK1
Como bactérias silenciam o sistema de alarme do corpo
Quando micróbios nocivos invadem, nossas células normalmente soam o alarme liberando mensageiros químicos que ativam defesas antivirais e antibacterianas potentes. Este estudo revela como a bactéria causadora de pneumonia Legionella pneumophila emprega uma pequena ferramenta proteica, chamada Lem17, para abafar esse alarme na sua origem. Ao mexer em um interruptor celular central, a via JAK‑STAT, a bactéria consegue escapar das defesas imunes e multiplicar-se dentro de nossas células.
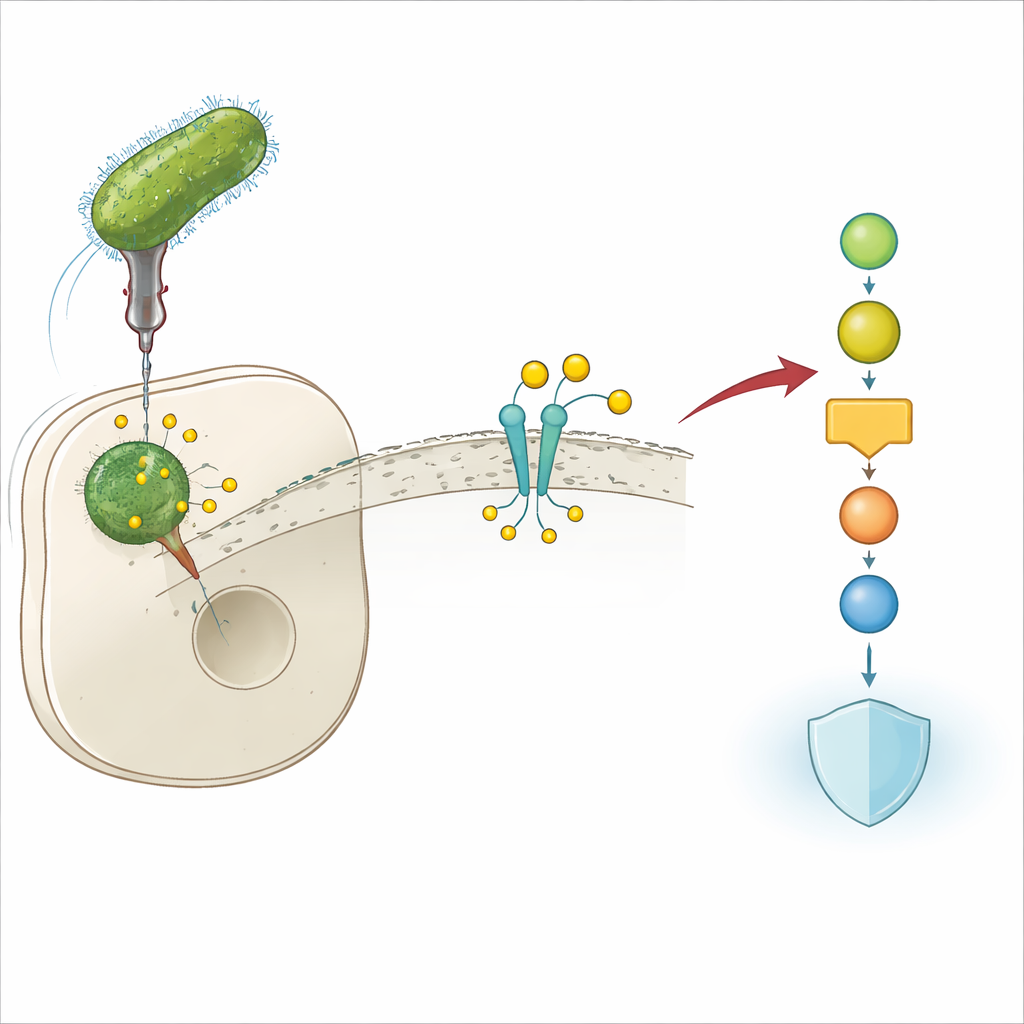
Um truque bacteriano para evitar defesas
Legionella pneumophila vive dentro de células do sistema imune humano e pode causar uma forma grave de pneumonia conhecida como doença dos legionários. Para sobreviver nesse ambiente hostil, a bactéria injeta muitas proteínas "efetoras" na célula hospedeira. Esses efetores reprogramam circuitos celulares chave que, de outra forma, bloqueiam a infecção. Os autores descobriram que um desses efetores, Lem17, é crucial para a capacidade da Legionella de crescer dentro das células: quando o gene de Lem17 é deletado, as bactérias se replicam mal em modelos celulares de camundongo e humano. Isso sugeriu imediatamente que Lem17 desempenha um papel central no desarmamento das defesas do hospedeiro.
O interruptor de sinalização do organismo sob ataque
Nossas células dependem da via JAK‑STAT para traduzir sinais de perigo, como interferons e interleucinas, em uma ampla resposta antiviral e antibacteriana. Essas moléculas sinalizadoras ligam-se a receptores na superfície celular, que então recrutam uma enzima chamada JAK1. JAK1 ativa proteínas STAT a jusante, que migram para o núcleo e ativam centenas de genes de proteção. Os pesquisadores demonstraram que Lem17 mira especificamente JAK1. Ele se liga diretamente a JAK1 em uma região que normalmente reconhece receptores de citocinas, efetivamente competindo com esses receptores e impedindo que JAK1 seja recrutado adequadamente quando sinais de perigo chegam.
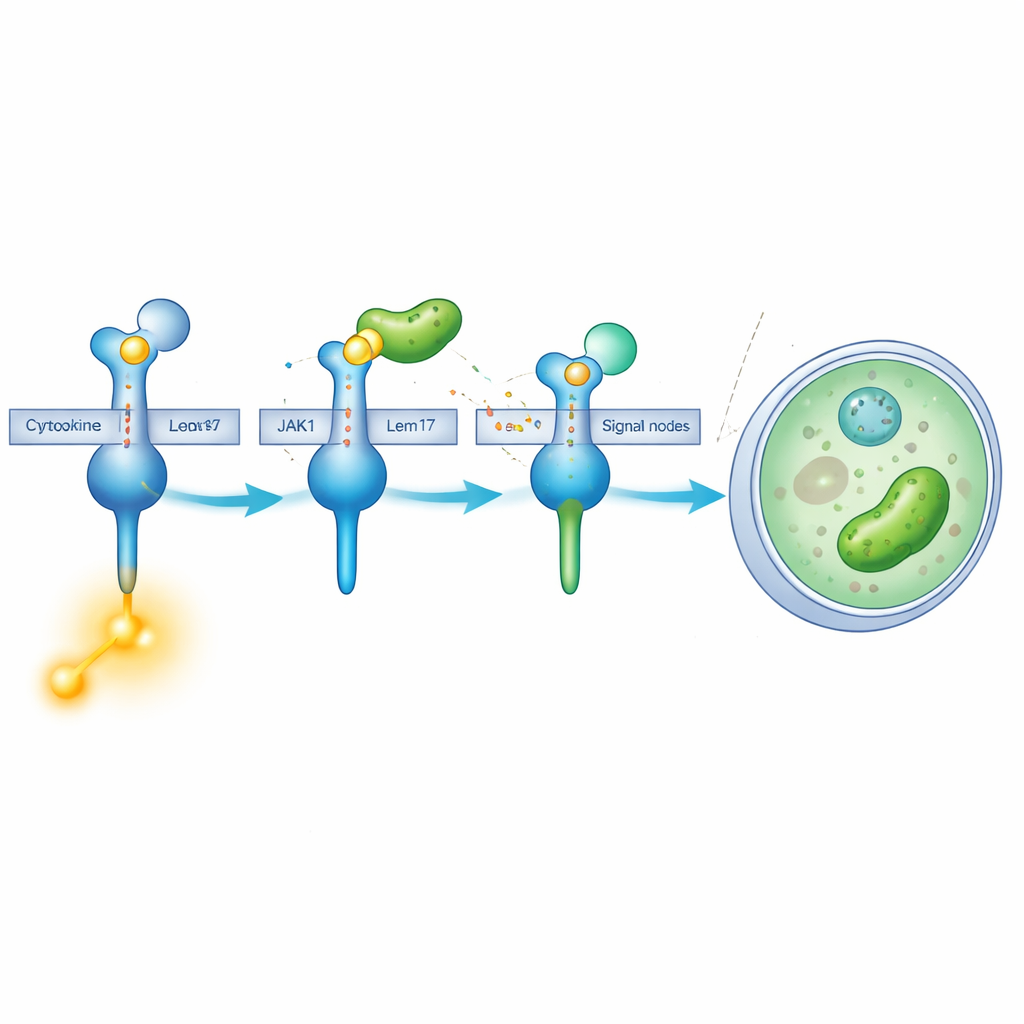
“Mascaramento” químico de uma enzima chave
Lem17 faz mais do que apenas atrapalhar. Pertence a uma família de enzimas que adicionam pequenos grupos acetil a outras proteínas. Usando experimentos em células e espectrometria de massa, a equipe encontrou que Lem17 decora vários sítios de lisina em JAK1 com essas marcas de acetil. Muitos dos sítios modificados se agrupam em duas regiões importantes: uma que ajuda JAK1 a acoplar-se aos receptores e outra que desempenha sua função quinase — o passo químico que transforma sinais em ação. Quando JAK1 é acetilado por Lem17, sua capacidade de utilizar moléculas de energia e fosforilar substratos cai drasticamente, o que significa que a cascata de sinalização é efetivamente desligada.
Molécula do hospedeiro ativa a arma bacteriana
O estudo também explica como Lem17 é ativado apenas dentro das células do hospedeiro. Trabalhos estruturais revelaram que Lem17 se liga firmemente ao inositol hexafosfato (IP6), uma pequena molécula naturalmente abundante em células eucarióticas, mas não em bactérias. O IP6 se encaixa em um bolso carregado positivamente em Lem17 e se fixa sob um domínio “tampa” flexível. Sem IP6, Lem17 não consegue ligar seu doador de acetil e permanece inativo. Essa exigência garante que a atividade acetiltransferase de Lem17 seja ligada somente depois que a Legionella entrou numa célula hospedeira, evitando ativação prematura dentro da própria bactéria.
Silenciamento imune e crescimento bacteriano
Medições de atividade gênica e modificações proteicas em células humanas tratadas com interferon mostraram que Lem17 reduz fortemente a sinalização JAK‑STAT: a fosforilação de STAT1 e STAT2 é reduzida, e muitos genes estimulados por interferon deixam de ser ativados. Células nas quais JAK1 é removido ou silenciado tornam-se mais permissivas à replicação de Legionella, imitando o efeito de Lem17. Em conjunto, esses resultados sustentam um modelo claro: Legionella usa Lem17 para se ligar e mascarar quimicamente JAK1, bloqueando a transmissão dos sinais de citocinas e permitindo que a bactéria prospere dentro de um nicho celular protegido.
Por que isso importa para infecção e terapia
Este trabalho revela uma maneira precisa pela qual um patógeno bacteriano desativa um dos interruptores centrais do sistema imunológico. Ao mostrar que Lem17 tanto compete com receptores pelo acesso a JAK1 quanto inativa quimicamente sua função, o estudo destaca a via JAK‑STAT como um campo de batalha chave em infecções bacterianas, não apenas em doenças virais. Compreender esse mecanismo pode orientar estratégias futuras para reforçar as defesas do hospedeiro, por exemplo projetando fármacos que bloqueiem a interação de Lem17 com JAK1 ou que impeçam sua atividade acetiltransferase, restaurando assim a capacidade da célula de montar uma resposta imune robusta.
Citação: Chen, TT., Zheng, SR., Yang, B. et al. A bacterial YopJ-family acetyltransferase suppresses host immune response by Nε-acetylation of JAK1. Nat Commun 17, 2910 (2026). https://doi.org/10.1038/s41467-026-69623-6
Palavras-chave: Legionella pneumophila, Sinalização JAK-STAT, efetores bacterianos, acetilação de proteínas, imunidade inata