Clear Sky Science · fr
Une acétyltransférase bactérienne de la famille YopJ supprime la réponse immunitaire de l’hôte par Nε-acétylation de JAK1
Comment les bactéries étouffent le système d’alarme du corps
Lorsque des microbes nuisibles envahissent, nos cellules déclenchent normalement l’alarme en libérant des messagers chimiques qui activent des défenses antivirales et antibactériennes puissantes. Cette étude révèle comment la bactérie responsable de pneumonies, Legionella pneumophila, déploie un petit outil protéique, nommé Lem17, pour étouffer cette alarme à sa source. En trafiquant un interrupteur cellulaire central, la voie JAK‑STAT, la bactérie peut contourner les défenses immunitaires et se multiplier à l’intérieur de nos cellules.
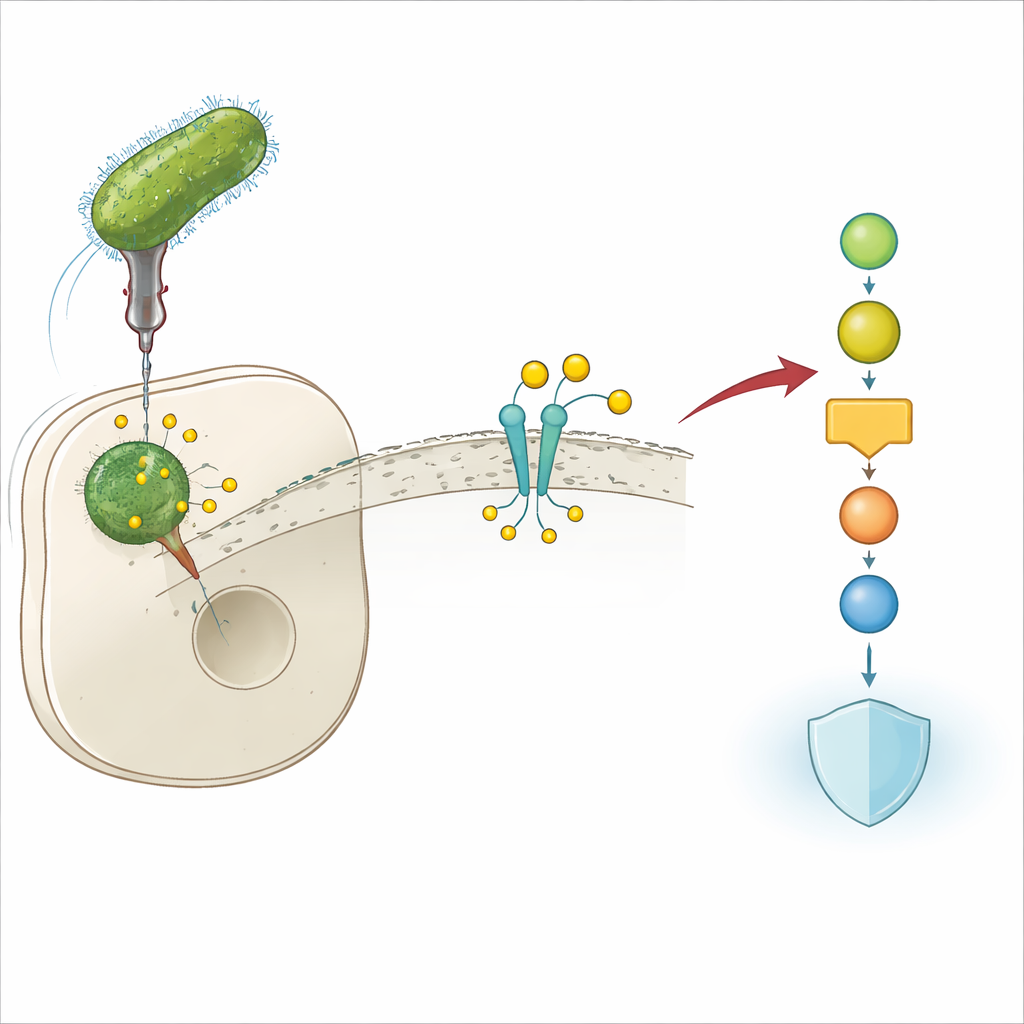
Une ruse bactérienne pour échapper aux défenses
Legionella pneumophila vit à l’intérieur des cellules immunitaires humaines et peut provoquer une forme grave de pneumonie connue sous le nom de maladie du légionnaire. Pour survivre dans cet environnement hostile, la bactérie injecte de nombreuses protéines « effectrices » dans sa cellule hôte. Ces effecteurs reconfigurent des circuits cellulaires clés qui, autrement, bloqueraient l’infection. Les auteurs ont découvert que l’un de ces effecteurs, Lem17, est crucial pour la capacité de Legionella à croître à l’intérieur des cellules : lorsque le gène codant Lem17 est supprimé, les bactéries se répliquent mal dans des modèles cellulaires murins et humains. Cela suggère immédiatement que Lem17 joue un rôle central dans le désarmement des défenses de l’hôte.
L’interrupteur de signalisation du corps attaqué
Nos cellules s’appuient sur la voie JAK‑STAT pour traduire les signaux de détresse, tels que les interférons et les interleukines, en une large réponse antivirale et antibactérienne. Ces molécules de signalisation se lient à des récepteurs à la surface cellulaire, qui recrutent alors une enzyme appelée JAK1. JAK1 active des protéines STAT en aval qui se déplacent vers le noyau et déclenchent des centaines de gènes protecteurs. Les chercheurs ont montré que Lem17 cible spécifiquement JAK1. Il se lie directement à JAK1 dans une région qui reconnaît normalement les récepteurs de cytokines, faisant concurrence à ces récepteurs et empêchant efficacement le recrutement correct de JAK1 lorsque les signaux de danger arrivent.
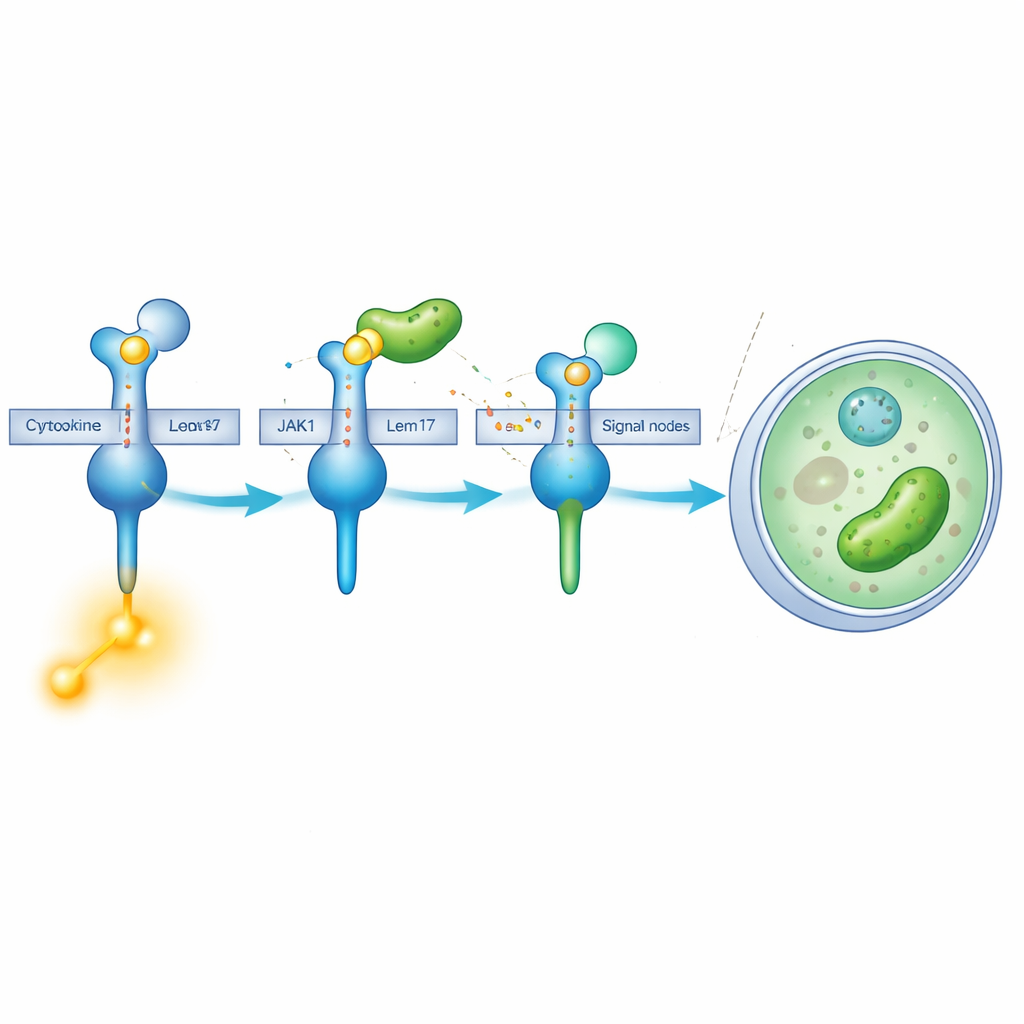
« Masquage » chimique d’une enzyme clé
Lem17 ne se contente pas de faire obstruction. Il appartient à une famille d’enzymes qui fixent de petits groupes acétyle sur d’autres protéines. À l’aide d’expériences cellulaires et de spectrométrie de masse, l’équipe a constaté que Lem17 marque plusieurs sites lysine de JAK1 par ces groupes acétyle. Nombre des sites modifiés se concentrent dans deux régions importantes : l’une qui aide JAK1 à s’ancrer sur les récepteurs et une autre qui assure sa fonction de kinase — l’étape chimique qui transforme les signaux en action. Lorsqu’il est acétylé par Lem17, la capacité de JAK1 à utiliser des molécules énergétiques et à phosphoryler des substrats chute fortement, ce qui signifie que la cascade de signalisation est efficacement coupée.
Une molécule de l’hôte active l’arme bactérienne
L’étude explique aussi comment Lem17 lui‑même n’est activé qu’à l’intérieur des cellules de l’hôte. Des travaux structuraux ont révélé que Lem17 se lie fortement à l’inositol hexaphosphate (IP6), une petite molécule naturellement abondante dans les cellules eucaryotes mais absente des bactéries. L’IP6 s’insère dans une poche chargée positivement de Lem17 et se verrouille sous un domaine « couvercle » flexible. Sans IP6, Lem17 ne peut pas lier son donneur d’acétyle et reste inactif. Cette exigence garantit que l’activité acétyltransférase de Lem17 ne s’enclenche qu’après l’entrée de Legionella dans une cellule hôte, évitant une activation prématurée à l’intérieur de la bactérie.
Silenciement immunitaire et croissance bactérienne
En mesurant l’activité génique et les modifications protéiques dans des cellules humaines traitées par interféron, les auteurs ont montré que Lem17 atténue fortement la signalisation JAK‑STAT : la phosphorylation de STAT1 et STAT2 est réduite, et de nombreux gènes stimulés par les interférons ne s’activent pas. Les cellules dont JAK1 est supprimé ou silencé deviennent plus perméables à la réplication de Legionella, reproduisant l’effet de Lem17. Ensemble, ces résultats soutiennent un modèle clair : Legionella utilise Lem17 pour se lier à JAK1 et le masquer chimiquement, bloquant la transmission des signaux de cytokines et permettant à la bactérie de prospérer à l’intérieur d’une niche cellulaire protégée.
Pourquoi cela compte pour l’infection et la thérapie
Ce travail met au jour une façon précise qu’un pathogène bactérien a de désactiver l’un des interrupteurs d’alarme centraux du système immunitaire. En montrant que Lem17 fait à la fois concurrence aux récepteurs pour l’accès à JAK1 et inactiver chimiquement la fonction de JAK1, l’étude met en lumière la voie JAK‑STAT comme un champ de bataille essentiel dans les infections bactériennes, pas seulement dans les maladies virales. Comprendre ce mécanisme pourrait orienter des stratégies futures pour renforcer les défenses de l’hôte, par exemple en concevant des médicaments qui bloquent l’interaction de Lem17 avec JAK1 ou empêchent son activité d’acétyltransférase, restaurant ainsi la capacité de la cellule à monter une réponse immunitaire robuste.
Citation: Chen, TT., Zheng, SR., Yang, B. et al. A bacterial YopJ-family acetyltransferase suppresses host immune response by Nε-acetylation of JAK1. Nat Commun 17, 2910 (2026). https://doi.org/10.1038/s41467-026-69623-6
Mots-clés: Legionella pneumophila, signalisation JAK-STAT, effecteurs bactériens, acétylation des protéines, immunité innée