Clear Sky Science · pl
Bakteryjna acetylotransferaza z rodziny YopJ tłumi odpowiedź immunologiczną gospodarza przez Nε-acetylację JAK1
Jak bakterie uciszają alarmy organizmu
Gdy szkodliwe mikroby atakują, nasze komórki zwykle uruchamiają alarm, uwalniając przekaźniki chemiczne, które włączają silne mechanizmy przeciwwirusowe i przeciwbakteryjne. Badanie to pokazuje, jak bakteria wywołująca zapalenie płuc, Legionella pneumophila, wykorzystuje niewielkie białko o nazwie Lem17, by stłumić ten alarm u źródła. Poprzez manipulację kluczowym przełącznikiem komórkowym — szlakiem JAK‑STAT — bakteria potrafi ominąć obronę immunologiczną i namnażać się wewnątrz naszych komórek.
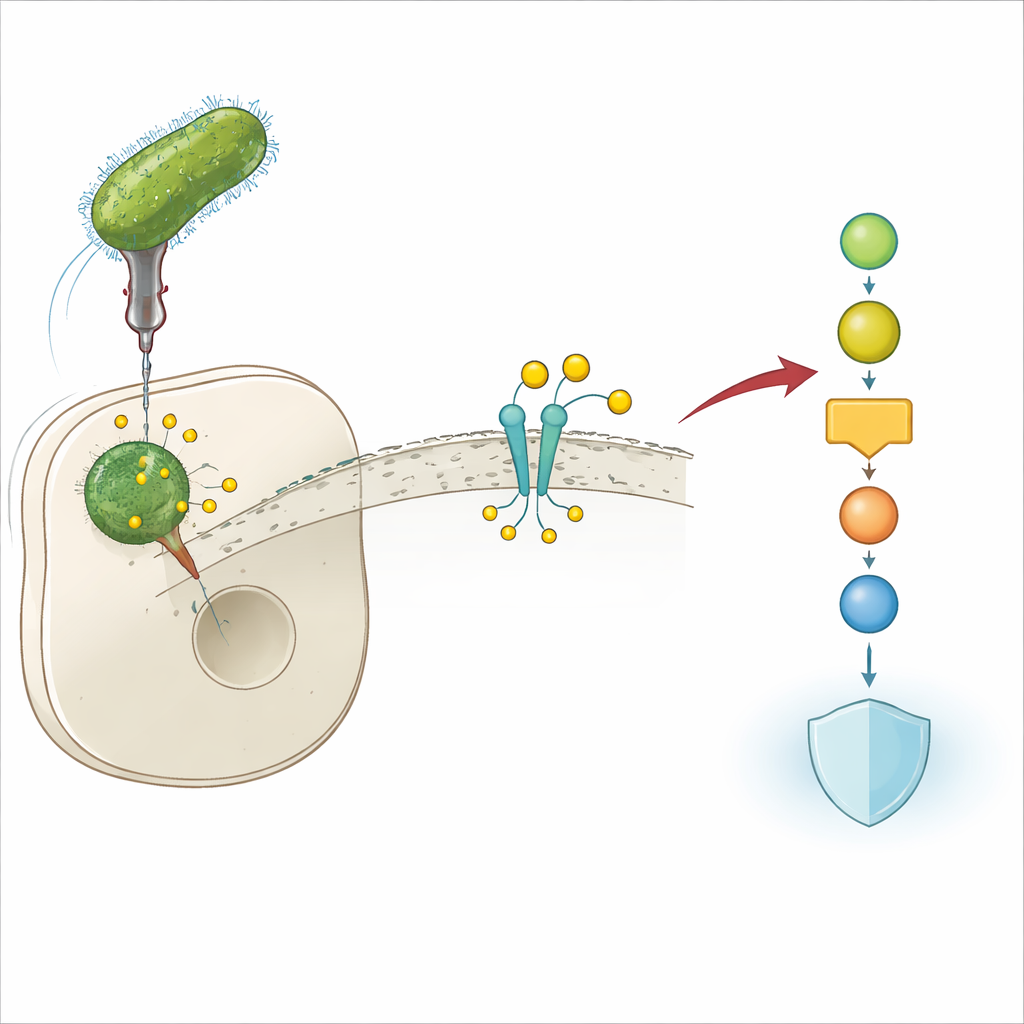
Bakteryjny trik pozwalający unikać obrony
Legionella pneumophila żyje wewnątrz ludzkich komórek układu odpornościowego i może powodować ciężką postać zapalenia płuc znaną jako choroba legionistów. Aby przetrwać w tym wrogim środowisku, bakteria wstrzykuje do komórki gospodarza liczne białka „efektorowe”. Efektory te przebudowują kluczowe obwody komórkowe, które w przeciwnym razie blokowałyby infekcję. Autorzy odkryli, że jeden z tych efektorów, Lem17, jest niezbędny do wzrostu Legionelli wewnątrz komórek: po usunięciu genu lem17 bakterie słabo replikują się w modelach komórek mysich i ludzkich. To natychmiast zasugerowało, że Lem17 odgrywa centralną rolę w unieszkodliwianiu obrony gospodarza.
Atak na przełącznik sygnałowy organizmu
Nasze komórki polegają na szlaku JAK‑STAT do przetwarzania sygnałów alarmowych, takich jak interferony i interleukiny, na szeroką odpowiedź przeciwwirusową i przeciwbakteryjną. Te cząsteczki sygnałowe wiążą się z receptorami na powierzchni komórki, które następnie rekrutują enzym zwany JAK1. JAK1 aktywuje białka STAT, które przemieszczają się do jądra i uruchamiają setki genów ochronnych. Badacze wykazali, że Lem17 celuje specyficznie w JAK1. Wiąże się bezpośrednio z obszarem JAK1, który normalnie rozpoznaje receptory cytokinowe, skutecznie konkurując z tymi receptorami i blokując prawidłowe rekrutowanie JAK1 w momencie nadejścia sygnału zagrożenia.
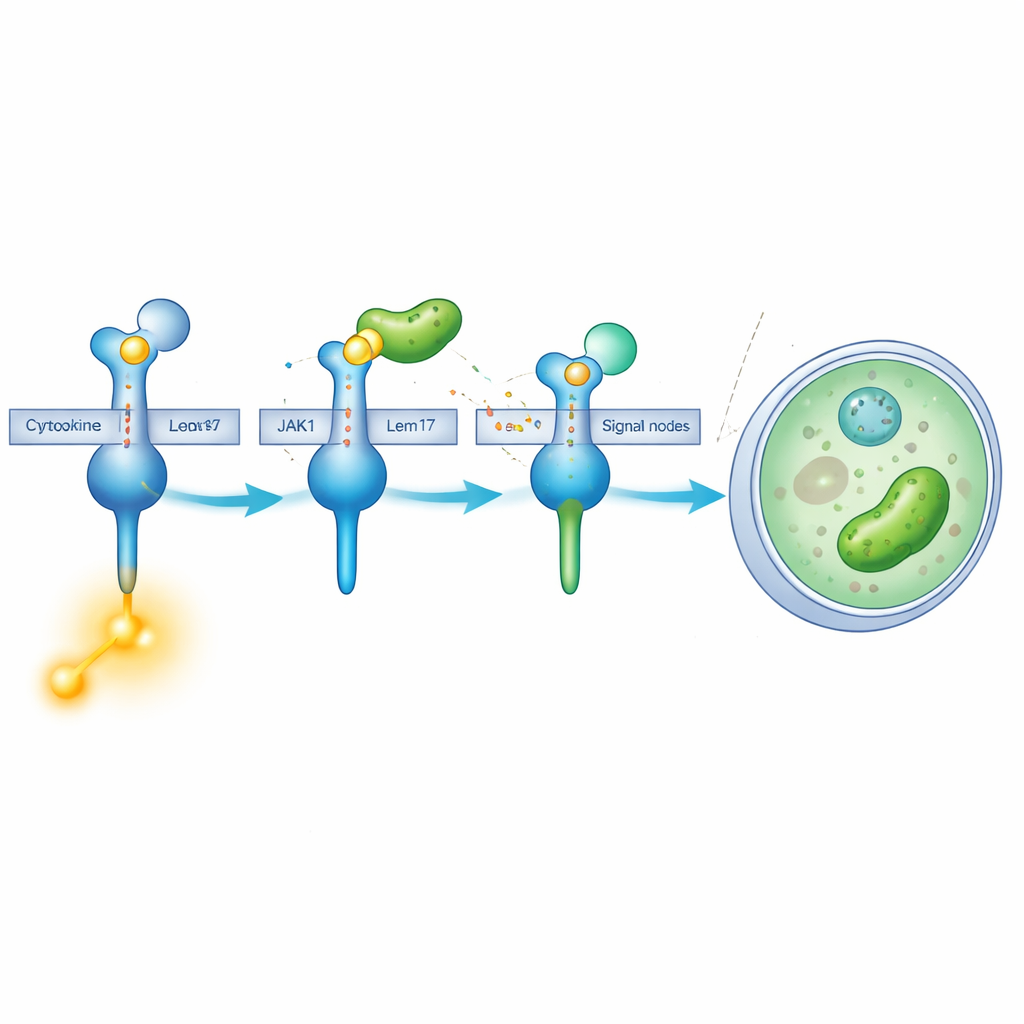
Chemiczne „maskowanie” kluczowego enzymu
Lem17 robi więcej niż tylko przeszkadza. Należy do rodziny enzymów, które przyłączają małe grupy acetylowe do innych białek. W oparciu o eksperymenty komórkowe i spektrometrię mas zespół wykrył, że Lem17 ozdabia kilka reszt lizyny w JAK1 tymi znakami acetylacji. Wiele zmodyfikowanych miejsc skupia się w dwóch ważnych regionach: jednym pomagającym JAK1 dokować do receptorów i drugim odpowiedzialnym za funkcję kinazy — chemiczny etap, który przekształca sygnały w działanie. Gdy JAK1 zostaje acetylowany przez Lem17, jego zdolność do wykorzystania cząsteczek energetycznych i fosforylowania substratów gwałtownie maleje, co oznacza, że kaskada sygnałowa jest skutecznie wyłączona.
Molekuła gospodarza włącza bakteryjną broń
Badanie wyjaśnia także, dlaczego Lem17 jest aktywowany dopiero wewnątrz komórek gospodarza. Analizy strukturalne ujawniły, że Lem17 silnie wiąże inozytol heksafosforan (IP6), małą cząsteczkę naturalnie obfitującą w komórkach eukariotycznych, ale nieobecną w bakteriach. IP6 mieści się w dodatnio naładowanej kieszeni Lem17 i zakleszcza się pod elastyczną domeną „pokrywy”. Bez IP6 Lem17 nie może wiązać swego donorowego czynnika acetylowego i pozostaje nieaktywny. To wymaganie zapewnia, że aktywność acetylotransferazowa Lem17 włącza się dopiero po wejściu Legionelli do komórki gospodarza, zapobiegając przedwczesnej aktywacji wewnątrz bakterii.
Uciszanie odporności i wzrost bakterii
Mierząc aktywność genów i modyfikacje białek w ludzkich komórkach traktowanych interferonem, autorzy pokazali, że Lem17 silnie tłumi sygnalizację JAK‑STAT: fosforylacja STAT1 i STAT2 jest zmniejszona, a wiele genów stymulowanych przez interferon nie zostaje włączonych. Komórki, w których JAK1 jest usunięty lub wyciszony, stają się bardziej podatne na replikację Legionelli, naśladując efekt Lem17. Razem wyniki te wspierają jasny model: Legionella używa Lem17 do wiązania i chemicznego maskowania JAK1, blokując przekazywanie sygnałów cytokinowych i pozwalając bakterii rozkwitać wewnątrz chronionej niszy komórkowej.
Dlaczego to ma znaczenie dla zakażeń i terapii
Praca ujawnia precyzyjny sposób, w jaki patogen bakteryjny dezaktywuje jeden z centralnych przełączników alarmowych układu odpornościowego. Pokazując, że Lem17 zarówno konkuruje z receptorami o dostęp do JAK1, jak i chemicznie inaktywuje funkcję JAK1, badanie uwydatnia szlak JAK‑STAT jako kluczowe pole bitwy w zakażeniach bakteryjnych, nie tylko wirusowych. Zrozumienie tego mechanizmu może ukierunkować przyszłe strategie wzmacniania obrony gospodarza, na przykład przez projektowanie leków blokujących interakcję Lem17 z JAK1 lub hamujących jego aktywność acetylotransferazową, przywracając w ten sposób komórce zdolność do uruchomienia silnej odpowiedzi immunologicznej.
Cytowanie: Chen, TT., Zheng, SR., Yang, B. et al. A bacterial YopJ-family acetyltransferase suppresses host immune response by Nε-acetylation of JAK1. Nat Commun 17, 2910 (2026). https://doi.org/10.1038/s41467-026-69623-6
Słowa kluczowe: Legionella pneumophila, szlak JAK-STAT, bakterialne efektory, acetylacja białek, odporność wrodzona