Clear Sky Science · sv
Orsaker och konsekvenser av experimentell variation i tillfällig uttryckning i Nicotiana benthamiana
Varför små växtexperiment spelar roll
Många genombrott inom växtvetenskap och biobaserad tillverkning börjar med ett enkelt knep: att tillfälligt förvandla växtblad till miniatyrtestfabriker. I arten Nicotiana benthamiana kan forskare snabbt införa ny DNA och se vad som händer inom några dagar. Denna hastighet har gjort växten till ett arbetsdjur för att testa gener, bygga metaboliska vägar och prototypa nya biologiska konstruktioner. Men precis som när man bakar samma recept i olika ugnar kan resultaten variera från körning till körning. Denna studie ställer en i grunden enkel fråga med stora konsekvenser: hur konsekventa är dessa snabba växttester, och vad kan forskare göra för att tämja brus så att de kan lita på subtila skillnader i sina data?
Hur en favoritväxt kan ge olika svar
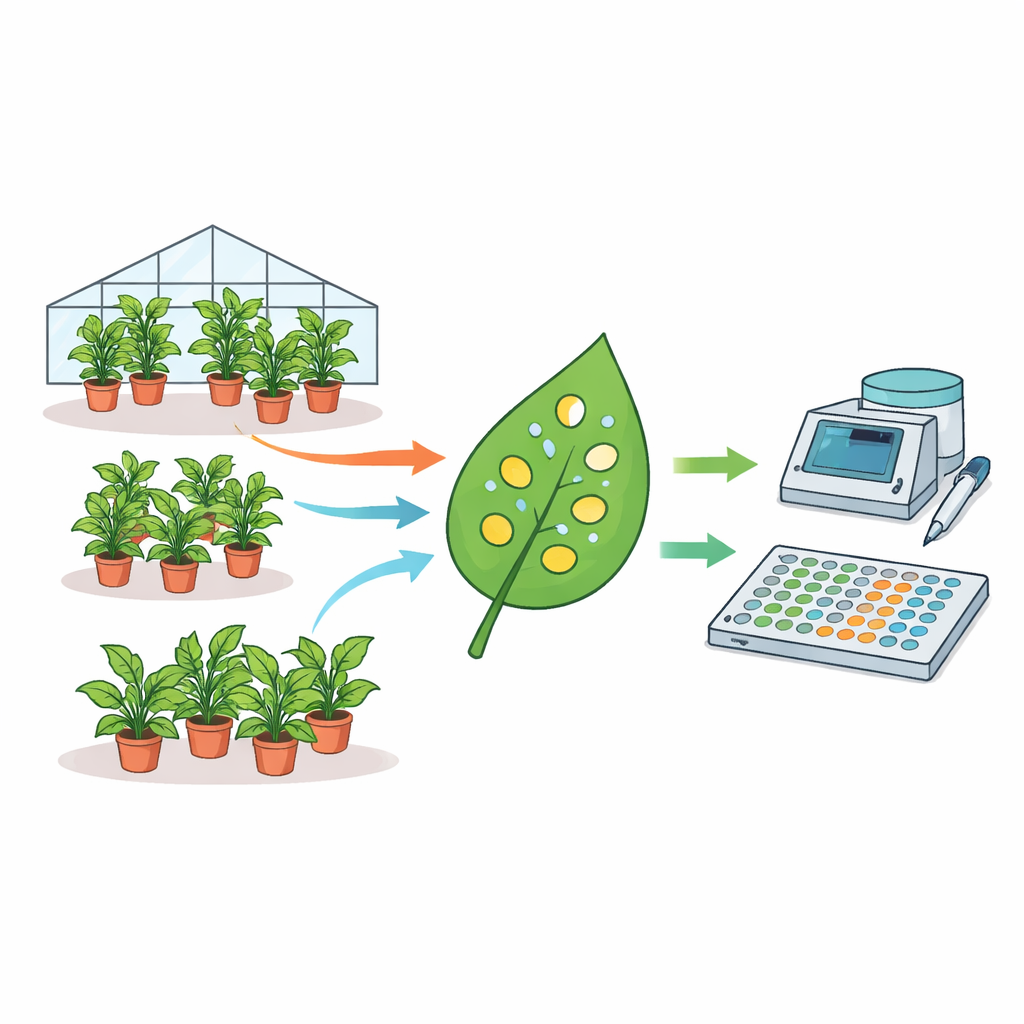
Författarna sammanställde en ovanligt stor datamängd: mätningar från 1915 individuella N. benthamiana‑plantor insamlade under nästan tre år. Varje planta infiltrerades med Agrobacterium‑bakterier som bar en fluorescerande rapportörgen, och små skivor togs från blad och lästes med en platteläsare. Med statistiska modeller bröt de ned varifrån variationen kommer. De fann att skillnader mellan plantbatchar, mellan plantor inom en batch och till och med mellan skivor tagna från samma blad alla bidrog avsevärt till den totala spridningen i fluorescens. Faktum är att medeluttrycksnivåer kunde skilja sig upp till fyra gånger mellan till synes identiska experiment utförda på olika dagar. Faktorer som plantålder och bevattningsvolym påverkade också signalstyrkan, medan tid på dagen för provtagning inte gjorde det.
Test av knep för att jämna ut bruset
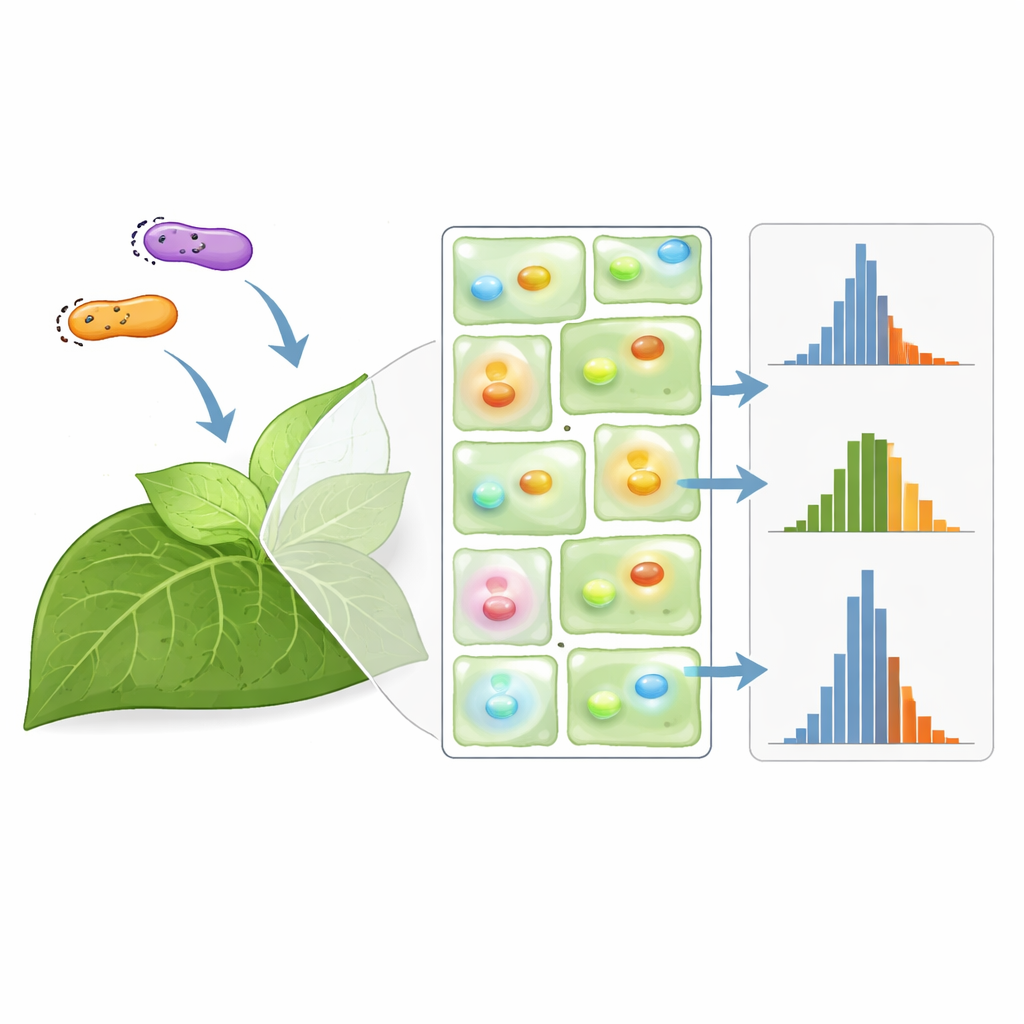
För att minska denna spridning använder många laboratorier en ”normaliseringsgen”: de levererar två fluorescerande rapportörer samtidigt och analyserar förhållandet mellan deras signaler i hopp om att delade källor till brus tar ut varandra. Teamet jämförde systematiskt 17 sätt att samleverera dessa dubbla rapportörer, inklusive att blanda separata bakteriestammar, stapla båda generna på samma DNA‑segment och använda enstaka stammar som bär två plasmider. De visade att alla dessa strategier kan förändra baslinjeuttrycksnivåer, ibland dramatiskt, beroende på genorientering och plasmidkopietal. Viktigt är att de flesta — men inte alla — normaliseringsscheman minskade variationen jämfört med att mäta en enda rapportör, där en enkel co‑infiltrering av två liknande plasmider framträdde som ett av de mest effektiva alternativen.
När hjälpsamma korrigeringar slår tillbaka
Berättelsen visade sig vara mer nyanserad när teamet undersökte promotorer — DNA‑brytare som styr hur starkt varje gen slås på. De testade kombinationer av svaga, medelstarka och starka promotorer som drev de två fluorescerande proteinerna. Normalisering fungerade bäst när båda rapportörerna använde exakt samma promotor; under dessa förhållanden visade kvoten mycket mindre spridning. Men när promotorerna skiljde sig åt blev kvoten ibland mer oberäknelig än den råa signalen från en enda gen, vilket faktiskt försämrade den statistiska styrkan. Författarna fann också att justering av tätheten hos bakteriestammarna huvudsakligen ändrade hur ljusa signalerna var, inte hur variabla de var. Överlag visar arbetet att normalisering inte är en universallösning: dess framgång beror starkt på detaljerna i konstruktets design.
Hur många plantor räcker?
Citering: Tang, S.N., Szarzanowicz, M.J., Lanctot, A. et al. Causes and consequences of experimental variation in Nicotiana benthamiana transient expression. Nat Commun 17, 2772 (2026). https://doi.org/10.1038/s41467-026-69458-1
Nyckelord: Nicotiana benthamiana, tillfällig uttryckning, syntetisk biologi, experimentell variabilitet, Agrobacterium