Clear Sky Science · es
Causas y consecuencias de la variación experimental en la expresión transitoria de Nicotiana benthamiana
Por qué importan los experimentos vegetales en pequeña escala
Muchos avances en la ciencia vegetal y en la fabricación basada en biotecnología comienzan con un truco sencillo: convertir temporalmente hojas de plantas en pequeñas fábricas de ensayo. En la especie Nicotiana benthamiana, los científicos pueden introducir rápidamente nuevo ADN y observar qué ocurre en cuestión de días. Esta rapidez ha convertido a la planta en una herramienta de referencia para probar genes, construir vías metabólicas y prototipar nuevos diseños biológicos. Pero, como hornear la misma receta en distintos hornos, los resultados pueden variar de una tanda a otra. Este estudio plantea una pregunta aparentemente simple con grandes consecuencias: ¿qué tan coherentes son estas pruebas rápidas en plantas y qué pueden hacer los investigadores para domar el ruido y confiar en diferencias sutiles de sus datos?
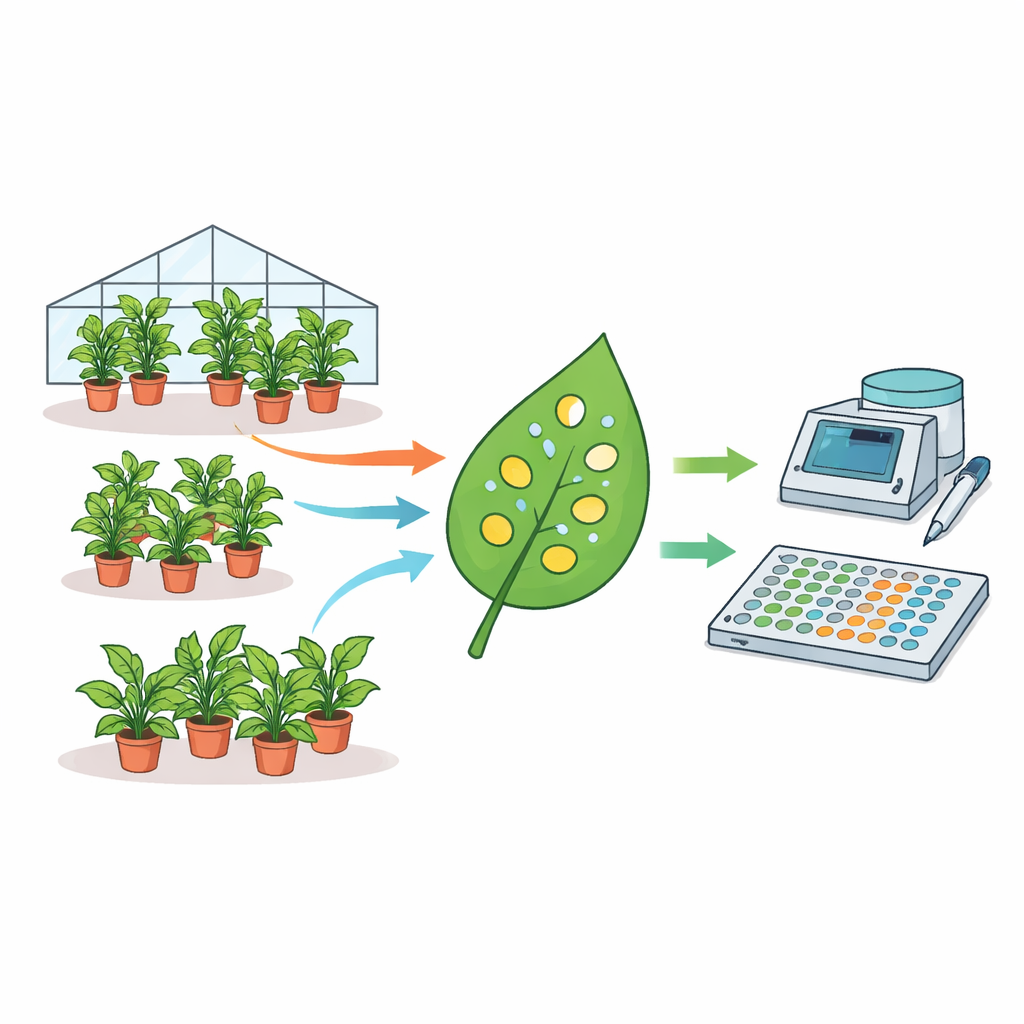
Cómo una planta de ensayo favorita puede dar respuestas diferentes
Los autores reunieron un conjunto de datos inusualmente grande: mediciones de 1915 plantas individuales de N. benthamiana recogidas a lo largo de casi tres años. Cada planta fue infiltrada con bacterias Agrobacterium portadoras de un gen reportero fluorescente, y se tomaron pequeños discos de las hojas que se midieron en un lector de placas. Empleando modelos estadísticos, desglosaron de dónde proviene la variabilidad. Encontraron que las diferencias entre lotes de plantas, entre plantas dentro de un mismo lote e incluso entre discos tomados de la misma hoja contribuyeron de forma sustancial a la dispersión global de la fluorescencia. De hecho, los niveles medios de expresión podían diferir hasta cuatro veces entre experimentos nominalmente idénticos realizados en distintos días. Factores como la edad de la planta y el volumen de riego también influyeron en la intensidad de la señal, mientras que la hora del día del muestreo no lo hizo.
Probando trucos para reducir el ruido
Para reducir esta dispersión, muchos laboratorios usan un gen “normalizador”: entregan dos reporteros fluorescentes a la vez y analizan la razón entre sus señales, con la esperanza de que las fuentes de ruido compartidas se cancelen. El equipo comparó sistemáticamente 17 formas de coentregar estos reporteros duales, incluyendo mezclar cepas bacterianas separadas, apilar ambos genes en el mismo segmento de ADN y usar cepas únicas que portan dos plásmidos. Mostraron que todas estas estrategias pueden cambiar los niveles basales de expresión, a veces de forma drástica, dependiendo de la orientación del gen y del número de copias del plásmido. Es importante que la mayoría—pero no todas—las estrategias de normalización redujeron la variación en comparación con medir un único reportero, y que una co-infiltración simple de dos plásmidos similares surgió como una de las opciones más efectivas.
Cuando las correcciones útiles salen mal
La historia resultó ser más matizada cuando el equipo examinó los promotores —los interruptores de ADN que controlan la fuerza con que se activa cada gen. Probaron combinaciones de promotores débiles, medios y fuertes que impulsaban las dos proteínas fluorescentes. La normalización funcionó mejor cuando ambos reporteros usaban exactamente el mismo promotor; en esas condiciones, la razón mostró mucha menos dispersión. Pero cuando los promotores eran distintos, la razón a veces se volvió más errática que la señal cruda de un único gen, empeorando en realidad la potencia estadística. Los autores también observaron que ajustar la densidad de las cepas bacterianas principalmente cambiaba el brillo de las señales, no su variabilidad. En conjunto, el trabajo muestra que la normalización no es una solución universal: su éxito depende en gran medida de los detalles del diseño del constructo.
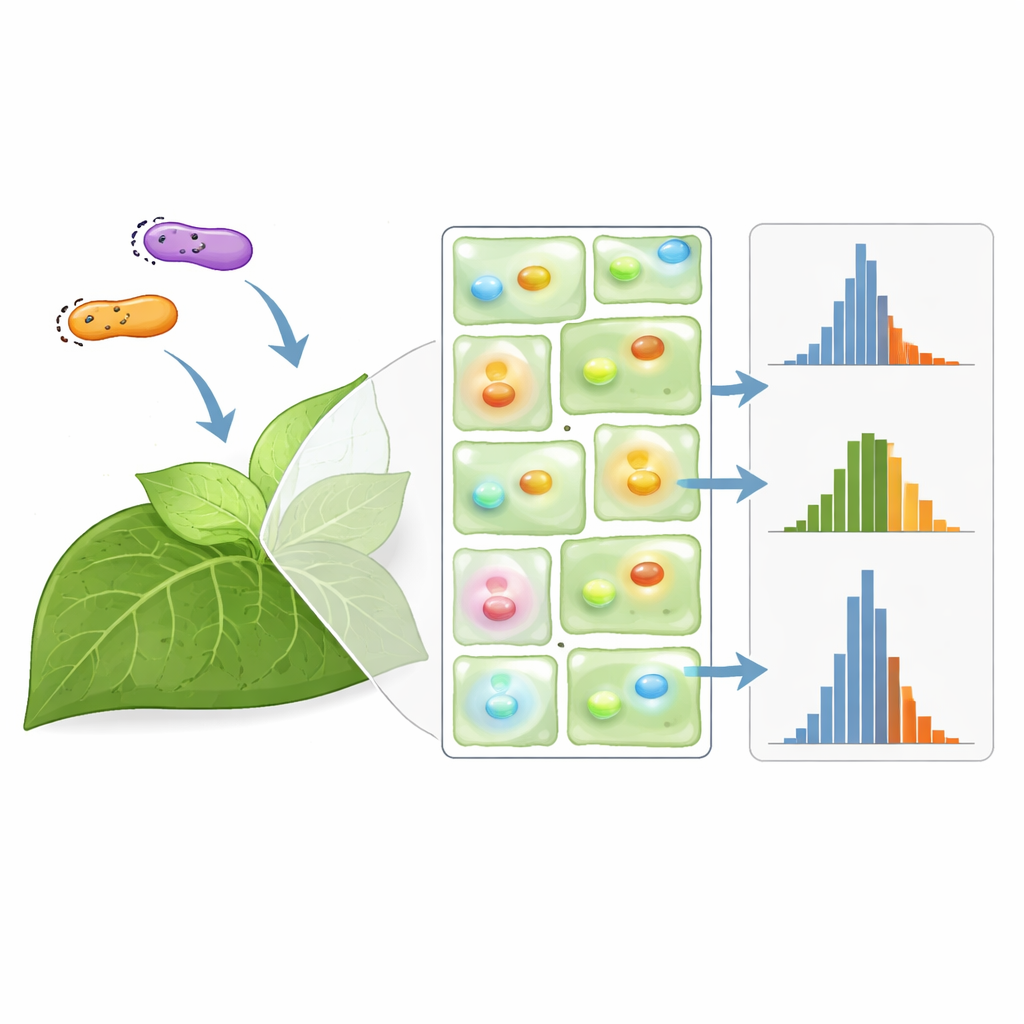
¿Cuántas plantas son suficientes?
Con su amplio conjunto de datos, los investigadores construyeron una simulación Monte Carlo para modelar cómo se propaga la variabilidad en experimentos típicos. La usaron para plantear una pregunta que todo experimentalista se hace: dado un cierto nivel de ruido, ¿cuántas plantas necesitas para detectar de forma fiable una diferencia real entre dos constructos? Para cepas comunes de Agrobacterium, encontraron que efectos mayores de aproximadamente un 50 por ciento pueden detectarse con solo unas pocas plantas, mientras que discernir diferencias menores del 20 por ciento puede requerir docenas, a veces más de lo práctico. Una normalización cuidadosamente elegida puede reducir ligeramente estos números, especialmente cuando se usan promotores idénticos y solo hay pocas plantas disponibles, pero en algunos diseños ofrece poca ventaja.
Qué significa esto para la ingeniería vegetal futura
Para los no especialistas, el mensaje clave es que incluso en un sistema vegetal muy popular y cómodo, el ruido experimental es tanto sustancial como manejable. El estudio cartografía de dónde proviene la variación, muestra que los métodos de corrección populares pueden ayudar o perjudicar según cómo se construyan, y proporciona directrices sencillas de análisis de potencia para planificar experimentos. En términos cotidianos, dice a los biólogos vegetales cómo dimensionar sus estudios para no confundir fluctuaciones aleatorias con efectos biológicos reales y cómo diseñar constructos reporteros que ofrezcan comparaciones más fiables. Estos conocimientos deberían convertir a N. benthamiana en una plataforma aún más fiable para probar genes rápidamente, ensamblar nuevas vías metabólicas y avanzar en la biología sintética hacia una ingeniería de sistemas vivos más predecible.
Cita: Tang, S.N., Szarzanowicz, M.J., Lanctot, A. et al. Causes and consequences of experimental variation in Nicotiana benthamiana transient expression. Nat Commun 17, 2772 (2026). https://doi.org/10.1038/s41467-026-69458-1
Palabras clave: Nicotiana benthamiana, expresión transitoria, biología sintética, variabilidad experimental, Agrobacterium