Clear Sky Science · de
Ursachen und Folgen experimenteller Variabilität bei transienter Expression in Nicotiana benthamiana
Warum winzige Pflanzenexperimente wichtig sind
Viele Durchbrüche in der Pflanzenwissenschaft und biobasierter Produktion beginnen mit einem einfachen Trick: Blattstücke werden kurzzeitig zu winzigen Testfabriken umfunktioniert. Bei der Art Nicotiana benthamiana können Forschende schnell neue DNA einbringen und innerhalb weniger Tage beobachten, was passiert. Diese Geschwindigkeit hat die Pflanze zu einem Arbeitspferd gemacht, um Gene zu testen, Stoffwechselwege aufzubauen und neue biologische Entwürfe zu prototypisieren. Aber wie beim Backen desselben Rezepts in unterschiedlichen Öfen können die Ergebnisse von Versuch zu Versuch variieren. Diese Studie stellt eine auf den ersten Blick einfache Frage mit großen Konsequenzen: Wie konsistent sind diese schnellen Pflanzentests, und was können Forschende tun, um das Rauschen zu zähmen, damit sie subtilen Unterschieden in ihren Daten vertrauen können?
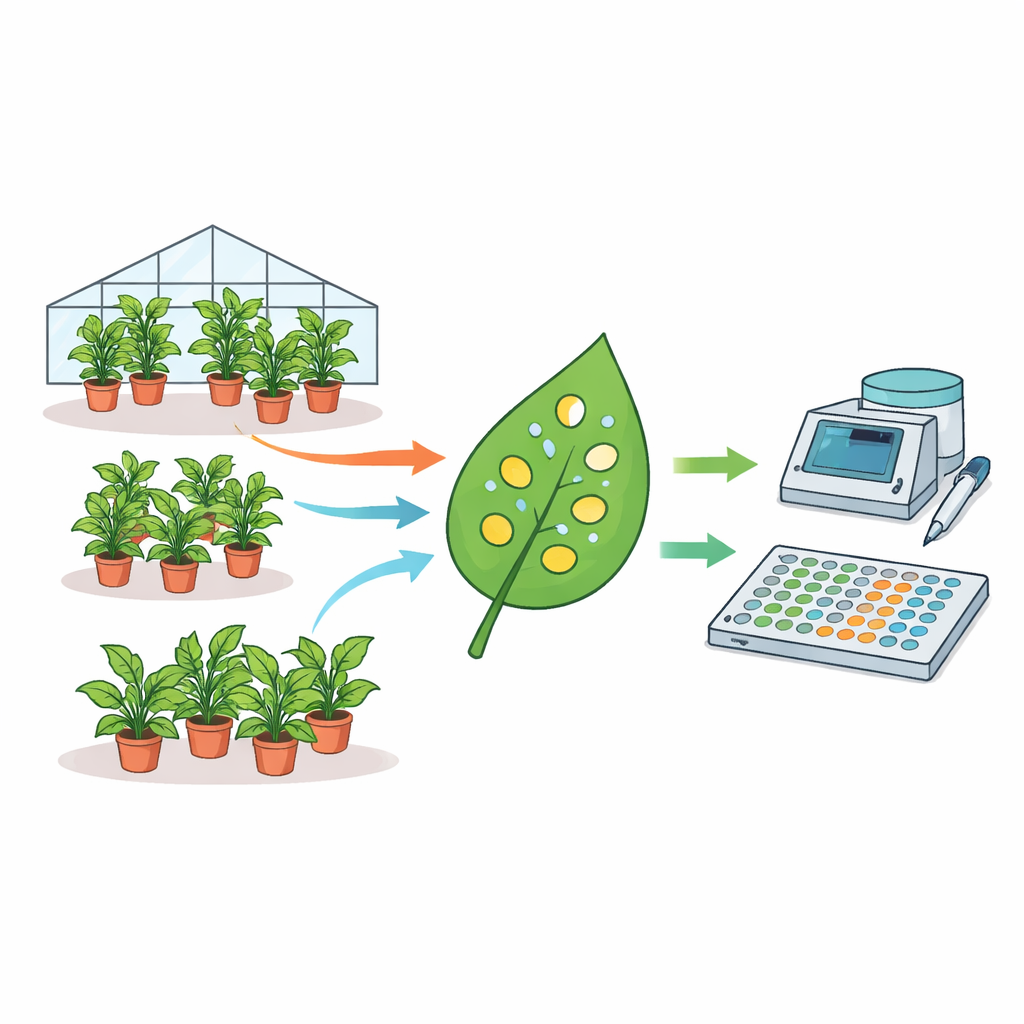
Wie eine beliebte Testpflanze unterschiedliche Antworten liefern kann
Die Autorinnen und Autoren haben einen ungewöhnlich großen Datensatz zusammengestellt: Messwerte von 1915 einzelnen N. benthamiana-Pflanzen, gesammelt über fast drei Jahre. Jede Pflanze wurde mit Agrobacterium-Bakterien infiltriert, die ein fluoreszierendes Reportergen trugen, und es wurden winzige Scheiben aus den Blättern ausgestanzt und auf einem Plattenleser ausgelesen. Mithilfe statistischer Modelle zerlegten sie, woher die Variabilität stammt. Sie fanden heraus, dass Unterschiede zwischen Pflanzenchargen, zwischen Pflanzen innerhalb einer Charge und sogar zwischen Scheiben derselben Blatteinheit alle wesentlich zur Gesamtabweichung in der Fluoreszenz beitrugen. Tatsächlich konnten die mittleren Expressionsniveaus zwischen nominal identischen Experimenten an verschiedenen Tagen um das Vierfache variieren. Faktoren wie Pflanzenalter und Wassermenge beeinflussten die Signalstärke, während die Tageszeit der Probenahme dies nicht tat.
Strategien testen, um das Rauschen zu glätten
Um diese Streuung zu verringern, nutzen viele Labore ein „Normalisierungsgen“: Sie liefern zwei fluoreszierende Reporter gleichzeitig und analysieren das Verhältnis ihrer Signale in der Hoffnung, dass gemeinsame Störquellen sich gegenseitig aufheben. Das Team verglich systematisch 17 Methoden zur gemeinsamen Abgabe dieser Dual-Reporter, darunter das Mischen separater Bakterienstämme, das Stapeln beider Gene auf demselben DNA-Abschnitt und die Verwendung einzelner Stämme, die zwei Plasmide tragen. Sie zeigten, dass alle diese Strategien die Basisausprägung verändern können, manchmal dramatisch, abhängig von Genorientierung und Plasmidkopienzahl. Wichtig ist, dass die meisten — aber nicht alle — Normalisierungsschemata die Variation gegenüber der Messung eines einzelnen Reporters verringerten; eine einfache Ko-Infiltration zweier ähnlicher Plasmide erwies sich als eine der effektivsten Optionen.
Wenn hilfreiche Korrekturen nach hinten losgehen
Die Geschichte erwies sich als nuancierter, als das Team Promotoren — die DNA-Schalter, die steuern, wie stark ein Gen eingeschaltet wird — untersuchte. Sie testeten Kombinationen aus schwachen, mittleren und starken Promotoren, die die beiden fluoreszierenden Proteine antreiben. Die Normalisierung funktionierte am besten, wenn beide Reporter exakt denselben Promotor verwendeten; unter diesen Bedingungen zeigte das Verhältnis deutlich weniger Streuung. Wenn die Promotoren jedoch unterschiedlich waren, wurde das Verhältnis gelegentlich unberechenbarer als das Rohsignal eines einzelnen Gens und verschlechterte damit die statistische Aussagekraft. Die Forschenden fanden außerdem heraus, dass die Anpassung der Dichte der Bakterienstämme vor allem die Helligkeit der Signale veränderte, nicht aber deren Variabilität. Insgesamt zeigt die Arbeit, dass Normalisierung kein Allheilmittel ist: Ihr Erfolg hängt stark von den Details des Konstrukt-Designs ab.
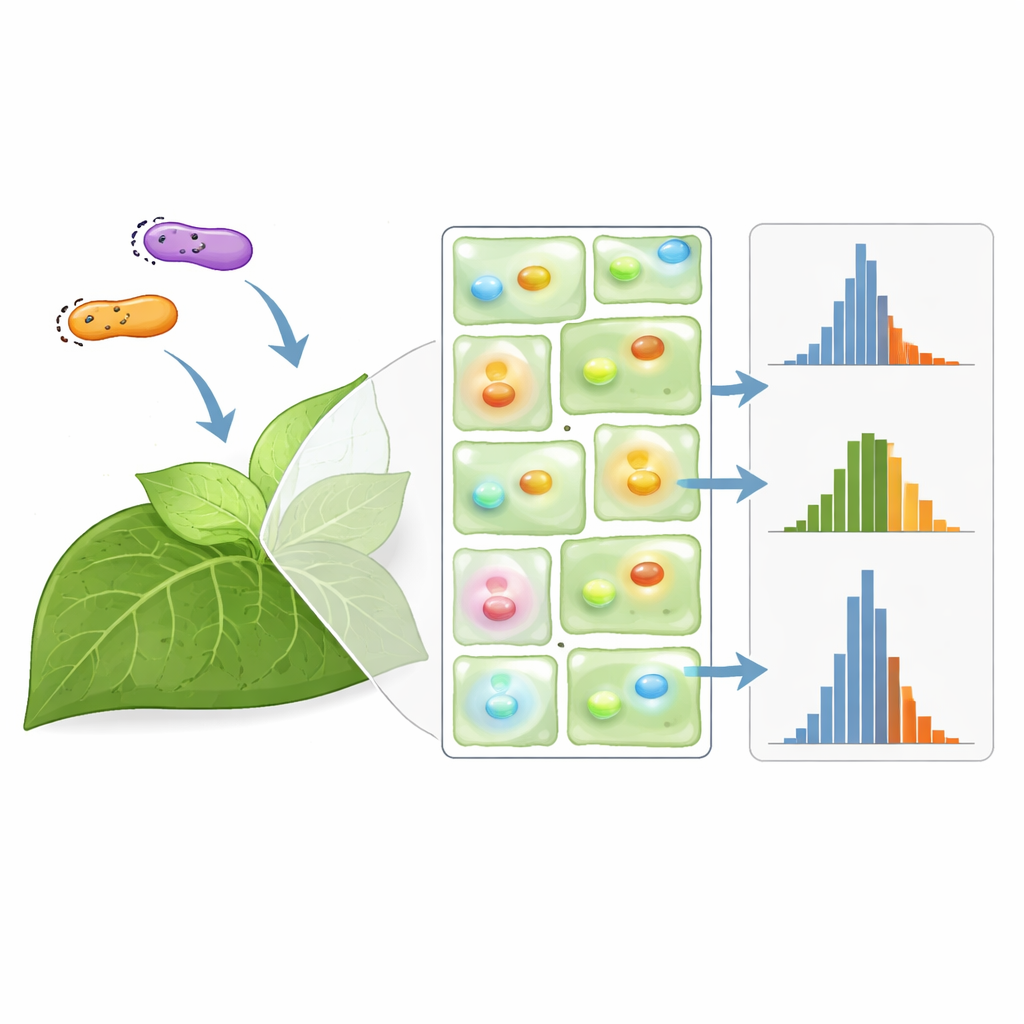
Wie viele Pflanzen sind genug?
Mit ihrem großen Datensatz bauten die Forschenden eine Monte-Carlo-Simulation, um zu modellieren, wie Variabilität sich durch typische Experimente fortpflanzt. Damit stellten sie eine Frage, die sich jeder Experimentator stellt: Bei einem bestimmten Rauschpegel, wie viele Pflanzen braucht man, um zuverlässig einen echten Unterschied zwischen zwei Konstrukten zu erkennen? Für gängige Agrobacterium-Stämme stellten sie fest, dass Effekte von mehr als etwa 50 Prozent bereits mit nur wenigen Pflanzen detektiert werden können, während Unterschiede unter 20 Prozent Dutzende Pflanzen erfordern können — manchmal mehr, als praktisch möglich ist. Sorgfältig gewählte Normalisierungen können diese Zahlen leicht reduzieren, insbesondere wenn identische Promotoren verwendet werden und nur wenige Pflanzen zur Verfügung stehen, aber in manchen Designs bietet sie kaum einen Vorteil.
Was das für die zukünftige Pflanzenentwicklung bedeutet
Für Nicht-Spezialisten lautet die Kernbotschaft: Selbst in einem beliebten, sehr praktischen Pflanzensystem ist das experimentelle Rauschen sowohl erheblich als auch beherrschbar. Die Studie kartiert, woher Variation stammt, zeigt, dass gängige Korrekturmöglichkeiten je nach Aufbau helfen oder schaden können, und liefert einfache Richtlinien zur Power-Analyse für die Planung von Experimenten. Alltagssprachlich sagt sie Pflanzenbiologinnen und -biologen, wie sie ihre Studien dimensionieren, damit sie zufällige Schwankungen nicht mit echten biologischen Effekten verwechseln, und wie sie Reporter-Konstrukte so gestalten, dass sie vertrauenswürdigere Vergleiche liefern. Diese Erkenntnisse sollten N. benthamiana zu einer noch verlässlicheren Plattform machen, um Gene schnell zu testen, neue Stoffwechselwege zusammenzustellen und die synthetische Biologie hin zu vorhersehbarerer Technik lebender Systeme voranzubringen.
Zitation: Tang, S.N., Szarzanowicz, M.J., Lanctot, A. et al. Causes and consequences of experimental variation in Nicotiana benthamiana transient expression. Nat Commun 17, 2772 (2026). https://doi.org/10.1038/s41467-026-69458-1
Schlüsselwörter: Nicotiana benthamiana, transiente Expression, synthetische Biologie, experimentelle Variabilität, Agrobacterium